
【題目】如圖是CO2生產甲醇的能量變化示意圖。下列說法正確的是( )
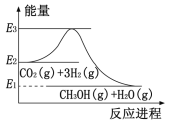
A.E2-E1是該反應的反應熱
B.E3-E1是該反應的反應熱
C.該反應放熱,在常溫常壓下就能進行
D.實現變廢為寶,且有利于控制溫室效應
 波波熊暑假作業江西人民出版社系列答案
波波熊暑假作業江西人民出版社系列答案 學而優暑期銜接南京大學出版社系列答案
學而優暑期銜接南京大學出版社系列答案 Happy holiday歡樂假期暑假作業廣東人民出版社系列答案
Happy holiday歡樂假期暑假作業廣東人民出版社系列答案科目:高中化學 來源: 題型:
【題目】常溫下,下列各溶液中微粒的物質的量濃度關系正確的是
①c(NH![]() )相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液中:c(NH4HSO4)>c[(NH4)2SO4]>c(NH4Cl)
)相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液中:c(NH4HSO4)>c[(NH4)2SO4]>c(NH4Cl)
②向醋酸鈉溶液中加入適量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
③1.0mol/LNa2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3)
④某二元弱酸的酸式鹽NaHA溶液中:c(H+)+c(Na+)=c(OH-)+c(HA-)+c(A2-)
⑤將pH=6的H2SO4稀釋1000倍后,c(H+)=200c(SO![]() )
)
A.①②B.③⑤C.④⑤D.②④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為測定某樣品中所含晶體FeSO47H2O的質量分數,取晶體樣品ag,溶于稀硫酸配成100.00mL溶液,取出20.00mL溶液,用KMnO4溶液滴定(雜質與KMnO4不反應)。若消耗0.2000molL-1KMnO4溶液20.00mL,所得晶體中FeSO47H2O的質量分數為__(用a表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知在2L的密閉容器中進行如下可逆反應,各物質的有關數據如下:
![]()
起始物質的量濃度/![]() :1.5 1 0
:1.5 1 0
2s末物質的量濃度/![]() :0.9 0.8 0.4
:0.9 0.8 0.4
請回答下列問題。
①該可逆反應的化學方程式可表示為______。
②用物質B來表示![]() 的平均反應速率為______。
的平均反應速率為______。
③從反應開始到2s末,A的轉化率為______。
④下列事實能夠說明上述反應在該條件下已經達到化學平衡狀態的是______(填序號)
A.![]()
B.容器內氣體的總壓強保持不變
C容器內氣體的密度不變
D.![]()
E.容器內氣體C的物質的量分數保持不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2SO2+O2![]() 2SO3是工業制硫酸的一步重要反應,下列說法正確的是
2SO3是工業制硫酸的一步重要反應,下列說法正確的是
A. 使用催化劑能改變該反應限度
B. 減小SO2的濃度能加快該反應的速率
C. 升高體系溫度能加快反應速率
D. 1 mol SO2和足量的O2在一定條件下充分反應,生成1 mol SO3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】改革開放40年,“發展與保護”的方針使我國在取得了很多世界矚目的科技成果的同時,文物也得到了很好的保護。下列說法不正確的是( )
|
|
|
|
A.蛟龍號潛水器用到鈦合金,22號鈦元素屬于過渡元素 | B.港珠澳大橋水下鋼柱鑲鋅塊的防腐方法為犧牲陽極的陰極保護法 | C.除銹劑使有銹跡的銀器見新,是化學變化 | D.變形的金屬香爐整形復原,是化學變化 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學與社會、生活密切相關,對下列現象或事實的解釋正確的是( )
現象或事實 | 解釋 | |
A | 用熱的純堿溶液去油污 | Na2CO3可直接與油污反應 |
B | 漂白粉在空氣中久置變質 | 漂白粉中的CaCl2與空氣中的CO2反應生成CaCO3 |
C | 施肥時,草木灰(主要成分K2CO3)不能與NH4Cl混合使用 | K2CO3與NH4Cl在潮濕的土壤中會反應生成氨氣,降低肥效 |
D | FeCl3溶液可用于銅質印刷線路板制作 | Cu能從FeCl3溶液中把鐵還原為游離態 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列離子方程式正確的是![]()
A.石灰水與過量碳酸氫鈉溶液反應:![]()
B.硫酸氫鈉溶液中加入氫氧化鋇溶液至中性:![]()
C.氧化銅與稀硫酸反應:![]()
D.碳酸氫鈉溶液中加入鹽酸:![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期主族元素X、Y、Z、R、T的原子半徑與原子序數關系如下圖所示。R原子最外層電子數是電子層數的2倍,Y與Z能形成Z2Y、Z2Y2型離子化合物,Z與T形成的化合物Z2T能破壞水的電離平衡。下列推斷正確的是

A.原子半徑和離子半徑均滿足:Y>Z
B.氫化物的沸點不一定是:Y<R
C.最高價氧化物對應水化物的酸性:T>R
D.由X、R、Y、Z四種元素組成的化合物水溶液一定顯堿性
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com