
ĪŠŅ}─┐Ī┐Ų¹▄ćäĪ┴ę┼÷ū▓ĢrŻ¼░▓╚½ÜŌ─ęųą░l╔·Ę┤æ¬10NaN3+2KNO3=K2O+5Na2O+16N2Ī³ĪŻ╚¶ėą2molN2╔·│╔Ż¼ätŽ┬┴ą┼ąöÓš²┤_Ą─╩Ū
A. ╔·│╔44.8LN2
B. ėą0.125molKNO3▒╗č§╗»
C. N2╝╚╩Ūč§╗»«a╬’ėų╩Ū▀ĆįŁ«a╬’
D. ▐DęŲļŖūėĄ─╬’┘|Ą─┴┐×ķ10mol
ĪŠ┤░ĖĪ┐C
ĪŠĮŌ╬÷Ī┐įōĘ┤æ¬ųąNį¬╦ž╗»║Žārė╔-![]() ārĪó+5ārūā×ķ0ārŻ¼╦∙ęįč§╗»«a╬’║═▀ĆįŁ«a╬’Č╝╩ŪĄ¬ÜŌŻ¼╝┘įOėą16molĄ¬ÜŌ╔·│╔Ż¼č§╗»«a╬’╩Ū15molĪó▀ĆįŁ«a╬’╩Ū1molŻ¼╚¶ėą2molN2╔·│╔Ż¼ätģó╝ėĘ┤æ¬Ą─nŻ©KNO3Ż®=
ārĪó+5ārūā×ķ0ārŻ¼╦∙ęįč§╗»«a╬’║═▀ĆįŁ«a╬’Č╝╩ŪĄ¬ÜŌŻ¼╝┘įOėą16molĄ¬ÜŌ╔·│╔Ż¼č§╗»«a╬’╩Ū15molĪó▀ĆįŁ«a╬’╩Ū1molŻ¼╚¶ėą2molN2╔·│╔Ż¼ätģó╝ėĘ┤æ¬Ą─nŻ©KNO3Ż®=![]() =0.25molŻ¼ AŻ«ś╦£╩ĀŅørŽ┬╔·│╔Ą¬ÜŌĄ─¾wĘe×ķ44.8 LŻ¼Ą½Ņ}Ė╔ųąø]ėąšf├„Ż¼▀xĒŚAÕeš`Ż╗BŻ«Ž§╦ßŌøĄ├ļŖūėū„č§╗»ä®Č°▒╗▀ĆįŁŻ¼▀xĒŚBÕeš`Ż╗CŻ«Ė∙ō■╔Ž╩÷Ęų╬÷Ż¼N2╝╚╩Ūč§╗»«a╬’ėų╩Ū▀ĆįŁ«a╬’Ż¼▀xĒŚCš²┤_Ż╗DĪó▐DęŲļŖūėĄ─╬’┘|Ą─┴┐=3nŻ©KNO3Ż®=5Ī┴0.25mol=1.25molŻ¼▀xĒŚDÕeš`Ż╗┤░Ė▀xCĪŻ
=0.25molŻ¼ AŻ«ś╦£╩ĀŅørŽ┬╔·│╔Ą¬ÜŌĄ─¾wĘe×ķ44.8 LŻ¼Ą½Ņ}Ė╔ųąø]ėąšf├„Ż¼▀xĒŚAÕeš`Ż╗BŻ«Ž§╦ßŌøĄ├ļŖūėū„č§╗»ä®Č°▒╗▀ĆįŁŻ¼▀xĒŚBÕeš`Ż╗CŻ«Ė∙ō■╔Ž╩÷Ęų╬÷Ż¼N2╝╚╩Ūč§╗»«a╬’ėų╩Ū▀ĆįŁ«a╬’Ż¼▀xĒŚCš²┤_Ż╗DĪó▐DęŲļŖūėĄ─╬’┘|Ą─┴┐=3nŻ©KNO3Ż®=5Ī┴0.25mol=1.25molŻ¼▀xĒŚDÕeš`Ż╗┤░Ė▀xCĪŻ


 ▌p╦╔╩Ņ╝┘┐éÅ═┴ĢŽĄ┴ą┤░Ė
▌p╦╔╩Ņ╝┘┐éÅ═┴ĢŽĄ┴ą┤░Ė
| ─Ļ╝ē | Ė▀ųąšn│╠ | ─Ļ╝ē | │§ųąšn│╠ |
| Ė▀ę╗ | Ė▀ę╗├Ō┘Mšn│╠═Ų╦]ŻĪ | │§ę╗ | │§ę╗├Ō┘Mšn│╠═Ų╦]ŻĪ |
| Ė▀Č■ | Ė▀Č■├Ō┘Mšn│╠═Ų╦]ŻĪ | │§Č■ | │§Č■├Ō┘Mšn│╠═Ų╦]ŻĪ |
| Ė▀╚² | Ė▀╚²├Ō┘Mšn│╠═Ų╦]ŻĪ | │§╚² | │§╚²├Ō┘Mšn│╠═Ų╦]ŻĪ |
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐═¼£ž═¼ē║Ž┬ėąā╔Ę▌¾wĘeŽÓ═¼Ą─CO2║═O3 Ż¼ ĻPė┌╦³éāĄ─öó╩÷š²┤_Ą─╩ŪŻ© Ż®
A.ĘųūėöĄų«▒╚╩Ū1Ż║1
B.įŁūėéĆöĄ▒╚╩Ū3Ż║2
C.┘|ūėöĄ▒╚╩Ū12Ż║11
D.├▄Č╚ų«▒╚╩Ū1Ż║1
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐─│ŽĪ┴“╦ß║═ŽĪŽ§╦ߥ─╗ņ║Ž╚▄ę║200mLŻ¼ŲĮŠ∙Ęų│╔ā╔Ę▌Ż¼Ž“Ųõųąę╗Ę▌ųąųØu╝ė╚ļŃ~Ę█Ż¼ūŅČÓ─▄╚▄ĮŌ19.2g(ęčų¬Ž§╦ßų╗─▄▒╗▀ĆįŁ×ķNOÜŌ¾w)ĪŻŽ“┴Ēę╗Ę▌ųąųØu╝ė╚ļĶFĘ█Ż¼«a╔·ÜŌ¾wĄ─┴┐ļSĶFĘ█┘|┴┐į÷╝ėĄ─ūā╗»╚ńłD╦∙╩ŠĪŻŽ┬┴ąĘų╬÷╗“ĮY╣¹Õeš`Ą─╩Ū
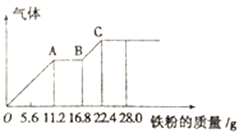
A. įŁ╗ņ║Ž╦ßę║ųąNO3-Ą─╬’┘|Ą─┴┐×ķ0.4mol B. ABČ╬Ę┤æ¬×ķ2Fe3++Fe=3Fe2+
C. ╚▄ę║ųąūŅĮK╚▄┘|×ķFeSO4 D. c(H2SO4)×ķ5mol/L
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐ęčų¬─│╚▄ę║ųą║¼ėąNa+ĪóBa2+ĪóFe3+╚²ĘNĻ¢ļxūėŻ¼─Ū├┤╚▄ę║ųąĄ─ĻÄļxūė┐╔─▄╩ŪŻ© Ż®
A. SO42ŻŁ B. ClŻŁ C. OHŻŁ D. CO32ŻŁ
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐ļ┬Ż©N2H4Ż®╩Ū╗╝²░läėÖCĄ─ę╗ĘN╚╝┴ŽŻ¼Ę┤æ¬ĢrN2O4×ķč§╗»ä®Ż¼╔·│╔N2║═H2OŻ©gŻ®Ż¼ęčų¬Ż║ N2Ż©gŻ®+2O2Ż©gŻ®©TN2O4Ż©gŻ®Ż¼Ī„H=+8.7kJ/molŻ╗
N2H4Ż©gŻ®+O2Ż©gŻ®©TN2Ż©gŻ®+2H2OŻ©gŻ®Ż¼Ī„H=®ü534.0kJ/molŻ╗
Ž┬┴ą▒Ē╩Šļ┬Ė·N2O4Ę┤æ¬Ą─¤ß╗»īWĘ┤æ¬ĘĮ│╠╩ĮŻ¼š²┤_Ą─╩ŪŻ© Ż®
A.2N2H4Ż©gŻ®+N2O4Ż©gŻ®©T3N2Ż©gŻ®+4H2OŻ©gŻ®Ż╗Ī„H=®ü542.7 kJ/mol
B.2N2H4Ż©gŻ®+N2O4Ż©gŻ®©T3N2Ż©gŻ®+4H2OŻ©gŻ®Ż╗Ī„H=®ü1059.3 kJ/mol
C.N2H4Ż©gŻ®+ ![]() N2O4Ż©gŻ®©T
N2O4Ż©gŻ®©T ![]() N2Ż©gŻ®+2H2OŻ©gŻ®Ż╗Ī„H=®ü1076.7 kJ/mol
N2Ż©gŻ®+2H2OŻ©gŻ®Ż╗Ī„H=®ü1076.7 kJ/mol
D.2N2H4Ż©gŻ®+N2O4Ż©gŻ®©T3N2Ż©gŻ®+4H2OŻ©gŻ®Ż╗Ī„H=®ü1076.7 kJ/mol
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐─│┴“╦ßÅS«a╔·Ą─¤²į³(ų„ę¬║¼Fe2O3ĪóFeO,▀Ć║¼ėąę╗Č©┴┐Ą─SiO2)┐╔ė├ė┌ųŲéõFeCO3,Ųõ┴„│╠╚ńŽ┬:
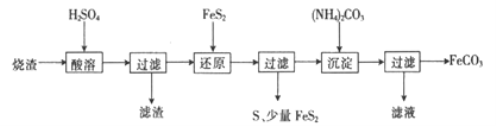
ęčų¬:▀ĆįŁĢr,FeS2┼cH2SO4▓╗Ę┤æ¬,Fe3+═©▀^Ę┤æ¬ó±Īóó“▒╗▀ĆįŁ,ŲõųąĘ┤æ¬ó±W×ķ
FeS2+14Fe3++8H2O=15Fe2++2SO42-+16H+ĪŻ
Ż©1Ż®Ę┤æ¬ó±ųą▀ĆįŁä®╩Ū_________
Ż©2Ż®×Vį³Ą─│╔Ęų╩Ū_______(╠Ņ├¹ĘQ)ĪŻ
Ż©3Ż®╦∙Ą├FeCO3ąĶ│õĘųŽ┤£ņ,Öz“×FeCO3╩ŪʱŽ┤ā¶Ą─ĘĮĘ©╩Ū____________
Ż©4Ż®ó┘┼õŲĮĘ┤æ¬Ą─ļxūėĘĮ│╠╩Į: ![]() ____________
____________
ó┌▀ĆįŁŪ░║¾╚▄ę║ųą▓┐ĘųļxūėĄ─ØŌČ╚ęŖŽ┬▒Ē(╚▄ę║¾wĘeūā╗»║÷┬į▓╗ėŗ):
ļxūė | ļxūėØŌČ╚(mol/L) | |
▀ĆįŁŪ░ | ▀ĆįŁ║¾ | |
Fe2+ | 0.10 | 2.50 |
SO42- | 3.50 | 3.70 |
ätĘ┤æ¬ó±Īóó“ųą╔·│╔Fe2+Ą─╬’┘|Ą─┴┐ų«▒╚×ķ______________
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐▀^č§╗»Ō}(CaO2)╩Ūę╗ĘN░ū╔½Š¦¾wŻ¼¤o│¶¤o╬ČŻ¼─▄│▒ĮŌŻ¼ļy╚▄ė┌╦«Ż¼┐╔┼c╦«ŠÅ┬²Ę┤æ¬Ż╗▓╗╚▄ė┌┤╝ŅÉĪóęę├čĄ╚Ż¼ęū┼c╦ßĘ┤æ¬Ż¼│Żė├ū„ÜóŠ·ä®ĪóĘ└Ė»ä®Ą╚ĪŻ═©│Ż└¹ė├CaCl2į┌ēAąįŚl╝■Ž┬┼cH2O2Ę┤æ¬ųŲĄ├ĪŻ
─│╗»īW┼d╚żąĪĮMį┌īŹ“×╩ęųŲéõCaO2Ą─īŹ“×ĘĮ░Ė║═čbų├╩ŠęŌłDŻ©łDę╗Ż®╚ńŽ┬Ż║


šł╗ž┤Ž┬┴ąå¢Ņ}Ż║
Ż©1Ż®╚²Ņi¤²Ų┐ųą░l╔·Ą─ų„ę¬Ę┤æ¬Ą─╗»īWĘĮ│╠╩Į×ķ___________________________________Ż╗
Ż©2Ż®ų¦╣▄BĄ─ū„ė├╩Ū_________________________Ż╗
Ż©3Ż®▓Į¾Eó█ųąŽ┤£ņCaO2Īż8H2OĄ─ę║¾wXĄ─ūŅ╝č▀xō±╩Ū____________Ż╗
AŻ«¤o╦«ęę┤╝ BŻ«ØŌ¹}╦ß CŻ«╦« DŻ«CaCl2╚▄ę║
Ż©4Ż®▀^č§╗»Ō}┐╔ė├ė┌ķL═Š▀\▌ö¶~├ńŻ¼▀@¾w¼F┴╦▀^č§╗»Ō}___________Ą─ąį┘|Ż╗
AŻ«┐╔ŠÅ┬²╣®č§ BŻ«─▄╬³╩š¶~├ń║¶│÷Ą─CO2ÜŌ¾w CŻ«─▄│▒ĮŌ DŻ«┐╔ęųŠ·
Ż©5Ż®ęčų¬CaO2į┌350ĪµĢr─▄čĖ╦┘ĘųĮŌŻ¼╔·│╔CaO║═O2ĪŻįōąĪĮM▓╔ė├╚ńłDČ■╦∙╩ŠĄ─čbų├£yČ©äé▓┼ųŲéõĄ─«aŲĘųąCaO2Ą─╝āČ╚(įOļs┘|▓╗ĘųĮŌ«a╔·ÜŌ¾w)
ó┘Öz▓ķįōčbų├ÜŌ├▄ąįĄ─ĘĮĘ©╩ŪŻ║_________________________________Ż╗
ó┌╩╣ė├________(╠ŅāxŲ„├¹ĘQ)£╩┤_ĘQ╚Ī0.5000gśėŲĘŻ¼ų├ė┌įć╣▄ųą╝ė¤ß╩╣Ųõ═Ļ╚½ĘųĮŌŻ¼╩š╝»ĄĮ33.60mL(ęčōQ╦Ń×ķś╦£╩ĀŅør)ÜŌ¾wŻ¼ät«aŲĘųą▀^č§╗»Ō}Ą─┘|┴┐ĘųöĄ×ķ________(▒Ż┴¶4╬╗ėąą¦öĄūų)Ż╗
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐Ž┬┴ąėąĻPöó╩÷ųąš²┤_Ą─╩Ū
A. Ž“NaHSO4╚▄ę║ųą╝ė╚ļĄ╚ØŌČ╚Ą╚¾wĘeĄ─Ba(OH)2╚▄ę║:pH=13
B. NaCl╚▄ę║║═CH3COONH4╚▄ę║Š∙’@ųąąįŻ¼ā╔╚▄ę║ųą╦«Ą─ļŖļx│╠Č╚▓╗═¼
C. Ž“┤ū╦ß╚▄ę║ųą╝ė╔┘┴┐╦«ŽĪßīŻ¼ 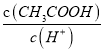 į÷┤¾
į÷┤¾
D. Ž“0.10mol/LNa2CO3╚▄ę║ųą═©╚ļ╔┘┴┐CO2║¾:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐ę╗Č©£žČ╚Ž┬Ż¼į┌╚▌Ęe×ķVLĄ─├▄ķ]╚▌Ų„ųą▀MąąĘ┤æ¬Ż║aNŻ©gŻ®bMŻ©gŻ®Ż¼MĪóNĄ─╬’┘|Ą─┴┐ļSĢrķgĄ─ūā╗»Ū·ŠĆ╚ńłD╩ŠŻ« 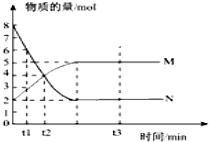
Ż©1Ż®┤╦Ę┤æ¬Ą─╗»īWĘĮ│╠╩ĮųąaŻ║b=
Ż©2Ż®t1ĄĮt2Ģr┐╠Ż¼ęįMĄ─ØŌČ╚ūā╗»▒Ē╩ŠĄ─ŲĮŠ∙╗»īWĘ┤æ¬╦┘┬╩×ķ
Ż©3Ż®┤╦Ę┤æ¬į┌įōŚl╝■Ž┬▀_ĄĮŽ▐Č╚ĢrŻ¼Ę┤æ¬╬’Ą─▐D╗»┬╩×ķ
Ż©4Ż®Ž┬┴ąöó╩÷ųą─▄šf├„╔Ž╩÷Ę┤æ¬▀_ĄĮŲĮ║ŌĀŅæBĄ─╩Ū AŻ«Ę┤æ¬ųąM┼cNĄ─╬’┘|Ą─┴┐ų«▒╚×ķ1Ż║1
BŻ«╗ņ║ŽÜŌ¾wĄ─┐é┘|┴┐▓╗ļSĢrķgĄ─ūā╗»Č°ūā╗»
CŻ«╗ņ║ŽÜŌ¾wĄ─┐é╬’┘|Ą─┴┐▓╗ļSĢrķgĄ─ūā╗»Č°ūā╗»
DŻ«å╬╬╗Ģrķgā╚Ž¹║─amol NŻ¼═¼Ģr╔·│╔bmol M
EŻ«╗ņ║ŽÜŌ¾wĄ─ē║ÅŖ▓╗ļSĢrķgĄ─ūā╗»Č°ūā╗»
FŻ«NĄ─▐D╗»┬╩▀_ĄĮūŅ┤¾Ż¼Ūę▒Ż│ų▓╗ūāŻ«
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
ć°ļHīWąŻā×▀x - ŠÜ┴Ģāį┴ą▒Ē - įćŅ}┴ą▒Ē
║■▒▒╩Ī╗ź┬ōŠW▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ŲĮ┼_ | ŠW╔Žėą║”ą┼Žó┼eł¾īŻģ^ | ļŖą┼įp“_┼eł¾īŻģ^ | ╔µÜv╩Ę╠ō¤oų„┴xėą║”ą┼Žó┼eł¾īŻģ^ | ╔µŲ¾ŪųÖÓ┼eł¾īŻģ^
▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ļŖįÆŻ║027-86699610 ┼eł¾Ó]ŽõŻ║58377363@163.com