
【題目】某化學興趣小組利用圖甲裝置制取氨氣并探究氨氣的有關性質。
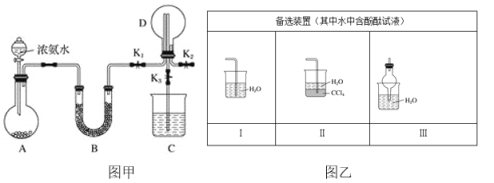
(1)裝置A中燒瓶內試劑可選用__(填序號)。
a.堿石灰 b.濃硫酸 c.五氧化二磷 d.氯化鈣
(2)若探究氨氣的溶解性,當裝置D中集滿氨氣后,關閉K1、K2,打開K3,引發噴泉的實驗操作是__。不能在K2的導管末端連接圖乙中的__裝置(填序號)。
(3)若探究氨氣的還原性,需關閉K1、K3,K2連接純凈、干燥氯氣的裝置。
①用二氧化錳與濃鹽酸制取氯氣,生成的氣體必須依次通過盛有__試劑和__試劑的洗氣瓶。
②D中氨氣與氯氣反應產生白煙,同時生成一種無色無味的氣體,該反應的化學方程式為__。
③尾氣可用C裝置處理,若尾氣中含有少量Cl2,則C裝置中應盛放__溶液(填化學式),反應的離子方程式為__。
【答案】a 用熱毛巾捂住圓底燒瓶底部,當C 中導管中的水超過C中水面時,撤走毛巾即可引發噴泉 Ⅰ 飽和食鹽水 濃硫酸 3Cl2+8NH3![]() 6NH4Cl+N2 NaOH Cl2+2OH﹣
6NH4Cl+N2 NaOH Cl2+2OH﹣![]() Cl﹣+ClO﹣+H2O
Cl﹣+ClO﹣+H2O
【解析】
(1)氨水易揮發,升高溫度能促進氨水分解生成氨氣,為促進氨水分解,則燒瓶中加入的物質遇氨水后能放出大量熱,且和氨水不反應;
(2)氨氣極易溶于水,關閉K1、K2,打開K3,利用壓強差將燒杯中的水排到燒瓶中,在K2的導管末端連接圖乙中的能防止倒吸的裝置;
(3)①濃鹽酸制取的氯氣中含有氯化氫氣體和水蒸氣,為防止干擾實驗,氯氣在進入燒瓶前,應該用飽和食鹽水和濃硫酸除去氯化氫和水蒸氣;
②根據氧化還原反應知, 氨氣與氯氣反應產生白煙是氯化銨,生成的無色無味的氣體是氮氣,根據反應物和生成物寫出反應方程式;
③氯氣的水溶液呈酸性,所以可以用堿除去氯氣。
(1)氨水易揮發,升高溫度能促進氨水分解生成氨氣,為促進氨水分解,則燒瓶中加入的物質遇氨水后能放出大量熱,且和氨水不反應,
a.堿石灰遇水放出大量熱,能使氨水溫度升高,且和氨水不反應,故a選;;
b.濃硫酸和氨水反應,故b不選;
c.五氧化二磷能和氨水反應,故c不選;
d.氯化鈣和氨水溶液中氨氣反應生成絡合物,溶解不放熱,故d不選,;
本題答案是:a。
(2)利用壓強差將燒杯中的水排到燒瓶中,操作為用熱毛巾將燒瓶捂熱,燒瓶中的氣體進入燒杯中,導致大氣壓強大于燒瓶中氣體壓強,從而使燒杯中的水通過導管進入燒瓶中產生噴泉實驗,氨氣極易溶于水,為防止倒吸,吸收氨氣的裝置中應該有緩沖裝置,Ⅱ、Ⅲ裝置中都有緩沖裝置,Ⅰ沒有緩沖裝置能產生倒吸,不能在K2的導管末端連接圖乙中的 I;
本題答案是:用熱毛巾捂住圓底燒瓶底部,當C 中導管中的水超過C中水面時,撤走毛巾即可引發噴泉,Ⅰ。
(3)①濃鹽酸制取的氯氣中含有氯化氫氣體和水蒸氣,為防止干擾實驗,氯氣在進入燒瓶前,應該用飽和食鹽水和濃硫酸除去氯化氫和水蒸氣;
本題答案為:飽和食鹽水,濃硫酸;。
②根據氧化還原反應知,生成的無色無味的氣體是氮氣,所以其反應方程式為:3Cl2![]() 8NH3=6NH4Cl
8NH3=6NH4Cl![]() N2,
N2,
本題答案為:3Cl2![]() 8NH3=6NH4Cl
8NH3=6NH4Cl![]() N2;
N2;
③氯氣和水反應生成鹽酸和次氯酸導致氯氣的水溶液呈酸性,所以可以用氫氧化鈉溶液除去氯氣,反應離子方程式為:Cl2![]() 2OH-=Cl-
2OH-=Cl-![]() ClO-
ClO-![]() H2O;
H2O;
本題答案為:NaOH,Cl2![]() 2OH-=Cl-
2OH-=Cl-![]() ClO-
ClO-![]() H2O。
H2O。


 寒假大串聯黃山書社系列答案
寒假大串聯黃山書社系列答案科目:高中化學 來源: 題型:
【題目】汽車尾氣是城市主要污染之一,治理的一種辦法是在汽車排氣管上裝催化轉化器,它使一氧化氮與一氧化碳反應生成可參與大氣生態循環的無毒氣體,并促使烴類充分燃燒及二氧化硫的轉化,下列說法錯誤的是
A. 一氧化氮與一氧化碳反應的化學方程式為2CO+2NO![]() 2CO2+N2
2CO2+N2
B. 此方法的缺點是由于二氧化碳的增多,會大大提高空氣的酸度
C. 為減少城市污染應開發新能源
D. 汽車尾氣中有兩種氣體與血紅蛋白結合而使人中毒
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學小組為了證明二氧化硫和氯氣的漂白性,設計了如下圖所示的實驗裝置:
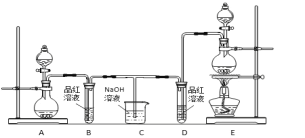
他們制備二氧化硫和氯氣所依據的原理分別是:
Na2SO3+H2SO4 = Na2SO4+H2O+SO2↑
MnO2+4HCl(濃) ![]() MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
(1)用來制取氯氣的裝置是______(填字母),反應中濃鹽酸所表現出________________性質。
(2)反應開始一段時間后,B、D試管中的品紅溶液均退色。停止通氣后,再給B、D兩個試管分別加熱____ (填" B”或“D")試管中無明顯現象。
(3)裝置C的作用是________________________;
(4)若裝置D中的品紅溶液換成紫色的石蕊溶液,則出現的現象是____________________________;
(5)該小組同學將兩種氣體混合后通入品紅溶液,一段時間后,品紅溶液幾乎不退色。查閱資料得知:兩種氣體按體積比1:1混合,再與水反應可生成兩種常見的酸,因而失去漂白作用,該反應的化學方程式是:________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學用右圖所示的裝置及藥品進行酸性強弱比較的實驗,下列說法不正確的是
A.①和②中發生的反應均為復分解反應
B.向Na2SiO3飽和溶液中滴酚酞溶液無明顯現象
C.一段時間后②中有膠凍狀物質生成
D.該實驗能證明酸性強弱的順序是:硫酸>碳酸>硅酸
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】“84”消毒液(有效成分為![]() )可用于消毒和漂白,下列實驗現象的分析不正確的是
)可用于消毒和漂白,下列實驗現象的分析不正確的是
實驗操作 | ①
| ② | ③
|
實驗現象 | 混合后溶液的 | 混合后溶液 | 混合后溶液 |
A. 對比實驗①和②,②中藍色迅速褪去的原因是發生了反應![]()
B. 實驗③中產生的氣體是![]() ,由
,由![]() 分解得到:
分解得到:![]()
C. 對比實驗②和③,溶液的![]() 可能會影響
可能會影響![]() 的氧化性或
的氧化性或![]() 的還原性
的還原性
D. 加酸可以提高“84”消毒液的漂白效果,但需要調控到合適的![]() 才能安全使用
才能安全使用
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某課外活動小組欲利用CuO與NH3反應,研究NH3的某種性質并測定其組成,設計了如下實驗裝置(夾持裝置未畫出)進行實驗。請回答下列問題:
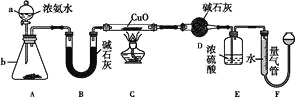
(1)儀器a的名稱為____,儀器b中可選擇的試劑為____。
(2)實驗室中,利用裝置A,還可制取的無色氣體是____(填字母)。
A.Cl2 | B.O2 | C.CO2 | D.NO2 |
(3)實驗中觀察到裝置C中黑色CuO粉末變為紅色固體,量氣管有無色無味的氣體產生,上述現象證明NH3具有____性,寫出相應的化學方程式:_______________________。
(4)E裝置中濃硫酸的作用是_____________________________________。
(5)讀取氣體體積前,應對裝置F進行的操作:____________________________。
(6)實驗完畢,若測得干燥管D增重m g,裝置F測得氣體的體積為n L(已折算成標準狀況),則氨分子中氮、氫的原子個數比為____(用含m、n字母的代數式表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某反應過程如圖所示,關于該反應的下列說法中不正確的是( )
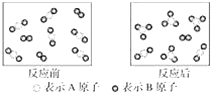
A. 該反應為可逆反應
B. 該反應可表示為2AB2+B2![]() 2AB3
2AB3
C. 若反應開始加入1 mol B2,則會生成2 mol AB3
D. 該過程中,已反應的AB2占AB2總數的![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖是一種正投入生產的大型蓄電系統,放電前,被膜隔開的電解質為Na2S2和NaBr3,放電后分別變為Na2S4和NaBr。下列敘述正確的是( )
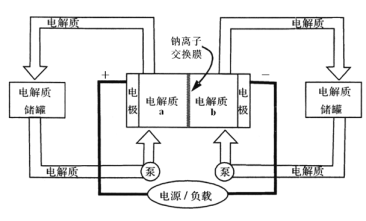
A. 放電時,負極反應為3NaBr-2e-=NaBr3+2Na+
B. 充電時,陽極反應為2Na2S2-2e-=Na2S4+2Na+
C. 放電時,Na+經過離子交換膜,由b池移向a池
D. 用該電池電解飽和食鹽水,產生2.24 L H2時,b池生成17.40gNa2S4
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一條魚、蝦絕跡的小河邊有四座工廠甲、乙、丙、丁(如圖),它們排出的廢液里,每個工廠只有 Na2CO3、CuCl2、Ca(OH)2、HCl 中的一種。某中學環保小組對河水監測時發現:① 甲處河水澄清且呈藍色;② 乙處河水由乳白色渾濁變淺藍色渾濁;③ 丙處河水由渾變清;④ 丁處產生氣泡,河水仍清,請推斷:
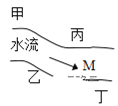
(1)四座工廠排除的廢液里含有的污染物:甲_______,乙________,丙_______,丁________。
(2)在M處取出的河水中,肯定含有的離子是____________________。
(3)寫出丙廠處可能發生的離子方程式______________________________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com