
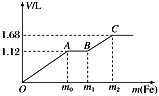
【題目】向100 mL稀H2SO4與稀HNO3的混合溶液中逐漸加入鐵粉,假設加入鐵粉的質量與產生氣體的體積(標準狀況)之間的關系如圖所示,且每一段只對應一個反應。下列說法正確的是( )
A. 開始時產生的氣體為H2
B. AB段發生的反應為置換反應
C. 所用混合溶液中c(HNO3)=0.5 mol·L-1
D. 參加反應鐵粉的總質量m2=8.4 g
【答案】C
【解析】已知氧化性:NO3->Fe3+>H+,OA段發生Fe+ NO3-+4 H+= Fe3++NO↑+2H2O,AB段發生Fe+ 2Fe3+=3 Fe2+,B以后發生Fe+2 H+= Fe2++H2↑;開始時產生的氣體為NO,A錯誤;AB段發生化合反應,B錯誤;根據Fe+ NO3-+4 H+= Fe3++NO↑+2H2O反應看出:HNO3—NO關系,生成NO的量=1.12/22.4=0.05 mol,所以所用混合溶液中c(HNO3)=0.5 mol·L-1,C正確;根據電子守恒:最終產物中含有Fe2+,所以:3×n(NO)+2×n(H2)=2 n(Fe),帶入數值進行計算:3×0.05+2×(1.68-1.12)/22.4=2 n(Fe),n(Fe)=0.1 mol,參加反應鐵粉的總質量m2=5.6 g,D,錯誤;正確選項C。


 期末金牌卷系列答案
期末金牌卷系列答案 輕松課堂標準練系列答案
輕松課堂標準練系列答案科目:高中化學 來源: 題型:
【題目】下列各組物質不能按![]() “
“![]() ” 表示反應一步完成關系轉化的是
” 表示反應一步完成關系轉化的是 ![]()
選項 | a | b | c |
A | SiO2 | Na2SiO3 | H2SiO3 |
B | AlCl3 | Al(OH)3 | NaAlO2 |
C | Fe | Fe(OH)3 | Fe2O3 |
D | MgCl2 | Mg(OH)2 | MgO |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將4 mol A氣體和2 mol B氣體在2 L的容器中混合并在一定條件下發生如下反應2A(g)+B(g) ![]() 2C(g),若2 s(秒)后測得C的濃度為0.6 mol/L,現有下列幾種說法:
2C(g),若2 s(秒)后測得C的濃度為0.6 mol/L,現有下列幾種說法:
①用物質A表示反應的平均速率為0.3 mol/(L·s)
②用物質B表示反應的平均速率為0.6 mol/(L·s)
③2 s時物質A的轉化率為70%
④2 s時物質B的濃度為0.7 mol/L
其中正確的是( )
A.①③
B.①④
C.②③
D.③④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化合物6.4g在氧氣中完全燃燒,只生成8.8g CO2和7.2g H2O.下列說法正確( )
A.該化合物僅含碳、氫兩種元素
B.該化合物中碳、氫原子個數比為1:4
C.無法確定該化合物是否含有氧元素
D.該化合物中一定含有氧元素
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某烴的結構簡式為 ![]() ,它可能具有的性質是( )
,它可能具有的性質是( )
A.易溶于水也易溶于有機溶劑
B.能發生加聚反應,其生成物可用  表示
表示
C.能使溴水褪色,但不能使酸性KMnO4溶液褪色
D.既能使溴水褪色,又能使酸性KMnO4溶液褪色
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ.某鈉鹽溶液中通入足量氨氣,無明顯現象.再在所得溶液中通入過量CO2 , 產生大量白色沉淀。
(1)寫出氨氣的電子式。
(2)該鈉鹽溶液中一定不可能含有下列哪種微粒(填編號)。
A.Cl﹣
B.Fe2+
C.SiO32﹣
D.AlO2﹣
(3)寫出一個通入過量CO2時生成白色沉淀的離子方程式。
(4)Ⅱ.電鍍工業中往往產生大量的有毒廢水,必須嚴格處理后才可以排放.某種高濃度有毒的含A離子(陰離子)廢水在排放前的處理過程如下: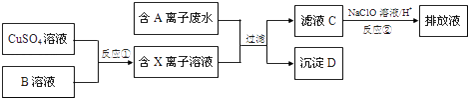
已知:9.0g沉淀D在氧氣中灼燒后,產生8.0g黑色固體,反應后的氣體通過足量澄清石灰水時,產生10.0g白色沉淀,最后得到的混合氣體除去氧氣后,還剩余標況下密度為1.25g/L的氣體1.12L。
沉淀D的化學式是。
(5)寫出沉淀D在氧氣中灼燒發生的化學方程式。
(6)濾液C中還含有微量的A離子,通過反應②,可將其轉化為對環境無害的物質,試用離子方程式表示該原理。
(7)反應①為制得某種元素的低價X離子,從氧化還原反應的角度分析,(填“能”或“不能”用Na2SO3溶液來代替B溶液,原因是。
(8)設計實驗證明所用Na2SO3溶液是否變質。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在足量的NaI溶液中,加入少量氯水及四氯化碳,振蕩后靜置,出現的現象( )
A.溶液不分層,溶液呈紫紅色B.溶液分兩層,上層液體呈紫紅色
C.溶液分兩層,下層液體呈紫紅色D.溶液分兩層,下層是無色液體
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com