
【題目】如圖表示某些物質之間的轉化關系,每個字母代表一種物質,部分產物已略去。A是一種碳酸氫鹽,也是一種常用的化學肥料,B是能使濕潤的紅色石蕊試紙變藍色的無色氣體,D是無色無味氣體。
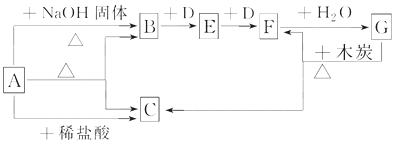
回答下列問題:
(1)物質A的名稱是________________。
(2)寫出物質B的一種主要用途______________。
(3)寫出實驗室制取氣體B的化學方程式__________________________。
寫出工業上制取氣體B的化學方程式__________________________。
(4)寫出反應的化學方程式:
B→E______________________________。
F→G____________________________________。
【答案】 碳酸氫銨 制氮肥(或制硝酸或作制冷劑) 2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O N2+3H2
CaCl2+2NH3↑+2H2O N2+3H2![]() 2NH3 4NH3+5O2
2NH3 4NH3+5O2![]() 4NO+6H2O 3NO2+H2O === 2HNO3+NO
4NO+6H2O 3NO2+H2O === 2HNO3+NO
【解析】A是一種酸式鹽,也是一種常用的化學肥料,B是能使濕潤的紅色石蕊試紙變藍色的無色氣體是NH3,是A和氫氧化鈉反應生成,說明A中含銨根離子,B和D發生兩部連續反應,說明D是無色無味的氣體O2,E為NO,F為NO2,G為HNO3,G和C反應生成二氧化氮和二氧化碳,所以C為CO2,A是一種酸式鹽,確定A為碳酸氫銨;
(1)根據上面的分析可知,A為碳酸氫銨;
(2)物質B是NH3,工業用途可以工業制硝酸(或制氮肥,制氨水等);
(3)B是NH3,實驗室制取氣體B的化學方程式為2NH4Cl+Ca(0H)2![]() CaCl2+2NH3↑+2H2O,工業上制取氣體B是用氫氣和氮氣高溫高壓催化劑條件下合成氨,反應的化學方程式為:N2+3H2
CaCl2+2NH3↑+2H2O,工業上制取氣體B是用氫氣和氮氣高溫高壓催化劑條件下合成氨,反應的化學方程式為:N2+3H2![]() 2NH3;
2NH3;
(4)B-→E反應的化學方程式為4NH3+5O2![]() 4NO+6H2O,F→G反應的化學方程式為3NO2+H2O=2HNO3+NO。
4NO+6H2O,F→G反應的化學方程式為3NO2+H2O=2HNO3+NO。


科目:高中化學 來源: 題型:
【題目】砷化鎵(GaAs)是優良的半導體材料,可用于制作微型激光器或太陽能電池的材料等。回答下列問題:
(1)寫出基態As原子的核外電子排布式________________________。
(2)根據元素周期律,原子半徑Ga_____________As,第一電離能Ga____________As。(填“大于”或“小于”)
(3)AsCl3分子的立體構型為____________________,其中As的雜化軌道類型為_________。
(4)GaF3的熔點高于1000℃,GaCl3的熔點為77.9℃,其原因是_____________________。
(5)GaAs的熔點為1238℃,密度為ρg·cm-3,其晶胞結構如圖所示。該晶體的類型為________________,Ga與As以________鍵鍵合。Ga和As的摩爾質量分別為MGa g·mol-1和MAs g·mol-1,原子半徑分別為rGa pm和rAs pm,阿伏伽德羅常數值為NA,則GaAs晶胞中原子的體積占晶胞體積的百分率為____________________。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】120 mL含有0.20 mol碳酸鈉的溶液和200 mL鹽酸,不管將前者滴加入后者,還是將后者滴加入前者,都有氣體產生,但最終生成的氣體體積不同,則鹽酸的濃度合理的是( )
A. 2.0 mol·L-1 B. 1.5 mol·L-1 C. 0.18 mol·L-1 D. 0.24 mol·L
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設阿伏加羅常數為NA,下列說法正確的是
A. 常溫常壓下,11.2L甲烷中舍有的氫原子數為2NA
B. 標準狀況下,19.2g二氧化硫中含有的氧原子數為0.3NA
C. 1molNa被完全氧化生成Na202,轉移電子的數目為NA
D. 常溫下,1L0.1mol/L MgCl2溶液中含Cl-數為0.1NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】判斷下列說法不正確的是 ( )
A. NO2溶于水時發生氧化還原反應
B. CO、NO、NO2都是大氣污染氣體,在空氣中都能穩定存在
C. NO可用于某些疾病的治療
D. NO2與水的反應:3NO2+H2O===2NO![]() +NO↑+2H+
+NO↑+2H+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下,A與B反應可生成C和D,其能量變化如圖:

(1)下列有關反應A+B===C+D的說法正確的是________。
A.反應前后原子的種類和數目一定不變
B.該反應若有熱量變化,則一定是氧化還原反應
C.若該反應為放熱反應,則不需要加熱反應就一定能自發進行
D.反應物的總質量、總能量與反應產物的總質量、總能量均相等
(2)若H1<H2,則反應產物的總能量________(填“>”“<”或“=”)反應物的總能量,反應熱Q________0(填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】【宣城市2017屆第二次調研測試】抗癇靈(G)具有抗癲癇、抗驚厥、抗抑郁等功效,其合成路線如下圖所示(某些反應條件和副產物已略):
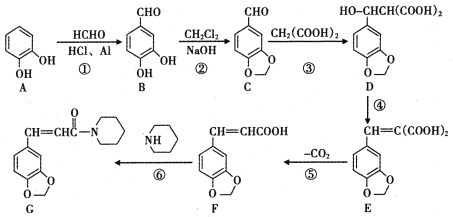
(1)A中含氧官能團名稱是____;簡述證明A含有該官能團的實驗方法:_________。
(2)若以醛基為母體,則B的系統命名法的名稱為_______;①~⑥的反應中屬于加成反應的是____ (填序號)。
(3)芳香化合物H是C的同分異構體,H的相關信息如下:
a.可發生銀鏡反應; b.可與NaHCO3溶液反應生成氣體;c.苯環上的一溴代物有2種,則H的結構簡式為__________。
(4)寫出反應⑥的化學反應方程式:_____________。
(5)( )的單體是薰衣草的調和香料,以苯甲醛(
)的單體是薰衣草的調和香料,以苯甲醛(![]() )為起始原料(其余有機、無機原料任選),參照G的合成,設計并補充完成下列合成路線圖:__________(空格內有幾步,寫幾步。)
)為起始原料(其余有機、無機原料任選),參照G的合成,設計并補充完成下列合成路線圖:__________(空格內有幾步,寫幾步。)

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某興趣小組探究SO2氣體還原Fe3+、I2,他們使用的藥品和裝置如下圖所示:

(1)下列實驗方案適用于在實驗室制取所需SO2的是_______。
A. Na2SO3溶液與HNO3 B. Na2SO3固體與濃硫酸
C. 硫化氫在空氣中燃燒 D. 高溫煅燒硫鐵礦
(2)裝置C的作用是______________________________。
(3)若要從A中所得溶液提取晶體,必須進行的實驗操作步驟:蒸發、冷卻結晶、________、自然干燥,在這一系列操作中沒有用到的儀器有________(填序號)。
A.蒸發皿 B.石棉網 C.漏斗 D.燒杯 E.玻璃棒 F.坩堝
(4)①寫出SO2與FeCl3溶液反應的離子方程式:______________________________;
②請設計實驗方案檢驗反應后A中Fe2+生成______________________________;
③本實驗中能表明SO2的還原性比I-的還原性強的現象是__________________,其反應的離子方程式為___________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Mg、Ca、Sr、Ba是按原子序數由小到大的順序排列的第ⅡA族元素。已知:①Mg(OH)2難溶于水,而Ca(OH)2微溶于水;②MgSO4溶于水,而CaSO4微溶于水。下列推測中,不正確的是( )。
A. Sr(OH)2溶解于水 B. SrSO4易溶于水
C. BaSO4不溶于水 D. Ba(OH)2比Ca(OH)2更易溶于水
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com