
向絕熱恒容密閉容器中通入SO2和NO2,一定條件下使反應SO2(g)+NO2(g)  SO3(g)+NO(g)達到平衡,正反應速率隨時間變化的示意圖如圖所示。由圖可得出的正確結論是( )
SO3(g)+NO(g)達到平衡,正反應速率隨時間變化的示意圖如圖所示。由圖可得出的正確結論是( )
| A.反應在c點達到平衡狀態 |
| B.反應物濃度:a點小于b點 |
| C.反應物的總能量低于生成物的總能量 |
| D.Δt1=Δt2時,SO2的轉化率:a~b段小于b~c段 |
科目:高中化學 來源: 題型:單選題
在相同條件下(T=500K),相同體積的甲乙兩容器,甲中充入1gSO2和1gO2,乙中充入2gSO2和2gO2,下列敘述中不正確的是( )
| A.反應速率:乙>甲 | B.平衡混合物中SO2的體積分數:乙>甲 |
| C.SO2的轉化率:乙>甲 | D.平衡時O2的濃度:乙>甲 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
向容積相同的甲、乙密閉容器中投入反應物,保持恒溫、恒容,測得反應達到平衡時的有關數據如下(已知N2(g) + 3H2(g)  2NH3(g) ΔH=-92.4 kJ·mol
2NH3(g) ΔH=-92.4 kJ·mol ):
):
| | 反應物投入量 | NH3的濃度 (mol·L  ) ) | 反應的 能量變化 | 體系壓強 (Pa) | 反應物 轉化率 |
| 甲 | 1mol N2、3mol H2 | c1 | 放出a kJ | p1 | α1 |
| 乙 | 2mol NH3 | c2 | 吸收b kJ | p2 | α2 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
對于化學反應方向的確定,下列說法正確的是( )
| A.在溫度、壓強一定的條件下,焓因素和熵因素共同決定一個化學反應的方向 |
| B.溫度、壓強一定時,吸熱的熵增反應一定能夠自發進行 |
| C.反應焓變是決定反應能否自發進行的唯一因素 |
| D.固體的溶解過程與熵變無關 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
將4 mol A和2 mol B放入2 L密閉容器中發生反應:2A (g)+B(g)??2C(g);ΔH<0,4 s后反應達到平衡狀態,此時測得C的濃度為0.6 mol/L。下列說法正確的是( )
A.4 s內,v(B)=0.075 mol/(L·s)
B.4 s后平衡狀態下,c(A)∶c(C)=2∶1
C.達到平衡狀態時,若只升高溫度,則C的物質的量濃度增大
D.達到平衡狀態后,若溫度不變,縮小容器的體積,則A的轉化率降低
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
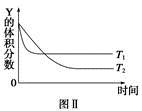
某溫度時,在密閉容器中,X、Y、Z三種氣體濃度的變化如圖Ⅰ所示,若其它條件不變,當溫度分別為T1和T2時,Y的體積分數與時間關系如圖Ⅱ所示。則下列結論正確的是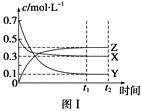
A.該反應的熱化學方程式為X(g)+3Y(g)  2Z(g) ΔH>0 2Z(g) ΔH>0 |
| B.若其它條件不變,升高溫度,正、逆反應速度均增大,X的轉化率減小 |
| C.達到平衡后,若其他條件不變,減小容器體積,平衡向逆反應方向移動 |
| D.達到平衡后,若其他條件不變,通入稀有氣體,平衡向正反應方向移動 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
NO2和N2O4可相互轉化:2NO2(g)  N2O4(g) ΔH<0現將一定量NO2和N2O4的混合氣體通入體積為1 L的恒溫密閉容器中,反應物濃度隨時間變化關系如圖。下列說法中正確的是
N2O4(g) ΔH<0現將一定量NO2和N2O4的混合氣體通入體積為1 L的恒溫密閉容器中,反應物濃度隨時間變化關系如圖。下列說法中正確的是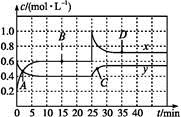
| A.圖中共有兩條曲線x和y,其中曲線y表示NO2濃度隨時間的變化 |
| B.A、B、C、D四個點中,表示化學反應處于平衡狀態的點是B和C |
| C.反應進行至25 min時,曲線發生變化的原因是加入0.4 mol N2O4 |
| D.若要達到與D相同的狀態,在25 min時還可采取的措施是適當縮小容器體積 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
化學平衡常數(K)、電離常數(Ka、Kb)、溶度積常數(Ksp)等常數是表示、判斷物質性質的重要常數,下列關于這些常數的說法中,正確的是
| A.化學平衡常數的大小與溫度、濃度、壓強有關,與催化劑無關 |
| B.Ka(HCN)<Ka(CH3COOH)說明相同物質的量濃度時,氫氰酸的酸性比醋酸強 |
| C.向氯化鋇溶液中加入同濃度的碳酸鈉和硫酸鈉溶液,先產生BaSO4沉淀,則Ksp(BaSO4)>Ksp(BaCO3) |
| D.當溫度升高時,弱酸、弱堿的電離常數(Ka、Kb)變大 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在容積不變的密閉容器中存在如下反應:2A(g)+B(g) 3C(g);ΔH<0,某研究小組研究了其他條件不變時,改變某一條件對上述反應的影響,下列分析正確的是( )
3C(g);ΔH<0,某研究小組研究了其他條件不變時,改變某一條件對上述反應的影響,下列分析正確的是( )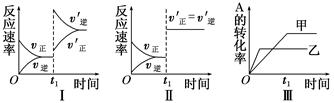
| A.圖Ⅰ表示的是t1時刻增大反應物的濃度對反應速率的影響 |
| B.圖Ⅱ表示的一定是t1時刻加入催化劑后對反應速率的影響 |
| C.圖Ⅲ表示的是溫度對化學平衡的影響,且乙的溫度較高 |
| D.圖Ⅲ表示的是催化劑對平衡的影響,且甲的催化效率比乙高 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com