
向容積相同的甲、乙密閉容器中投入反應物,保持恒溫、恒容,測得反應達到平衡時的有關數(shù)據(jù)如下(已知N2(g) + 3H2(g)  2NH3(g) ΔH=-92.4 kJ·mol
2NH3(g) ΔH=-92.4 kJ·mol ):
):
| | 反應物投入量 | NH3的濃度 (mol·L  ) ) | 反應的 能量變化 | 體系壓強 (Pa) | 反應物 轉化率 |
| 甲 | 1mol N2、3mol H2 | c1 | 放出a kJ | p1 | α1 |
| 乙 | 2mol NH3 | c2 | 吸收b kJ | p2 | α2 |
科目:高中化學 來源: 題型:單選題
在一個體積可變的密閉容器中,通入2molHI氣體,在一定條件下建立如下平衡:2HI(g) I2(g)+H2(g);△H>0,測得平衡時容器體積為1L,c(I2)=0.5mol/L。改變相關條件,下列結論正確的是
I2(g)+H2(g);△H>0,測得平衡時容器體積為1L,c(I2)=0.5mol/L。改變相關條件,下列結論正確的是
| A.保持容器體積不變,升高溫度,混合氣體的顏色逐漸變深 |
| B.恒溫,恒容,充入一定量氦氣(不參與反應),則正反應速率和逆反應速率均增大 |
| C.恒溫,緩慢壓縮容器,使容器體積恒定為0.2L,一定時間后,測得c(I2)=2.5mol/L |
| D.恒溫、恒壓,再通入2molHI氣體,到達平衡狀態(tài)后,HI轉化率會提高 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在20℃,5.05×105Pa條件下,密閉容器中進行反應2A(g)+xB(g) 4C(g),達平衡時c(A)=1.00mol?L-1,現(xiàn)將壓強減小到1.01×105Pa,建立平衡后,c(A)=0.18mol?L-1,則下列說法正確的是 ( )
4C(g),達平衡時c(A)=1.00mol?L-1,現(xiàn)將壓強減小到1.01×105Pa,建立平衡后,c(A)=0.18mol?L-1,則下列說法正確的是 ( )
A.系數(shù)x >2
B.若增大該體系的壓強,平衡向左移動,化學平衡常數(shù)變小
C.若增大該體系的壓強,平衡向右移動,化學平衡常數(shù)不變
D.該反應的化學平衡常數(shù)表達式是K=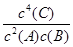
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在KI溶液中存在下列平衡:I2(aq)+I-(aq)=I(aq)。測得不同溫度下該反應的平衡常數(shù)K如表所示,下列說法正確的是
| t/℃ | 5 | 15 | 25 | 35 | 50 |
| K | 1 100 | 841 | 689 | 533 | 409 |
 I(aq)的ΔH>0
I(aq)的ΔH>0查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在一密閉容器中,反應 aA(g) bB(g)+cC(g) 達平衡后,保持溫度不變,將容器體積增加一倍,當達到新的平衡時,A的濃度變?yōu)樵瓉淼?0%,則( )
bB(g)+cC(g) 達平衡后,保持溫度不變,將容器體積增加一倍,當達到新的平衡時,A的濃度變?yōu)樵瓉淼?0%,則( )
| A.平衡向正反應方向移動了 | B.平衡向逆反應方向移動了 |
| C.物質B的質量分數(shù)減小了 | D.a>b+c |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在一個2L的容器中,放入2mol氣體A,5分鐘后,測得這種氣體A還剩余0.5mol,該反應中氣體A的化學反應速率是:
| A.1.5mol/(L·min) | B.0.15mol/(L·min) |
| C.0.75mol/(L·min) | D.0.075mol/(L·min) |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
2010年諾貝爾化學獎化學授予理查德·赫克等三位科學家,以表彰他們在“鈀催化交叉偶聯(lián)”方面的研究。下面關于催化劑的說法正確的是( )
| A.催化劑只改變反應的正反應速率 |
| B.催化劑通過升高反應的活化能來加快反應速率 |
| C.催化劑能夠改變反應的反應熱 |
| D.催化劑不能改變反應物的轉化率 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
向絕熱恒容密閉容器中通入SO2和NO2,一定條件下使反應SO2(g)+NO2(g)  SO3(g)+NO(g)達到平衡,正反應速率隨時間變化的示意圖如圖所示。由圖可得出的正確結論是( )
SO3(g)+NO(g)達到平衡,正反應速率隨時間變化的示意圖如圖所示。由圖可得出的正確結論是( )
| A.反應在c點達到平衡狀態(tài) |
| B.反應物濃度:a點小于b點 |
| C.反應物的總能量低于生成物的總能量 |
| D.Δt1=Δt2時,SO2的轉化率:a~b段小于b~c段 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在恒容密閉容器中通入A、B兩種氣體,在一定條件下發(fā)生反應:
2A(g)+B(g)  2C(g) ΔH>0。
2C(g) ΔH>0。
達到平衡后,改變一個條件(x),下列量(y)一定符合圖中曲線的是( )
| 選項 | x | y |
| A | 再通入A | B的轉化率 |
| B | 加入催化劑 | A的體積分數(shù) |
| C | 壓強 | 混合氣體的總物質的量 |
| D | 溫度 | 混合氣體的總物質的量 |
查看答案和解析>>
國際學校優(yōu)選 - 練習冊列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com