
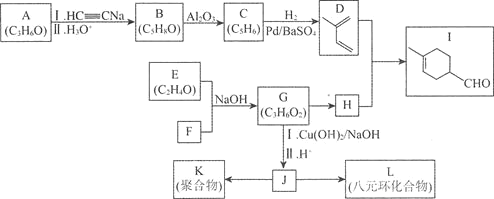
【題目】化合物J是有機合成中的一種重要中間體,其合成路線如下所示![]() 部分產物及條件略去
部分產物及條件略去![]() 。
。
已知:
①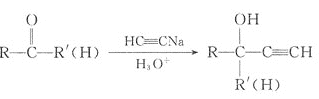 ;
;
②![]()
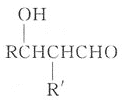
③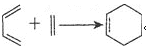
④A的一氯代物只有一種。
![]() Ⅰ分子中所含官能團的名稱為________。
Ⅰ分子中所含官能團的名稱為________。
![]() 中過程Ⅰ的反應類型為________,
中過程Ⅰ的反應類型為________,![]() 的反應類型為________。
的反應類型為________。
![]() 的化學名稱為________________。
的化學名稱為________________。
![]() 的結構簡式為________________,L的結構簡式為________________。
的結構簡式為________________,L的結構簡式為________________。
![]() 中過程Ⅰ的化學方程式為________________________。
中過程Ⅰ的化學方程式為________________________。
![]() 同時滿足下列條件的Ⅰ的同分異構體有________種
同時滿足下列條件的Ⅰ的同分異構體有________種![]() 不考慮立體異構,不包括Ⅰ
不考慮立體異構,不包括Ⅰ![]() 。
。
![]() 具有六元碳環結構
具有六元碳環結構
![]() 分子中含有一個甲基
分子中含有一個甲基
![]() 與Ⅰ具有相同的官能團
與Ⅰ具有相同的官能團
【答案】醛基、碳碳雙鍵 加成反應 消去反應 ![]() 甲基
甲基![]() ,
,![]() 丁二烯
丁二烯 ![]()
![]()
![]()
![]()
![]()
【解析】
由化合物A的一氯代物只有一種可知A是丙酮,則A為![]() ;由有機物的轉化關系可知,A與乙炔發生已知信息
;由有機物的轉化關系可知,A與乙炔發生已知信息![]() 的反應生成
的反應生成![]() ,則B為
,則B為![]() ;B在氧化鋁的作用下發生生成消去反應
;B在氧化鋁的作用下發生生成消去反應![]() ,則C為
,則C為![]() ;C與氫氣發生加成反應生成結構簡式為
;C與氫氣發生加成反應生成結構簡式為![]() 的D;D與
的D;D與![]() 發生信息
發生信息![]() 反應生成
反應生成![]() ,則H為
,則H為![]() ;
;![]() 在濃硫酸作用下,共熱發生消去反應生成
在濃硫酸作用下,共熱發生消去反應生成![]() ,則G為
,則G為![]() ,由E與F發生信息
,由E與F發生信息![]() 反應生成
反應生成![]() 可知E是乙醛、F是甲醛;G與新制的氫氧化銅發生氧化反應,酸化生成
可知E是乙醛、F是甲醛;G與新制的氫氧化銅發生氧化反應,酸化生成![]() ,則J為
,則J為![]() ;J一定條件下發生縮聚反應生成高聚酯
;J一定條件下發生縮聚反應生成高聚酯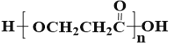 ,則K為
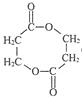
,則K為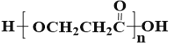 ;J在濃硫酸作用下發生酯化反應生成環酯
;J在濃硫酸作用下發生酯化反應生成環酯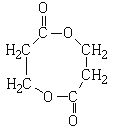 ,則L為
,則L為 。
。
(1)I的結構簡式為![]() ,官能團為醛基、碳碳雙鍵,故答案為:醛基、碳碳雙鍵;
,官能團為醛基、碳碳雙鍵,故答案為:醛基、碳碳雙鍵;
(2)![]() 的反應為
的反應為![]() 與乙炔發生已知信息
與乙炔發生已知信息![]() 的反應生成
的反應生成![]() ,
,![]() 的反應為
的反應為![]() 在濃硫酸作用下,共熱發生消去反應生成
在濃硫酸作用下,共熱發生消去反應生成![]() ,故答案為:加成反應;消去反應;
,故答案為:加成反應;消去反應;
(3)D的結構簡式為![]() ,名稱為
,名稱為![]() 甲基
甲基![]() ,
,![]() 丁二烯,故答案為:
丁二烯,故答案為:![]() 甲基
甲基![]() ,
,![]() 丁二烯;
丁二烯;
(4)C的結構簡式為![]() ,L的結構簡式為
,L的結構簡式為 ,故答案為:
,故答案為: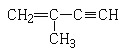 ;
; ;
;
(5)G→J的過程Ⅰ的反應為![]() 與新制的氫氧化銅共熱發生氧化反應,反應的化學方程式為HOCH2CH2CHO+2Cu(OH)2+NaOH
與新制的氫氧化銅共熱發生氧化反應,反應的化學方程式為HOCH2CH2CHO+2Cu(OH)2+NaOH![]() HOCH2CH2COONa+Cu2O↓+3H2O,故答案為:
HOCH2CH2COONa+Cu2O↓+3H2O,故答案為:
HOCH2CH2CHO+2Cu(OH)2+NaOH![]() HOCH2CH2COONa+Cu2O↓+3H2O;
HOCH2CH2COONa+Cu2O↓+3H2O;
(6)與I具有相同的官能團,說明分子中含有碳碳雙鍵和醛基,則具有六元碳環結構和分子中有一個甲基結構可能是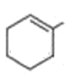 、
、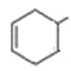 、
、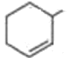 ,則
,則![]() 在環上的位置分別是5、6、6,由不考慮立體結構和不包括I可知符合條件的I的同分異構體共計16種,故答案為:16。
在環上的位置分別是5、6、6,由不考慮立體結構和不包括I可知符合條件的I的同分異構體共計16種,故答案為:16。


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
【題目】金屬鈦性能優越,被稱為繼鐵、鋁之后的“第三金屬”。鈦鐵礦(主要成分為FeTiO3,含少量Fe2O3、SiO2等雜質)可用來制備TiO2,同時得到副產品綠礬(FeSO4·7H2O),工藝流程如圖所示:
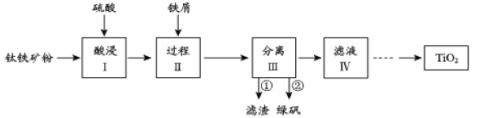
已知:①FeTiO3+2H2SO4=FeSO4+TiOSO4+2H2O
②TiO2+易水解,只能存在于強酸性溶液中
(1)酸浸I中Fe2O3與稀硫酸反應的離子方程式:_____________________。
(2)過程II中加入適量鐵屑的目的是_____________________________。
(3)分離III中步驟②得到綠礬的操作是__________________________。
(4)由濾液IV提取TiO2的過程如下:
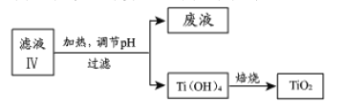
①請用化學平衡移動原理解釋濾液加熱煮沸的目的:_______________。
②由2Mg+TiCl4→Ti+2MgCl2反應后得到Mg、MgCl2、Ti的混合物,可采用真空蒸餾的方法分離得到Ti,依據如表信息,需加熱的溫度略高于______℃即可。
TiCl4 | Mg | MgCl2 | Ti | |
熔點/℃ | -26.0 | 648.8 | 714 | 1667 |
沸點/℃ | 136.4 | 1090 | 1412 | 3287 |
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數值。下列有關敘述正確的是
A.含16g氧原子的二氧化硅晶體中含有的鍵數目為1NA
B.1 mol N2與4 mol H2反應生成的NH3分子數為2NA
C.50℃時,1.0 L pH=1的H2SO4 溶液中含有的H+數目為0.1NA
D.12 g石墨烯(單層石墨)中含有六元環的數目為1.5NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】阿司匹林也叫乙酰水楊酸,是百年來三大經典藥物之一.用于治感冒、發熱、頭痛、牙痛、關節痛、風濕病,還能抑制血小板聚集,用于預防和治療缺血性心臟病、心絞痛、心肺梗塞、腦血栓形成,也可應用于血管形成術及旁路移植術.阿司匹林經典的合成方法如下流程:
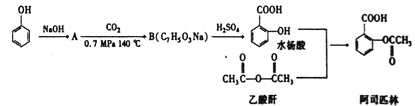
回答下列問題:
(1)阿司匹林的分子式為 ______ ,分子中所含官能團為 ______ 、 ______ ;水楊酸的系統命名為 ______。
(2)水楊酸和乙酸酐生成阿司匹林的反應類型屬于 ______ ,反應過程中控制溫度在![]() ,若溫度過高易發生期反應,可能生成的副產物中屬于脂的為 ______
,若溫度過高易發生期反應,可能生成的副產物中屬于脂的為 ______ ![]() 寫出兩種物質的結構簡式,毎個分子中只有兩個環
寫出兩種物質的結構簡式,毎個分子中只有兩個環![]() 。
。
(3)![]() 生成B的反應方程式為 ______ ,阿司匹林與足量的NaOH溶液反應的化學方程式為 ______ 。
生成B的反應方程式為 ______ ,阿司匹林與足量的NaOH溶液反應的化學方程式為 ______ 。
(4)水楊酸有多種同分異構體,符合下列條件的芳香族化合物有 ______ 種。
①能發生銀鏡反應②三氯化鐵溶液呈紫色。
(5)苯酚也有多種同分異構體,寫出其核磁共振氫譜只有一種的物質的結構簡式 ____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,下列有關敘述正確的是( )
A.Na2CO3溶液中:c(Na+)=2[c(CO32-)+c(HCO3-)]
B.pH相等的①NH4NO3 ②(NH4)2SO4 ③NH4HSO4溶液中,c(NH4+)大小順序①>②>③
C.NaY溶液的pH=8,c(Na+)-c(Y-)=9.9×10-7mol/L
D.向0.1mol/L的氨水中加入少量的硫酸銨固體,溶液中![]() 增大
增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某研究小組以乙烯和甲苯為主要原料,設計出醫藥中間體G的合成路線如下:

已知:![]()
RCOOH![]() RCOCl
RCOCl![]() RCOOR’
RCOOR’
(1)B的結構簡式為________。
(2)從乙烯到化合物E的轉化過程中,涉及的反應類型依次是________反應、________反應和________反應。
(3)F的分子式為________,M是F的某種能發生水解反應的同分異構體,經測定M的核磁共振氫譜為2組峰且峰面積之比為2:3,則M的結構簡式可能為________![]() 僅寫一列即可
僅寫一列即可![]() 。寫出M與足量NaOH溶液反應的作學方程式:________。
。寫出M與足量NaOH溶液反應的作學方程式:________。
(4)A的同分異構體有多種,同時符合下列條件的A的同分異構體有________種。
①含有一![]() 和
和![]() 且都與苯環直接相連。
且都與苯環直接相連。
②有4個碳原子在同一條直線上。
(5)設計出以甲苯為原料制備A的合成路線_____________。(無機試劑任選,已知:RCHO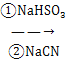
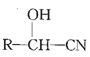 )合成路線常用的表示方式為:原料
)合成路線常用的表示方式為:原料 中間產物
中間產物 目標產物。
目標產物。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2016年5月千年繁華的古城揚州開通了寧啟動車,標志著古城揚州正式邁入“動車時代”,動車鐵路在建設施工中要大量使用各種材料.
①生產水泥和玻璃都用到的原料是______;制備玻璃的反應方程式______![]() 任寫一個
任寫一個![]() .
.
②動車車廂內飾板材多采用![]() 聚碳酸酯
聚碳酸酯![]() 及PC合金板材,PC屬于______
及PC合金板材,PC屬于______![]() 填字母
填字母![]() .
.
![]() 金屬材料
金屬材料![]() 無機非金屬材料
無機非金屬材料![]() 有機高分子材料
有機高分子材料
③動車大量使用鋁合金材料制作車廂.下列有關鋁合金敘述正確的是______![]() 填字母
填字母![]() .
.
![]() 屬于純凈物
屬于純凈物![]() 密度小,硬度大
密度小,硬度大![]() 在空氣中易被腐蝕
在空氣中易被腐蝕
④鐵路建設中如何防止鐵軌的腐蝕是工程技術人員攻克的難題之一.鐵在發生電化學腐蝕時的負極反應方程式為______.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用微生物燃料電池原理,可以處理宇航員排出的糞便,同時得到電能。美國宇航局設計的方案是:用微生物中的芽孢桿菌來處理糞便產生氨氣,氨氣與氧氣分別通入燃料電池兩極,最終生成常見的無毒物質。示意圖如下所示。下列說法錯誤的是( )
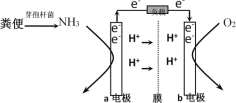
A.a電極是負極,b電極是正極
B.負極區發生的反應是2NH3 - 6e-=N2+6H+
C.正極區,每消耗標準狀況下2.24 L O2,a向b電極轉移0.4 mol電子
D.電池工作時電子通過由a經負載流向b電極,再穿過離子交換膜回到a電極
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,將NaOH溶液分別加到HA、HB兩種弱酸溶液中,兩溶液中pH與粒子濃度比值的對數關系如圖所示,已知![]() ,下列有關敘述錯誤的是( )
,下列有關敘述錯誤的是( )

A.HA、HB兩種酸中,HB的酸性弱于HA
B.b點時,![]()
C.同濃度同體積的NaA和NaB溶液中,陰離子總數相等
D.向HB溶液中加入NaOH溶液所得的混合溶液中,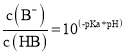
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com