
【題目】亞氯酸鈉(NaClO2)是一種重要漂白劑,實驗室可按下圖裝置制取NaClO2晶體。

已知:Ⅰ.A中發生的反應為:2ClO2+H2O2+2NaOH=2NaClO2+O2+2H2O
Ⅱ.NaClO2受熱易分解,溫度高于60℃時分解成NaClO3和NaCl。
(1)已知ClO2與Cl2類似具有漂白性,請設計檢驗ClO2漂白性的實驗方案______。
(2)A中用冰水浴的目的是______。
(3)裝置B的作用是______。
(4)測定樣品中NaClO2的質量分數的實驗過程如下:
步驟一:稱0.5000 g樣品,加入適量蒸餾水和過量的KI晶體和硫酸,發生如下反應:ClO![]() +4I﹣+4H+=2H2O+2I2+Cl﹣
+4I﹣+4H+=2H2O+2I2+Cl﹣
步驟二:將所得混合液稀釋成100 mL待測溶液。取25.00 mL待測溶液,加入淀粉溶液作指示劑,用0.2000 mol·L-1 Na2S2O3標準液滴定至終點,測得消耗標準溶液體積的平均值為15.00 mL(滴定過程中發生反應:I2+2S2O32-=2I﹣+S4O62-)。
①配制100 mL 0.2000 mol·L-1Na2S2O3標準溶液需要用到的玻璃儀器有燒杯、膠頭滴管、______。
②請計算所稱取樣品中NaClO2的質量分數_______________。(寫出計算過程)
【答案】將ClO2通入品紅溶液(或濕潤的有色布條) 防止NaClO2分解為NaClO3和NaCl 吸收尾氣 玻璃棒、100mL容量瓶 54.3%
【解析】
(1)已知ClO2與Cl2類似具有漂白性,檢驗Cl2可使用品紅溶液(或濕潤的有色布條),也可使用淀粉碘化鉀試紙,從而得出檢驗ClO2漂白性的實驗方案為:將ClO2通入品紅溶液(或濕潤的有色布條)。答案為:將ClO2通入品紅溶液(或濕潤的有色布條)。
(2) 因為NaClO2受熱易分解,溫度高于60℃時分解成NaClO3和NaCl ,所以應控制溫度以防副反應的發生。從而得出A中用冰水浴的目的是防止NaClO2分解為NaClO3和NaCl。答案為:防止NaClO2分解為NaClO3和NaCl。
(3) ClO2是污染環境的氣體,在A裝置中很難完全被吸收,所以應進行尾氣處理。從而得出裝置B的作用是吸收尾氣。答案為吸收尾氣。
(4) ① 配制100 mL 0.2000 mol·L-1Na2S2O3標準溶液需要用到的玻璃儀器有燒杯、膠頭滴管、玻璃棒、100mL容量瓶。答案為玻璃棒、100mL容量瓶。
(2)設樣品中所含NaClO2的物質的量為x
由ClO![]() +4I﹣+4H+=2H2O+2I2+Cl﹣,I2+2S2O32-=2I﹣+S4O62-中建立如下關系式:
+4I﹣+4H+=2H2O+2I2+Cl﹣,I2+2S2O32-=2I﹣+S4O62-中建立如下關系式:
ClO![]() ——2I2——4S2O32-
——2I2——4S2O32-
1mol 4mol
x ![]()
x=0.003mol
![]()
答案為54.3%


科目:高中化學 來源: 題型:
【題目】下列實驗裝置不能達到實驗目的的是
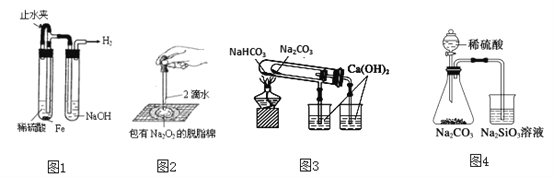
A. 圖1:制備并觀察氫氧化亞鐵
B. 圖2:證明過氧化鈉與水反應放熱
C. 圖3:驗證NaHCO3和Na2CO3的熱穩定性
D. 圖4:驗證酸性強弱H2SO4>H2CO3>H2SiO3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2.0molPCl3和1.0molCl2充入體積不變的密閉容器中,在一定條件下發生下述反應:PCl3(g)+Cl2(g)PCl5(g)達平衡時,PCl5為0.4mol,如果此時移走1.0molPCl3和0.50molCl2,在相同溫度下再達平衡時PCl5的物質的量是( )
A. 0.4mol
B. 0.2mol
C. 小于0.2mol
D. 大于0.2mol,小于0.4mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列裝置是實驗室制取氨氣的裝置圖,請回答下列問題:
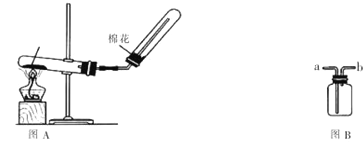
①寫出實驗室制取氨氣的化學方程式_______________________________;
②如果實驗室采用圖B來收集,則氨氣應從______端進。(填“a”或“b”)
③下列干燥劑能用來干燥氨氣的是________;
A.堿石灰 B.濃硫酸 C.氯化鈣固體
④圖A收集氨氣的裝置中棉花的作用是_______________________________;
⑤有圖A收集時,確定氨氣是否收滿的檢驗方法是________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上通常利用SiO2 和碳反應來制取硅,寫出反應的化學方程式___________________。
工業上還可以利用鎂制取硅,反應為2Mg+SiO2 = 2MgO+Si,同時會發生副反應:2Mg + Si = Mg2Si。如圖是進行Mg與SiO2反應的實驗裝置,試回答下列問題:

(1)由于O2和H2O(g)的存在對該實驗有較大影響,實驗中應通入氣體X作為保護氣,試管中的固體藥品可選用________(填序號)。
a.石灰石 b.鋅粒 c.純堿
(2)實驗開始時,必須先通一段時間X氣體,再加熱反應物,其理由是 ___________________________;當反應引發后,移走酒精燈,反應能繼續進行,其原因是______________________。
(3)反應結束后,待冷卻至常溫時,往反應后的混合物中加入稀鹽酸,可觀察到閃亮的火星,產生此現象的原因是副產物Mg2Si遇鹽酸迅速反應生成SiH4(硅烷)氣體,然后SiH4自燃.用化學方程式表示這兩個反應①________________________②___________________.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA表示阿伏加德羅常數的值,下列敘述中正確的是
A.常溫常壓下,等物質的量的N2和CO所含分子數均為NA
B.將含0.l mol FeCl3的飽和溶液制成膠體后,生成的Fe(OH)3膠粒數目為0.1NA
C.常溫常壓下,lmolNa 加熱后生成的Na2O、Na2O2混合物中陰離子數目一定為0.5NA
D.1molFe與足量水蒸氣在高溫下充分反應后失電子數為NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】苯和溴的取代反應的實驗裝置如圖所示。其中A為帶支管的試管改成的反應容器,在其下端開了一小孔,塞好石棉絨,再加入鐵屑粉少量。

(1)向反應容器A中逐滴加入溴和苯的混合液,幾秒鐘內就發生反應。寫出A中所發生反應的化學方程式:____________、____________;試管C中苯的作用____________。
(2)反應開始后,D、E試管的現象分別為__________________、____________; E中所發生反應的離子方程式為____________。
(3)在上述整套裝置中,具有防倒吸作用的儀器有(填字母) ____________。
(4)上述實驗裝置除①步驟簡單,操作方便,成功率高;②各步現象明顯;③對產品便于觀察這3個優點外,還有一個優點____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學與生命活動密切相關。以下是人體中血紅蛋白、肌紅蛋白與O2結合機制的相關研究,假定其環境溫度均為36.8℃。
(1)血紅蛋白Hb結合O2形成動脈血,存在反應①:HbH+(aq)+O2(g)![]() HbO2(aq)+H+(aq)。該反應可自發進行,則其ΔH______0(填“>”或“<”);血液中還同時存在反應②:CO2+H2O
HbO2(aq)+H+(aq)。該反應可自發進行,則其ΔH______0(填“>”或“<”);血液中還同時存在反應②:CO2+H2O![]() H++HCO3-,結合反應①②,肺部氧分壓_____(填“較高”或“較低”)有利于CO2排出體外,從化學平衡角度解釋原因 ____________。
H++HCO3-,結合反應①②,肺部氧分壓_____(填“較高”或“較低”)有利于CO2排出體外,從化學平衡角度解釋原因 ____________。
(2)肌肉中大量肌紅蛋白 Mb也可結合O2形成MbO2,即反應③:Mb(aq)+O2(g)![]() MbO2(aq),其平衡常數K=
MbO2(aq),其平衡常數K=![]() 。其它條件不變,隨著氧分壓p(O2)增大,K值___(填“變大”、“變小”或“不變”)。已知在氧分壓p(O2)=2.00 kPa 的平衡體系中,
。其它條件不變,隨著氧分壓p(O2)增大,K值___(填“變大”、“變小”或“不變”)。已知在氧分壓p(O2)=2.00 kPa 的平衡體系中, =4.0。吸入的空氣中p(O2)=21 kPa,計算此時 Mb與氧氣的最大結合度(平衡轉化率)約為_______________(保留兩位有效數字)。
=4.0。吸入的空氣中p(O2)=21 kPa,計算此時 Mb與氧氣的最大結合度(平衡轉化率)約為_______________(保留兩位有效數字)。
(3)Hb分子具有四個亞基,且每個亞基有兩種構型(T型和R型)。圖中,T0、R0表示未結合O2的T型和R型,且存在可逆的變構效應:T0![]() R0,正向平衡常數為K0;當四分子O2與Hb的四個亞基結合后,T4
R0,正向平衡常數為K0;當四分子O2與Hb的四個亞基結合后,T4![]() R4也是變構效應,正向平衡常數為K4。
R4也是變構效應,正向平衡常數為K4。

①已知某肺炎病人肺臟中T0+4O2![]() T4反應的n(O2)數據如下:
T4反應的n(O2)數據如下:
t/min | 0 | 2.0 | 4.0 | 6.0 | 8.0 |
n(O2)/10-6 mol | 1.68 | 1.64 | 1.58 | 1.50 | 1.40 |
計算2.0 min~8.0 min內以T的物質的量變化表示的反應速率v(T4)為_________mol·min-1。
②現假定R型Hb對O2的結合常數為KR,T型Hb對O2的結合常數為KT。已知KR>KT,則圖中K0____K4(填“>”或“<”)。
(4)氧氣是生命活動必不可少的物質。如下圖所示,以Pt為陽極,Pb(CO2)的載體,使CO2活化為陰極,電解經CO2飽和處理的KHCO3溶液可使氧氣再生,同時得到甲醇。其陰極反應式為____;從電解后溶液中分離甲醇的操作方法是_______________。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學與環境、科學、技術密切相關。下列有關說法中正確的是( )
A.華為首款5G手機搭載了智能的7nm制程SoC麒麟980芯片,此芯片主要成分是二氧化硅
B.用于制作N95型口罩的“熔噴布”主要原料是聚丙烯,聚丙烯的分子長鏈上無支鏈
C.國產飛機C919用到的氮化硅陶瓷是傳統有機非金屬材料
D.侯氏制堿法的工藝過程中應用了物質溶解度的差異
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com