
【題目】已知五種元素的原子序數大小順序為C>A>B>D>E,A、C同周期,B、C同主族。A與B形成的離子化合物A2B中所有離子的電子數相同,其電子總數為30;D和E可形成4核10個電子的分子。試回答下列問題:
(1)寫出四種元素的名稱:A________B_______C__________D_________
(2)用電子式表示化合物A2B的形成過程:______________________。
(3)寫出D元素形成的單質的結構式:__________________________。
(4)A、B兩種元素組成的化合物A2B2存在的化學鍵是________________。
(5)寫出下列物質的電子式:E與B形成的化合物__________________;A、B、E形成的化合物_____________。
【答案】 鈉 氧 硫 氮 ![]() N≡N 離子鍵和共價鍵
N≡N 離子鍵和共價鍵 ![]() 或
或![]()
![]()
【解析】A與B形成離子化合物A2B中所有粒子的電子數相同,且電子總數為30,所以每個離子都有10個電子,由化學式的結構可知,B帶2個單位負電荷,A帶1個單位正電荷,所以A是Na元素,B是O元素,因為A、C同周期,B與C同主族,所以C為S元素,D和E可形成4核10電子的分子,原子序數B>D>E,可知該分子是NH3,所以D是N元素,E是H元素,則
(1)根據以上分析可知A為鈉,B為氧,C為硫,D為氮;(2)A2B是Na2S,硫化鈉為離子化合物,用電子式表示Na2S的形成過程為![]() ;(3)氮氣的結構式為N≡N;(4)A、B兩種元素組成的化合物A2B2是過氧化鈉,存在的化學鍵是離子鍵和共價鍵;(5)E與B形成的化合物是水或雙氧水,電子式為
;(3)氮氣的結構式為N≡N;(4)A、B兩種元素組成的化合物A2B2是過氧化鈉,存在的化學鍵是離子鍵和共價鍵;(5)E與B形成的化合物是水或雙氧水,電子式為![]() 或
或![]() ;A、B、E形成的化合物為氫氧化鈉,NaOH中含有鈉離子與氫氧根離子構成的離子鍵、O與H形成共價鍵,電子式為
;A、B、E形成的化合物為氫氧化鈉,NaOH中含有鈉離子與氫氧根離子構成的離子鍵、O與H形成共價鍵,電子式為![]() 。
。


科目:高中化學 來源: 題型:
【題目】有A、B、C、D四種短周期元素, 它們的原子序數由A到D依次增大, 已知A和B原子有相同的電子層數, 且A的L層電子數是K層電子數的兩倍, C在空氣中燃燒時呈現黃色火焰, C的單質在加熱下與B的單質充分反應, 可以得到與D單質顏色相同的淡黃色固態化合物, 試根據以上敘述回答:
(1)元素名稱: A ______ B _____ C _____ D ______
(2)D元素位于周期表中___________周期____________族
(3)寫出AB2與C2B2反應的化學方程式:________________________________________。
(4)電子式表示化合物 C2D 的形成過程:________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知1g氫氣完全燃燒生成水蒸氣時放出熱量121kJ,且氧氣中1mol O=O鍵完全斷裂時吸收熱量496kJ,水蒸氣中1mol H﹣O鍵形成時放出熱量463kJ,則氫氣中1mol H﹣H鍵斷裂時吸收熱量為( )
A.920kJ
B.557kJ
C.436kJ
D.181kJ
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】能源是人類生活和社會發展的基礎,研究化學反應中的能量變化,有助于更好地利用化學反應為生產和生活服務。
(1)天然氣和可燃冰(mCH4nH2O)既是高效潔凈的能源,也是重要的化工原料。
①可燃冰(mCH4nH2O)屬于_____晶體,寫出CH4的結構式______。
②已知25℃、101kPa時,1g甲烷完全燃燒生成液態水放出55.65kJ熱量,則該條件下反應CH4(g)+2O2(g)=CO2(g)+2H2O(l)的 △H=___kJ/mol。
(2)用甲烷--氧氣堿性(KOH溶液)燃料電池作電源,電解CuCl2溶液。反應裝置如下圖所示:

①b電極名稱為______,d電極的電極反應式為__________。
②假設CuCl2溶液足量,當某電極上析出3.2g金屬Cu時,理論上燃料電池消耗的氧氣在標準狀兄下的體積是_______mL。
(3)25℃,101kPa條件下,14gN2和3gH2反應生成NH3的能量變化如下圖所示:
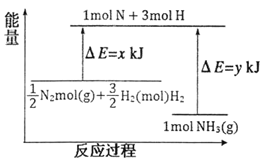
已知:①x=1127;
②25℃,101kPa下,N2(g)+3H2(g)![]() 2NH3(g) △H=-92kJmol-1。則y=______。
2NH3(g) △H=-92kJmol-1。則y=______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定溫度下,滿足下列條件的溶液一定呈酸性的是( )
A.能與金屬Al反應放出H2的溶液
B.加酚酞后顯無色的溶液
C.pH=6的某溶液
D.c(H+)>c(OH﹣)的任意水溶液
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某研究性學習小組設計了一組實驗來探究元素周期律。
甲同學根據元素非金屬性與對應最高價含氧酸之間的關系,設計了如圖1裝置來一次性完成同主族元素C和Si的非金屬性強弱比較的實驗研究;
乙同學設計了如圖2裝置來驗證鹵族元素性質的遞變規律,圖2中A、B、C三處分別是沾有NaBr溶液的棉花、濕潤的淀粉KI試紙、濕潤的紅紙。
已知常溫下濃鹽酸與高錳酸鉀能反應生成氯氣。

(1)從以下所給物質中選出甲同學設計的實驗所用到物質:圖1中試劑A、B為(填序號)____;
①稀硫酸溶液; ②濃鹽酸; ③碳酸鈉粉末;④Na2SO3溶液
寫出圖1燒瓶中發生反應的離子方程式為__________________________________________;
(2)甲同學所做實驗圖1燒杯中現象為____________________________________;
(3)乙同學所做實驗圖2中B處的現象為__________________________________;
(4)寫出圖2中A處發生反應的離子方程式為__________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知X、Y、Z三元素的原子序數依次增大,在周期表中X的原子半徑最小,Y、Z原子最外層電子數之和為10。C、D是由X、Y、Z中兩種元素組成的化合物,C通常狀況下為無色液體, D為無色非可燃性氣體,G為黃綠色單質氣體,J、M為金屬,I有漂白作用,反應①常用于制作印刷電路板。各物質之間的轉換關系如下圖,部分生成物省略。請回答下列問題:
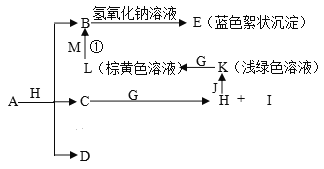
(1)寫出A的化學式__________________,C的電子式______________________,
D的結構式______________________________。
(2)將22.4L(標準狀況)D氣體通入1L 1mol/L NaOH溶液中,完全吸收后,溶液中除了Na+外,還大量存在的離子是______________________________。
(3)已知M溶于稀硝酸,溶液變成藍色,并放出無色氣體。請寫出該反應的離子方程式___________________________________________________________。
(4)檢驗化合物K中陽離子的實驗方法是______________________________________
(5)寫出反應K+G→L的化學方程式是________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對于放熱反應Zn+H2SO4===ZnSO4+H2↑,下列敘述正確的是( )
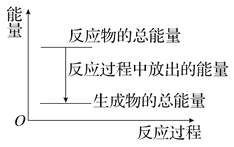
A. 反應過程中的能量關系可用上圖表示
B. 1 mol Zn的能量大于1 mol H2的能量
C. 若將其設計為原電池,則鋅作正極
D. 若將其設計為原電池,當有32.5 g Zn溶解時,正極放出的氣體一定為11.2 L
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是部分短周期元素原子半徑與原子序數的關系圖。字母代表元素,分析正確的是
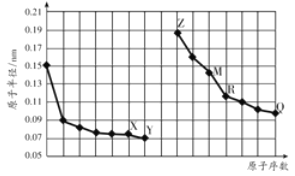
A. R在周期表的第15列
B. Y、Q兩種元素的氣態氫化物及其最高價氧化物的水化物均為強酸
C. 簡單離子的半徑:X>Z>M
D. Z的單質能從M與Q元素構成的鹽溶液中置換出單質M
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com