
【題目】已知 X、Y、Z、Q、R、E六種元素中,原子序數X<Y<Z<Q<R<E,其結構或性質信息如下表。
元素 | 結構或性質信息 |
X | 原子的L層上s電子數等于p電子數。 |
Y | 原子核外的L層有3個未成對電子。 |
Z | 在元素周期表的各元素中電負性僅小于氟。 |
Q | 單質常溫、常壓下是氣體,原子的M層上有1個未成對的p電子。 |
R | 核電荷數是Y與Q的核電荷數之和 |
E | 原子序數比R大3 |
請根據信息回答有關問題:
(1)元素Y的原子核外共有_____種不同運動狀態的電子,有______種不同能級的電子。
(2)X、Y、Z三種元素的電負性由高到低的排列次序依次為(寫元素符號)_______。
(3)R的最高化合價為_____________。R的一種配合物的化學式為RCl3·6H2O。
已知0.01 mol RCl3·6H2O在水溶液中用過量硝酸銀溶液處理,產生0.02 mol AgCl沉淀。此配合物最可能是___________。
A.[R(H2O)6]Cl3 B.[R(H2O)5Cl]Cl2·H2O
C.[R(H2O)4Cl2]Cl·2H2O D.[R(H2O)3Cl3]·3H2O
(4)元素E能形成八面體構型的配合物離子[E (YH3) x Q 2]+,則中心離子為(寫化學式)_______,配位體為(寫化學式)_______________________,x 的值為______。
【答案】 7 3 O、N、C +6 B CO3+ NH3、Cl— 4
【解析】X元素原子原子的L層上s電子數等于p電子數,核外電子排布為1s22s22p2,則X為C元素;Y元素原子核外的L層有3個未成對電子,核外電子排布為1s22s22p3,則Y為N元素;Z在元素周期表的各元素中電負性僅小于氟,則Z為O元素;Q元素單質常溫、常壓下是氣體,原子的M層上有1個未成對的p電子,原子核外電子排布為1s22s22p63s23p5,則Q為Cl;R核電荷數是Y與Q的核電荷數之和,其核電荷數=7+17=24,則R為Cr;E原子序數比R大3,則E為Co。(1)Y氮元素,原子核外有7個電子,即有7不同運動狀態的電子,有3種不同能級的電子;(2)在同周期元素中,從左向右,元素的電負性逐漸增大,所以X、Y、Z三種元素的電負性由高到低的排列次序依次為O、N、C;(3)R為鉻元素,它的最高化合價為+6價,根據題意可知,氯化鉻(CrCl3![]() 6H2O)和氯化銀的物質的量之比是0.01:0.02=1:2,根據氯離子守恒知,則CrCl3
6H2O)和氯化銀的物質的量之比是0.01:0.02=1:2,根據氯離子守恒知,則CrCl3![]() 6H2O化學式中含有2個氯離子為外界離子,剩余的1個氯離子是配原子,所以氯化鉻(CrCl3
6H2O化學式中含有2個氯離子為外界離子,剩余的1個氯離子是配原子,所以氯化鉻(CrCl3![]() 6H2O)的化學式可能為[Cr(H2O)5Cl]Cl2
6H2O)的化學式可能為[Cr(H2O)5Cl]Cl2![]() H2O,答案選B;(4)元素Co形成八面體構型的配合物離子[Co(NH3)xCl2]+中,根據配合物的有關定義可知,中心離子為Co3+,配位體為NH3,由于配合物形成的是八面體結構,所以該配合離子的配位數為6,即x+2=6,可知x 的值為4。
H2O,答案選B;(4)元素Co形成八面體構型的配合物離子[Co(NH3)xCl2]+中,根據配合物的有關定義可知,中心離子為Co3+,配位體為NH3,由于配合物形成的是八面體結構,所以該配合離子的配位數為6,即x+2=6,可知x 的值為4。


 期末沖刺100分創新金卷完全試卷系列答案
期末沖刺100分創新金卷完全試卷系列答案科目:高中化學 來源: 題型:
【題目】(1)已知:
①N2(g)+O2(g)=2NO(g) △H1= +180.5 kJmol-1
②4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H2=-905 kJmol-1
③2H2(g)+O2(g)=2H2O(g) △H3=-483.6 kJmol-1
請寫出N2和H2在高溫、高壓、催化劑條件下生成NH3的熱化學方程式________________。
(2)在一定溫度下,某恒容密閉容器中,發生反應:2X(g)+Y(g)![]() 2Z(g) △H<0,各物質的濃度隨時間變化如圖所示。
2Z(g) △H<0,各物質的濃度隨時間變化如圖所示。

①從反應開始到4min時平衡,Y的平均反應速率為____________________;
②根據圖中數據,4min時的平衡常數K= ______________________;
③若使重新平衡時體系中c(X)=c(Z),則改變的條件為_____________________(只寫一項)。
④若某時刻,V正(Y)=2V逆(Z),則反應_____達到平衡(填“已”或“未”)。
⑤圖中a、b點對應的正反應速率大小關系為Va________Vb(填“大于”、“小于”或“等于”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA代表阿伏加德羅常數的數值,下列說法中正確的是( )
A. 標準狀況時,22.4L二氯甲烷所含有的分子數為NA
B. 將16gO2與32gSO2在一定的條件下充分反應生成的SO3分子數為0.5NA
C. lmolNa2O2中含有的陰、陽離子總數是4NA
D. 44g丙烷中含有的非極性鍵數為2NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】隨著鹵素原子半徑的增大,下列遞變規律正確的是( )
A. 單質的熔、沸點逐漸降低 B. 鹵素離子的還原性逐漸增強
C. 單質的氧化性逐漸增強 D. 氣態氫化物的穩定性逐漸增強
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】據新華社消息,衛生部擬從2011年12月1日起,禁止在面粉生產中使用過氧化苯甲酰和過氧化鈣。過氧化苯甲酰的結構簡式如圖所示。

(1)過氧化苯甲酰的分子式為________,其一氯代物共有________種。
(2)工業上可以利用苯甲酰氯(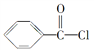 )和雙氧水為原料生產過氧化苯甲酰,寫出合成過氧化苯甲酰的化學反應方程式:___________________,該反應屬于________反應。
)和雙氧水為原料生產過氧化苯甲酰,寫出合成過氧化苯甲酰的化學反應方程式:___________________,該反應屬于________反應。
(3)過氧化苯甲酰用于面粉漂白后會產生苯甲酸:
![]()
![]() 。
。
苯甲酸的同分異構體中,屬于酯類的有__________,屬于酚類的有_________________ (寫結構簡式) 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列屬于氧化還原反應的是( )
A. 2NaHCO3![]() Na2CO3+CO2↑+H2O B. Na2O+H2O===2NaOH
Na2CO3+CO2↑+H2O B. Na2O+H2O===2NaOH
C. 2KI+Br2===2KBr+I2 D. MgO+2HCl===MgCl2+H2O
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com