
ĪŠŅ}─┐Ī┐tĪµĢrŻ¼AgX(X=CIĪóBr)Ą─╚▄Č╚Ęe┼cc(Ag+)║═c(X-)Ą─ŽÓ╗źĻPŽĄ╚ńłD╦∙╩ŠŻ¼ŲõųąAŠĆ▒Ē╩ŠAgClŻ¼BŠĆ▒Ē╩ŠAgBrŻ¼ęčų¬p(Ag+)=-lgc(Ag+)Ż¼p(X-)=-lgc(X-)ĪŻŽ┬┴ąšfĘ©š²┤_Ą─╩Ū

A. c³c┐╔▒Ē╩ŠAgClĄ─▓╗’¢║═╚▄ę║
B. b³cĄ─AgCl╚▄ę║╝ė╚ļAgNO3Š¦¾w┐╔ęįūā│╔a³c
C. AgCl(s)+Br-(aq) Ī·AgBr(s)+CI(aq)ŲĮ║Ō│ŻöĄK=10-4
D. a³cAgCl╚▄ę║║═b³cAgBr╚▄ę║Ą╚¾wĘe╗ņ║ŽŻ¼Ģ■╬÷│÷AgBr│┴ĄĒ
ĪŠ┤░ĖĪ┐D
ĪŠĮŌ╬÷Ī┐
Ė∙ō■łD╩ŠŻ¼A×ķ┬╚╗»Ńy╚▄ę║ųąp(Ag+)┼cp(Cl-)Ą─ĻPŽĄŪ·ŠĆŻ¼ŠĆ╔Ž├┐ę╗³cŠ∙×ķ┬╚╗»ŃyĄ─’¢║═╚▄ę║Ż¼╚ńa³cŻ¼ p(Ag+)=-lgc(Ag+)=5Ż¼ätc(Ag+)=10-5 mol/LŻ¼p(Cl-)= -lgc(Cl-)=5Ż¼ätc(Cl-)=10-5 mol/LŻ¼ätKsp(AgC1)=c(Ag)Ī┴c(Cl-)=10-5 mol/L Ī┴10-5 mol/L =10-10Ż¼═¼└ĒKsp (AgBr) =c(Ag+)c(Br-)=10-7Ī┴10-7=10-14ĪŻ
AĪóc³cŻ¼c(Ag+)=10-4mol/LŻ¼c(Cl-)=10-4 mol/LŻ¼ę“×ķ10-4Ī┴10-4>Kp (AgCl) =10-10Ż¼ šf├„╩ŪAgClĄ─▀^’¢║═╚▄ę║Ż¼▀xĒŚAÕeš`Ż╗
B. b³cĄ─AgC1╚▄ę║╝ė╚ļAgNO3Š¦¾wŻ¼c(Ag+)į÷┤¾Ż¼Ą½c(Cl-)╗∙▒Š▓╗ūāŻ¼▓╗─▄ūā│╔a³cŻ¼▀xĒŚBÕeš`Ż╗
C. tĪµĢrŻ¼AgCl(s)+Br-(aq) AgBr(s)+CI(aq)ŲĮ║Ō│ŻöĄK=![]() Ż¼▀xĒŚCÕeš`Ż╗
Ż¼▀xĒŚCÕeš`Ż╗
D. tĪµĢrŻ¼╚Īa³cĄ─AgC1╚▄ę║║═b³cAgBr╚▄ę║Ą╚¾wĘe╗ņ║ŽŻ¼ c(Ag+)=5Ī┴10-4 mol/L +![]() 10-7 mol/L
10-7 mol/L![]() 10-4 mol/LŻ¼c(Br-)=
10-4 mol/LŻ¼c(Br-)=![]() 10-7 mol/LŻ¼ätc(Ag+) c(Br-)=
10-7 mol/LŻ¼ätc(Ag+) c(Br-)=![]() 10-4 mol/LĪ┴
10-4 mol/LĪ┴![]() 10-7 mol/L>10-14Ż¼ėąõÕ╗»Ńy│┴ĄĒ╔·│╔Ż¼▀xĒŚDš²┤_ĪŻ
10-7 mol/L>10-14Ż¼ėąõÕ╗»Ńy│┴ĄĒ╔·│╔Ż¼▀xĒŚDš²┤_ĪŻ
┤░Ė▀xDĪŻ



| ─Ļ╝ē | Ė▀ųąšn│╠ | ─Ļ╝ē | │§ųąšn│╠ |
| Ė▀ę╗ | Ė▀ę╗├Ō┘Mšn│╠═Ų╦]ŻĪ | │§ę╗ | │§ę╗├Ō┘Mšn│╠═Ų╦]ŻĪ |
| Ė▀Č■ | Ė▀Č■├Ō┘Mšn│╠═Ų╦]ŻĪ | │§Č■ | │§Č■├Ō┘Mšn│╠═Ų╦]ŻĪ |
| Ė▀╚² | Ė▀╚²├Ō┘Mšn│╠═Ų╦]ŻĪ | │§╚² | │§╚²├Ō┘Mšn│╠═Ų╦]ŻĪ |
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐║Ż╦«ķ_░l└¹ė├Ą─▓┐Ęų▀^│╠╚ńłD╦∙╩ŠĪŻŽ┬┴ąėąĻPšfĘ©▓╗š²┤_Ą─╩Ū )

A. ║Ż╦«ĄŁ╗»Ą─ĘĮĘ©ų„ę¬ėąš¶sĘ©ĪóļŖØB╬÷Ę©ĪóļxūėĮ╗ōQĘ©Ą╚ĪŻ
B. ┐šÜŌ┤Ą│÷Ę©╩Ū╣żśIęÄ─Ż║Ż╦«╠ßõÕĄ─│Żė├ĘĮĘ©ĪŻŲõ╣ż╦ćĄ─Ųõųąę╗éĆŁh╣Ø╩Ū░č┬╚ÜŌ═©╚ļ╦ß╗»Ą─ØŌ┐s║Ż╦«Ż©╗“┐Ó¹uŻ®ųąĪŻ
C. į┌╣żśI╔Žę╗░Ń▀xė├Üõč§╗»Ō}╚▄ę║ū„×ķłD╩ŠųąĄ─│┴ĄĒä®ĪŻ
D. ė╔Mg(OH)2┐╔ęįųŲĄ├MgCl2Īż6H2OŻ¼─│┼d╚żąĪĮM═¼īW×ķ┴╦ųŲ╚Ī¤o╦«MgCl2Ż¼ų▒Įė╝ė¤ßMgCl2Īż6H2O╝┤┐╔ųŲéõ
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐ęį▒ĮĘė×ķįŁ┴ŽĄ─║Ž│╔┬ĘŠĆ╚ńŽ┬╦∙╩ŠŻ¼šł░┤ę¬Ū¾ū„┤Ż║
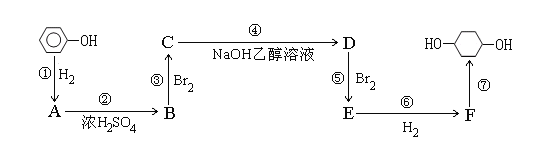
Ż©1Ż®īæ│÷ęįŽ┬╬’┘|Ą─ĮYśŗ║å╩ĮŻ║
B ____________________ Ż╗ E ______________________Ż╗
Ż©2Ż®īæ│÷Ę┤æ¬ó▄ó▀Ą─╗»īWĘ┤æ¬ĘĮ│╠╩ĮŻ║
ó▄ __________________________________________
ó▀ ___________________________________________
Ż©3Ż®Ę┤æ¬ó▌╩Ū1:1╝ė│╔┐╔ęįĄ├ĄĮEŻ¼═¼Ģr┐╔─▄Ą├ĄĮĄ─Ė▒«a╬’Ą─ĮYśŗ║å╩Į×ķŻ║
_______________________________________________________
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐ī”ė┌╣żśIųŲH2SO4▀^│╠ųąĄ─Ę┤æ¬Ż║2SO2(g)+O2![]() 2SO3(g)Ž┬┴ąšfĘ©Õeš`Ą─╩Ū
2SO3(g)Ž┬┴ąšfĘ©Õeš`Ą─╩Ū
A. ╩╣ė├║Ž▀mĄ─┤▀╗»ä®┐╔ęį╝ė┐ņ╗»īWĘ┤æ¬╦┘┬╩
B. į÷┤¾O2ØŌČ╚┐╔ęį╩╣SO2▐D╗»┬╩▀_ĄĮ100%
C. ĮĄ£žĢrŻ¼Ę┤æ¬╦┘┬╩£pąĪ
D. ┐sąĪ├▄ķ]╚▌Ų„Ą─¾wĘeŻ¼┐╔ęį╝ė┐ņĘ┤æ¬╦┘┬╩
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐Ė∙ō■Ž┬┴ąīŹ“×ā╚╚▌Ą├│÷Ą─ĮYšōš²┤_Ą─╩Ū
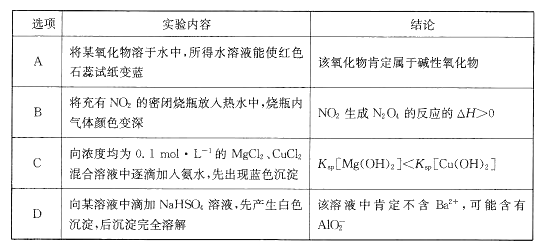
A. A B. B C. C D. D
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐ęčų¬─│£žČ╚Ž┬Ż¼MnCO3ĪóMnSĄ─╚▄Č╚ĘeĘųäe×ķ2Ż«0Ī┴10 -11Īó5Ż«0Ī┴10 -14ĪŻŽ┬┴ą═ŲöÓ▓╗š²┤_Ą─╩Ū ( )
A. ╠╝╦ßÕiĄ─╚▄ĮŌČ╚┤¾ė┌┴“╗»ÕiĄ─╚▄ĮŌČ╚
B. ╠╝╦ßÕi▐D╗»│╔┴“╗»ÕiĄ─ļxūėĘĮ│╠╩Į×ķMnCO3(s)+S2-(aq)![]() MnS(s)+ CO32-(aq)
MnS(s)+ CO32-(aq)
C. ╠╝╦ßÕi▐D╗»│╔┴“╗»ÕiĄ─ŲĮ║Ō│ŻöĄK=2Ż«5Ī┴10-3
D. į┌║¼ŽÓ═¼ØŌČ╚Ą─CO32ę╗Ż¼S2-Ą─╚▄ę║ųąĄ╬╝ė┬╚╗»Õi╚▄ę║Ż¼Ž╚«a╔·│┴ĄĒ╩ŪMnS
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐ŌÆ╩Ūę╗ĘNųąĄ╚╗ŅØŖĮī┘Ż¼╗»║Žār×ķ+2ār║═+3ārŻ¼ŲõųąCoC12ęū╚▄ė┌╦«ĪŻ─│ąŻ═¼īWįOėŗīŹ“×ųŲ╚ĪŻ©CH3COOŻ®2CoŻ©ęę╦ßŌÆŻ®▓ó“×ūCŲõĘųĮŌ«a╬’ĪŻ╗ž┤Ž┬┴ąå¢Ņ}Ż║
Ż©1Ż®╝ū═¼īWė├Co2O3┼c¹}╦ßĘ┤æ¬ųŲéõCoC124H2OŻ¼ŲõīŹ“×čbų├╚ńŽ┬Ż║

ó┘¤²Ų┐ųą░l╔·Ę┤æ¬Ą─ļxūėĘĮ│╠╩Į×ķ______ĪŻ
ó┌ė╔¤²Ų┐ųąĄ─╚▄ę║ųŲ╚ĪĖ╔į’Ą─CoC124H2OŻ¼▀ĆąĶĮø▀^Ą─▓┘ū„ėąš¶░lØŌ┐sĪó______ĪóŽ┤£ņĪóĖ╔į’Ą╚ĪŻ
Ż©2Ż®ęę═¼īW└¹ė├╝ū═¼īWųŲĄ├Ą─CoC124H2Oį┌┤ū╦ßĘšć·ųąųŲĄ├¤o╦«Ż©CH3COOŻ®2CoŻ¼▓ó└¹ė├Ž┬┴ąčbų├Öz“ׯ©CH3COOŻ®2Coį┌Ą¬ÜŌÜŌĘšųąĄ─ĘųĮŌ«a╬’ĪŻęčų¬PdC12╚▄ę║─▄▒╗CO▀ĆįŁ×ķPdĪŻ

ó┘čbų├EĪóF╩Ūė├ė┌Öz“×CO║═CO2Ą─Ż¼Ųõųą╩óĘ┼PdC12╚▄ę║Ą─╩Ūčbų├______Ż©╠ŅĪ░EĪ▒╗“Ī░FĪ▒Ż®ĪŻ
ó┌čbų├GĄ─ū„ė├╩Ū______Ż╗EĪóFĪóGųąĄ─įć䮊∙ūŃ┴┐Ż¼ė^▓ņĄĮIųąč§╗»Ń~ūā╝tŻ¼Jųą╣╠¾wė╔░ū╔½ūā╦{╔½Ż¼Kųą╩»╗ę╦«ūā£åØ߯¼ät┐╔Ą├│÷Ą─ĮYšō╩Ū______ĪŻ
ó█═©Ą¬ÜŌĄ─ū„ė├╩Ū______ĪŻ
ó▄īŹ“×ĮY╩°ĢrŻ¼Ž╚Ž©£ńD║═I╠ÄĄ─ŠŲŠ½¤¶Ż¼ę╗Č╬Ģrķg║¾į┘ĻPķ]ÅŚ╗╔ŖAŻ¼Ųõ─┐Ą─╩Ū______ĪŻ
ó▌╚¶ęę╦ßŌÆūŅĮKĘųĮŌ╔·│╔╣╠æBč§╗»╬’XĪóCOĪóCO2ĪóC2H6Ż¼ŪęnŻ©XŻ®Ż║nŻ©COŻ®Ż║nŻ©CO2Ż®Ż║nŻ©C2H6Ż®=1Ż║4Ż║2Ż║3Ż©┐šÜŌųąĄ─│╔Ęų▓╗ģó┼cĘ┤æ¬Ż®Ż¼ätęę╦ßŌÆį┌┐šÜŌÜŌĘšųąĘųĮŌĄ─╗»īWĘĮ│╠╩Į×ķ______ĪŻ
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐Ż©1Ż®ęčų¬Ž┬┴ąĘ┤æ¬Ą─¤ß╗»īWĘĮ│╠╩ĮŻ║
6C(s)+5H2(g)+3N2(g)+9O2(g)=2C3H5(ONO2)3(l) Ī„H1
2 H2(g)+ O2(g)= 2H2O(g) Ī„H2
C(s)+ O2(g)=CO2(g) Ī„H3
ätĘ┤æ¬4C3H5(ONO2)3(l)= 12CO2(g)+10H2O(g) + O2(g) +6N2(g)Ą─Ī„H×ķ__________
Ż©2Ż®Č■č§╗»╠╝║Ž│╔╝ū┤╝╩Ū╠╝£p┼┼Ą─ą┬ĘĮŽ“Ż¼īóCO2▐D╗»×ķ╝ū┤╝Ą─¤ß╗»īWĘĮ│╠╩Į×ķŻ║CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ”żH
CH3OH(g)+H2O(g) ”żH
ó┘╚Īę╗Č©¾wĘeCO2║═H2Ą─╗ņ║ŽÜŌ¾wŻ©╬’┘|Ą─┴┐ų«▒╚×ķ1Ī├3Ż®Ż¼╝ė╚ļ║Ń╚▌├▄ķ]╚▌Ų„ųąŻ¼░l╔·╔Ž╩÷Ę┤æ¬Ę┤æ¬▀^│╠ųą£yĄ├╝ū┤╝Ą─¾wĘeĘųöĄ”š(CH3OH)┼cĘ┤欣žČ╚TĄ─ĻPŽĄ╚ńłD1╦∙╩ŠŻ¼ätįōĘ┤æ¬Ą─”żH_______0Ż©╠ŅĪ░ŻŠĪ▒ĪóĪ░Ż╝Ī▒╗“Ī░ŻĮĪ▒Ż¼Ž┬═¼Ż®

ó┌į┌ā╔ĘN▓╗═¼Śl╝■Ž┬░l╔·Ę┤æ¬Ż¼£yĄ├CH3OHĄ─╬’┘|Ą─┴┐ļSĢrķgūā╗»╚ńłD2╦∙╩ŠŻ¼Ū·ŠĆIĪóó“ī”æ¬Ą─ŲĮ║Ō│ŻöĄĻPŽĄ×ķKó±_____________Kó“ĪŻ
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐į┌į¬╦žų▄Ų┌▒ĒųąŻ¼╦∙║¼į¬╦žĘNŅÉūŅČÓĄ─ūÕ╩Ū
A.ó°ūÕB.ó±AūÕ
C.0ūÕD.ó¾BūÕ
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
ć°ļHīWąŻā×▀x - ŠÜ┴Ģāį┴ą▒Ē - įćŅ}┴ą▒Ē
║■▒▒╩Ī╗ź┬ōŠW▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ŲĮ┼_ | ŠW╔Žėą║”ą┼Žó┼eł¾īŻģ^ | ļŖą┼įp“_┼eł¾īŻģ^ | ╔µÜv╩Ę╠ō¤oų„┴xėą║”ą┼Žó┼eł¾īŻģ^ | ╔µŲ¾ŪųÖÓ┼eł¾īŻģ^
▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ļŖįÆŻ║027-86699610 ┼eł¾Ó]ŽõŻ║58377363@163.com