
【題目】室溫下,用0.100molL﹣1 NaOH溶液分別滴定20.00mL 0.100molL﹣1的鹽酸和醋酸,滴定曲線如圖所示.下列說法正確的是( ) 
A.Ⅱ表示的是滴定醋酸的曲線
B.pH=7時,滴定醋酸消耗的V(NaOH)小于20mL
C.V(NaOH)=20.00mL時,兩份溶液中c(Cl﹣)=c(CH3COO﹣)
D.V(NaOH)=10.00mL時,醋酸溶液中c(Na+)>c(CH3COO﹣)>c(H+)>c(OH﹣)
【答案】B
【解析】解:A.醋酸是弱電解質,HCl是強電解質,相同濃度的醋酸和HCl溶液,醋酸的pH>鹽酸,所以I是滴定醋酸的曲線,故A錯誤;
B.pH=7時,溶液呈中性,醋酸鈉溶液呈堿性,要使溶液呈中性,則醋酸的體積稍微大于NaOH,所以滴定醋酸消耗的V(NaOH)小于20mL,故B正確;
C.V(NaOH)=20.00mL時,兩種溶液中的溶質分別是醋酸鈉和NaCl,醋酸根離子水解、氯離子不水解,所以c(Cl﹣)>c(CH3COO﹣),故C錯誤;
D.V(NaOH)=10.00mL時,醋酸溶液中的溶質為等物質的量濃度的CH3COOH、CH3COONa,醋酸電離程度大于醋酸根離子水解程度,溶液呈酸性,則c(H+)>c(OH﹣),再結合電荷守恒得c(Na+)<c(CH3COO﹣),故D錯誤;
故選B.


科目:高中化學 來源: 題型:
【題目】實驗室有密度為1.8g/m3、質簠分數為98%的“化學純”硫酸.
(1)取該濃硫酸1L加蒸餾水稀釋至18L,稀釋后硫酸的物質的量濃度為
(2)現有Na2CO3、NaHCO3組成的混合物,加熱到質量不再減少為止,放出標準狀況下氣體2.24L,取稀釋后硫酸200mL恰好與剩余的殘渣完全反應,又放出標準狀況下氣體AL,試計算①原混合物的質量
②原混合物Na2CO3與NaHCO3物質的量之比
③A= .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據所學知識完成題目:
(1)30%的H2SO4和50%的H2SO4等質量混合后,所得溶液的質量分數(填“大于”、“小于”或“等于”)40%,如果等體積混合,混合后溶液的質量分數(填“大于”、“小于”或“等于”)40%.
(2)已知98%的濃H2SO4的物質的量濃度為18.4molL﹣1 , 試判斷49%的H2SO4的物質的量濃度(填“大于”、“小于”或“等于”)9.2molL﹣1 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有轉化關系(其他產物及反應所需條件均已略去).
A ![]() B
B ![]() C
C ![]() D
D ![]() E
E ![]() F,以下推斷錯誤的是( )
F,以下推斷錯誤的是( )
A.當X是鹽酸時,則F是稀硝酸
B.當X是氫氧化鈉時,則F是稀硝酸
C.當X是氫氧化鈉時,B跟Cl2反應可能有白煙現象
D.當X是氫氧化鈉時,B能使酸性高錳酸鉀溶液褪色
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下面是實驗室制乙烯并檢驗其性質的裝置圖,請回答: 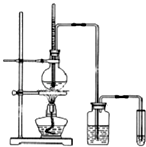
(1)寫出圓底燒瓶中反應的方程式 , 反應類型;
(2)燒瓶中混合液逐漸變黑,并產生某些無機雜質氣體,寫出產生雜質氣體的化學方程式:;
(3)為了檢驗乙烯的生成,試管中應盛放 , 現象為;
(4)洗瓶中盛放的試劑為 , 作用 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有關 ![]() 分子結構的下列敘述中正確的是( ) ①除苯環外的其余碳原子有可能都在一條直線上
分子結構的下列敘述中正確的是( ) ①除苯環外的其余碳原子有可能都在一條直線上
②除苯環外的其余碳原子不可能都在一條直線上
③12個碳原子不可能都在同一平面上
④12個碳原子有可能都在同一平面上.
A.①②
B.②③
C.①③
D.②④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NaClO和KAl(SO4)2都是重要的化工產品,均可應用于造紙業。
(1)NaClO溶液pH>7,用離子方程式表示原因__________
(2)根據NaClO的性質推測,在紙漿中加入NaClO溶液的目的是_________________。
(3)某小組同學用如圖所示裝置探究飽和NaClO和KAl(SO4)2溶液混合反應的實驗。打開活塞向燒瓶中加入飽和KAl(SO4)2溶液,產生大量的白色膠狀沉淀。反應的離子方程式_____________。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列表述正確的是( )
A.氫氧根離子的電子式是 ![]()
B.二氧化碳分子的比例模型是 ![]()
C.芳香烴的組成通式是CnH2n﹣6(n≥6)
D.12C和14C的原子結構示意圖均可表示為 ![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各組比較不正確的是 ( )
A. 鋰與水反應不如鈉與水反應劇烈
B. 堿金屬Li、Na、K單質都能在O2中燃燒生成過氧化物
C. 熔、沸點:Li>Na>K
D. 堿性:LiOH<NaOH<KOH
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com