
【題目】物質分離、提純的常用裝置如圖所示,根據題意選擇合適的裝置填入相應位置。

(1)我國明代《本草綱目》中收載藥物1892種,其中“燒酒”條目下寫到:“自元時始創其法,用濃酒和糟入甑,蒸令氣上……其清如水,味極濃烈,蓋酒露也。”這里所用的“法”所用的是__裝置(填“甲”、“乙”、“丙”、“丁”或“戊”,下同)。
(2)《本草衍義》中對精制砒霜過程的敘述為:“取砒之法,將生砒就置火上,以器覆之,令砒煙上飛著覆器,遂凝結累然下重如乳,尖長者為勝,平短者次之。”文中涉及的操作方法所用是_____裝置。
(3)海洋植物如海帶、海藻中含有大量的碘元素,碘元素以碘離子的形式存在。實驗室里從海藻中提取碘的流程如圖:
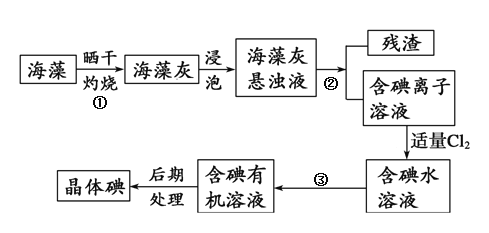
其中分離步驟①、②、③所用分別為:_____裝置、_____裝置、_____裝置。
科目:高中化學 來源: 題型:
【題目】一定量的CO2與足量的碳在體積可變的恒壓密閉容器中反應:C(s)+CO2(g)![]() 2CO(g)。平衡時,體系中氣體體積分數與溫度的關系如下圖所示:
2CO(g)。平衡時,體系中氣體體積分數與溫度的關系如下圖所示:

已知:氣體分壓(P分)=氣體總壓(P總)×體積分數。下列說法正確的是
A. 550℃時,若充入惰性氣體,正,逆 均減小,平衡不移動
B. 650℃時,反應達平衡后CO2的轉化率為25.0%
C. T℃時,若充入等體積的CO2和CO,平衡向逆反應方向移動
D. 925℃時,用平衡分壓代替平衡濃度表示的化學平衡常數KP=24.0P總
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各對物質,互為同系物的是( )
A. CH3CH2C1與CH3CHCl﹣CH2ClB. CH3COOH與CH3CH2COOCH3
C. 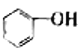 與
與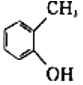 D.
D. ![]() 與
與![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】4℃時在100mL水中溶解了22.4L氯化氫氣體(在標準狀況下測得)。下列關于所形成的溶液說法中,正確的是( )
A. 該溶液溶質的物質的量濃度為10mol·L-1
B. 若已知該溶液的密度,則可求得溶液溶質的物質的量濃度
C. 該溶液中含有0.1mol的Cl-
D. 該溶液的體積為22.5L
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】主族元素![]() 、
、![]() 、
、![]() 、
、![]() 的原子序數依次增加,且均不大于20。
的原子序數依次增加,且均不大于20。![]() 、
、![]() 、
、![]() 族序數之和為10;
族序數之和為10;![]() 的原子半徑在同周期主族元素中最小;
的原子半徑在同周期主族元素中最小;![]() 與
與![]() 形成的化合物常溫下可與飽和
形成的化合物常溫下可與飽和![]() 溶液反應,產生的氣體常用于切割和焊接金屬。下列說法錯誤的是( )
溶液反應,產生的氣體常用于切割和焊接金屬。下列說法錯誤的是( )
A.簡單離子半徑:![]()
B.![]() 的單質是人類將太陽能轉化為電能的常用材料
的單質是人類將太陽能轉化為電能的常用材料
C.![]() 與
與![]() 形成的化合物均滿足8電子穩定結構
形成的化合物均滿足8電子穩定結構
D.![]() 與
與![]() 形成的化合物與飽和
形成的化合物與飽和![]() 溶液的反應可選用啟普發生器
溶液的反應可選用啟普發生器
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】標準狀態下,氣態分子斷開1 mol化學鍵的焓變稱為鍵焓。已知H—H、H—O和O===O鍵的鍵焓ΔH分別為436 kJ·mol-1、463 kJ·mol-1和495 kJ·mol-1。下列熱化學方程式正確的是
A. H2O(g)===H2+1/2O2(g)ΔH=-485 kJ·mol-1
B. H2O(g)===H2(g)+1/2O2(g) ΔH=+485 kJ·mol-1
C. 2H2(g)+O2(g)===2H2O(g) ΔH=+485 kJ·mol-1
D. 2H2(g)+O2(g)===2H2O(g) ΔH=-485 kJ·mol-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:①A的產量通常用來衡量一個國家的石油化工水平;②2CH3CHO+O2![]() 2CH3COOH。現以A為主要原料合成化合物E,其合成路線如圖1所示。回答下列問題:
2CH3COOH。現以A為主要原料合成化合物E,其合成路線如圖1所示。回答下列問題:
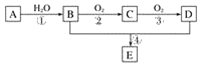
圖1
(1)寫出下列物質的官能團名稱:
B:____________________;D:____________________。
(2)反應④的化學方程式為________________________________________________,反應類型:________。
(3)某學習小組設計物質B催化氧化的實驗裝置如下,根據圖2裝置回答問題。
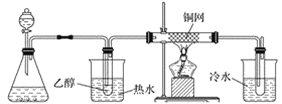
甲 乙 丙 丁
圖2
①裝置甲錐形瓶中盛放的固體藥品可能為________(填字母)。
A Na2O2 B KCl C Na2CO3 D MnO2
②實驗過程中,丙裝置硬質玻璃管中發生反應的化學方程式為_________________________。
③物質B的催化氧化產物與葡萄糖具有相同的特征反應,將所得的氧化產物滴加到新制氫氧化銅懸濁液中加熱,現象為______________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列“實驗結論”與“實驗操作及現象”相符的一組是
選項 | 實驗操作及現象 | 實驗結論 |
A | 向某溶液中加入 | 該溶液中一定含有 |
B | 向某溶液中加入稀鹽酸,有無色氣體產生 | 該溶液中一定含有 |
C | 向某溶液中加入 | 該溶液中一定含有 |
D | 向某溶液中加入酚酞溶液,溶液變為紅色 | 該溶液中一定含有 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,某化學小組探究硝酸銀溶液的性質。
裝置 | 實驗序號 | 實驗操作 | 實驗現象 |
| 實驗I | 向試管中滴加2%氨水并不斷振蕩 | 產生棕褐色沉淀,繼續滴加沉淀消失 |
實驗II | 1.向試管中加入0.1mol·L-lNaOH溶液1mL 2.繼續滴加3%H2O2至過量 | 1.產生棕褐色沉淀 2.產生大量無色無味氣體,有黑色沉淀生成 | |
實驗III | 1.向試管中滴加1mL0.1molL-1KI溶液 2.取少量上層清液于試管甲中,加入淀粉溶液 | 1.產生黃色沉淀 2.溶液無明顯變化 |
已知:AgOH是一種白色固體,常溫下極不穩定,易分解為棕褐色難溶于水的氧化銀固體
(1)常溫下,0.1mo1L-1AgNO3溶液pH約為4,請用離子方程式解釋原因___。
(2)實驗I中,反應的化學方程式是___。
(3)實驗II中,經檢驗,黑色沉淀的成分為Ag。有Ag產生的化學方程式是___。經測定,實驗產生的氣體體積遠遠大于該反應的理論值,可能的原因是___。
(4)實驗中,產生黃色沉淀的離子方程式是___。有同學猜想,I-有還原性,Ag+有氧化性,AgNO3溶液與KI溶液應該可以發生氧化還原反應。他設計了如圖原電池,做實驗IV證明了猜想成立。其中,在A燒杯中,石墨電極表面變亮,經檢測這種光亮的物質為銀單質。乙溶液是___,檢驗B燒杯中產物的操作及現象是___,該氧化還原反應的離子方程式是__。

(5)對比實驗III和實驗IV,實驗III無I2生成的可能原因是___(寫出兩條)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com