
【題目】Ba(NO3)2可用于生產煙花。某主要生產BaCl2、BaCO3、BaSO4的化工廠利用某種鋇泥[主要含有BaCO3、Ba(FeO2)2、極少量CuCO3等]制取Ba(NO3)2晶體,其部分工藝流程如下:

已知:Fe3+和Fe2+以氫氧化物形式沉淀完全時,溶液的pH分別為3.2和9.7。
(1)酸溶時不使用濃硝酸的原因是________。
(2)酸溶后溶液中pH=1,Ba(FeO2)2與HNO3的反應化學方程式為___________。
(3)該廠結合本廠實際,中和選用的X為____________(填化學式);中和使溶液中________(填離子符號)的濃度減少(中和引起的溶液體積變化可忽略)。
(4)濾液得到Ba(NO3)2晶體的操作依次為_____________、_____________、過濾。
(5)為了減少環境污染,請對上述流程中不合理的設計進行改進,改進措施是_______。
【答案】濃HNO3易揮發、分解 Ba(FeO2)2+8HNO3=Ba(NO3)2+2Fe(NO3)3+4H2O BaCO3 Fe3+、H+ 蒸發濃縮 冷卻結晶 洗滌廢渣并回收洗滌液
【解析】
BaCO3中含有Ba(FeO2)2、極少量CuCO3等,其中Ba(FeO2)2中鋇元素為+2價,鐵元素為+3價,加入硝酸,在容器中充分溶解得到溶液,此溶液中含有鋇離子、銅離子、三價鐵離子,可加入X碳酸鋇,調節溶液pH=4~5,使鐵離子、銅離子水解生成氫氧化鐵沉淀、氫氧化銅沉淀,過濾后濾渣為氫氧化鐵、氫氧化銅,濾液中主要含有硝酸、硝酸鋇,經蒸發濃縮,冷卻結晶,過濾得到硝酸晶體,據此分析解答。
BaCO3中含有Ba(FeO2)2、極少量CuCO3等,其中Ba(FeO2)2中鋇元素為+2價,鐵元素為+3價,加入硝酸,在容器中充分溶解得到溶液,此溶液中含有鋇離子、銅離子、三價鐵離子,可加入X碳酸鋇,調節溶液pH=4~5,使鐵離子、銅離子水解生成氫氧化鐵沉淀、氫氧化銅沉淀,過濾后濾渣為氫氧化鐵、氫氧化銅,濾液中主要含有硝酸、硝酸鋇,經蒸發濃縮,冷卻結晶,過濾得到硝酸晶體,
(1)濃HNO3易揮發、分解,則酸溶時不宜使用濃硝酸;
故答案為:濃HNO3易揮發、分解;
(2)酸溶后溶液中pH=1,Ba(FeO2)2與HNO3的反應生成硝酸鋇、硝酸鐵和水,反應的化學方程式為Ba(FeO2)2+8HNO3=Ba(NO3)2+2Fe(NO3)3+4H2O;
故答案為:Ba(FeO2)2+8HNO3=Ba(NO3)2+2Fe(NO3)3+4H2O;
(3)該廠結合本廠實際,中和選用的X必須能消耗過量的硝酸并使鐵離子沉淀而除去,且不引入新雜質,可為BaCO3;中和使溶液中Fe3+、H+的濃度減少;
故答案為:BaCO3;Fe3+、H+;
(4)濾液中主要含有硝酸、硝酸鋇,則濾液得到Ba(NO3)2晶體的操作依次為蒸發濃縮,冷卻結晶,過濾;
故答案為:蒸發濃縮;冷卻結晶;
(5)為了減少環境污染,請對上述流程中不合理的設計進行改進,改進措施是洗滌廢渣并回收洗滌液;
故答案為:洗滌廢渣并回收洗滌液。


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
【題目】丙三酸是一種有機酸,用H3A表示。25℃時,向1molL-1的H3A溶波中逐滴加入NaOH溶液,滴加過程中各種含A微粒物質的物質的量分數(δ)隨溶液pH的變化曲線如圖所示。下列相關說法錯誤的是( )
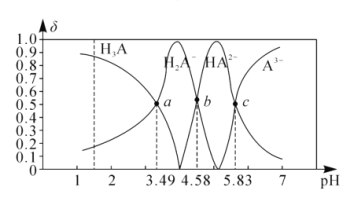
A.a點溶液中:c(H2A-)>c(Na+)>c(H+)>c(OH-)
B.25℃時,H3A的第二步電離平衡常數的數量級為10-5
C.b點溶液中:c(Na+)+c(H+)=3c(H2A-)+3c(A3-)+c(OH-)
D.當該溶液中c(HA2-)=c(A3-)時,溶液中水電離出的c(H+)>10-7molL-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】釩(V)、 錳(Mn)、鐵(Fe)、 砷(As)、硒(Se)均為第四周期的元素,完成下列問題。
(1)釩有+2、+3、+4、+5等幾種化合價。這幾種價態中,最穩定的是______。
(2)基態Fe2+的價層電子的軌道表示式為________,檢驗Fe3+可以用KSCN溶液,寫出SCN-的一種等電子體分子_______。
(3)部分電離能數據如下:
Mn:![]() =717kJ/mol ,
=717kJ/mol ,![]() =1509kJ/mol ,
=1509kJ/mol ,![]() =3248kJ/mol ,
=3248kJ/mol ,
Fe:![]() =759kJ/mol,
=759kJ/mol,![]() =1562kJ/mol ,
=1562kJ/mol ,![]() =2957kJ/mol ,
=2957kJ/mol ,
根據數據可知,氣態Mn2+ 再失去一個電子比氣態Fe2+ 再失去一個電子難,其原因是____________________。
(4)沸點:NH3__________AsH3(填“>”、“<”或“=”),原因是_____________________。
(5)H2SeO4和H2SeO3是硒的兩種含氧酸,請根據結構與性質的關系,解釋H2SeO4比H2SeO3 酸性強的原因___________________________________ 。
(6)科學家通過X射線推測膽礬中既含有配位鍵,又含有氫鍵,其結構示意圖可簡單表示如下:
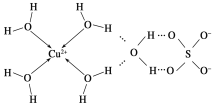
膽礬的化學式用配合物的形式表示為____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】香葉醇、橙花醇和乙酸橙花酯在工業上用作香料,它們可由月桂烯來合成。
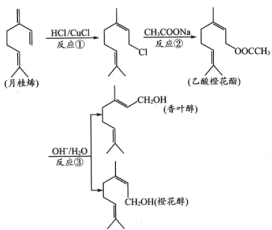
下列說法正確的是
A.反應①②③均為取代反應
B.月桂烯分子中所有碳原子全部處在同一平面上
C.香葉醇和橙花醇具有相同的分子式
D.乙酸橙花酯可以發生取代、加成、氧化和聚合反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】不飽和酯類化合物在藥物、涂料等領域應用廣泛。
(1)下列關于化合物Ⅰ的說法,正確的是___。

A.可能發生酯化反應和銀鏡反應
B.化合物Ⅰ含有5種官能團
C.1mol化合物Ⅰ在一定條件下最多能與7molH2發生加成反應
D.能與溴發生取代和加成反應
(2)下面反應是一種由烯烴直接制備不飽和酯的新方法。
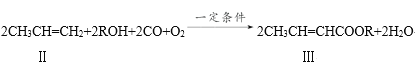
化合物Ⅲ與足量的NaOH溶液共熱的化學方程式為__;反應類型是__。
(3)2—丁烯酸甲酯(E)是一種用于合成抗血栓藥的中間體,其合成路線如下:
CH4+CO![]() CH3CHO(A)
CH3CHO(A)![]() B
B![]() CH3CH=CHCOOH(D)
CH3CH=CHCOOH(D)![]() E
E
已知:HCHO+CH3CHO![]() CH2=CHCHO+H2O
CH2=CHCHO+H2O
①B中官能團的名稱為___。
②E的結構簡式為___。
③試劑C可選用下列中的___。
a.溴水 b.銀氨溶液 c.酸性KMnO4溶液 d.新制Cu(OH)2懸濁液
④B在一定條件下可以生成高聚物F,該反應的化學方程式為____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列敘述正確的是( )
A.FeO與稀硝酸反應屬于復分解反應
B.常溫下Fe與濃硝酸不反應
C.銅片與濃硝酸發生離子反應:Cu+NO3-+4H+=Cu2++NO2↑+2H2O
D.向Fe(NO3)2稀溶液中加入鹽酸發生反應:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示甲是某學生驗證銅和濃硝酸反應的裝置,乙、丙是另外兩位同學對甲裝置改進后的裝置:

(1)甲、乙、丙三個裝置中都發生的反應的化學方程式:__。
(2)和甲裝置相比,乙裝置的優點是
①__;
②__。
(3)為了進一步驗證NO2和水的反應,某學生設計了丙裝置。實驗時先關閉止水夾__,再打開止水夾__,才能使NO2氣體充滿②試管;當氣體充滿②試管后,將銅絲提起與溶液脫離。欲使燒杯中的水進入②試管,應該__。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】據圖回答下列問題:

(1)若燒杯中的溶液為稀硫酸,則觀察到的現象是___________,負極反應式為___________。
(2)若燒杯中的溶液為氫氧化鈉溶液,則正極反應為___________,總反應的化學方程式為___________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com