
【題目】甲烷燃燒時的能量變化如圖,有關說法正確的是( )

A.圖1中反應為:CH4(g)+2O2(g)=CO2(g)+2H2O(l) H=+890.3kJ/mol
B.圖2中反應為:CH4(g)+![]() O2(g)=CO(g)+2H2O(g) H=﹣607.3kJ/mol
O2(g)=CO(g)+2H2O(g) H=﹣607.3kJ/mol
C.由圖可以推得:CO(g)+![]() O2(g)=CO2(g) H=﹣283kJ/mol
O2(g)=CO2(g) H=﹣283kJ/mol
D.由圖可以推知:等物質的量的CO2和CO,CO2具有的能量高
【答案】C
【解析】
A.根據圖像分析,反應物的總能量高于生成物總能量,則圖1中反應為:CH4(g)+2O2(g)=CO2(g)+2H2O(l) H=-890.3kJ/mol,A錯誤;
B.根據圖像分析,生成物水的狀態是液態,則圖2中反應為:CH4(g)+![]() O2(g)=CO(g)+2H2O(l) H=﹣607.3kJ/mol,B錯誤;
O2(g)=CO(g)+2H2O(l) H=﹣607.3kJ/mol,B錯誤;
C.CO(g)+![]() O2(g)=CO2(g) 的焓變可根據CH4(g)+2O2(g)=CO2(g)+2H2O(l) H=-890.3kJ/mol和反應H=﹣283kJ/mol,CH4(g)+
O2(g)=CO2(g) 的焓變可根據CH4(g)+2O2(g)=CO2(g)+2H2O(l) H=-890.3kJ/mol和反應H=﹣283kJ/mol,CH4(g)+![]() O2(g)=CO(g)+2H2O(l) H=﹣607.3kJ/mol求出焓變H=﹣283kJ/mol,C正確;
O2(g)=CO(g)+2H2O(l) H=﹣607.3kJ/mol求出焓變H=﹣283kJ/mol,C正確;
D.CO(g)+![]() O2(g)=CO2(g) H=﹣283kJ/mol,該反應放熱,反應物的總能量高于生成物的總能量,所以等物質的量的CO2和CO,CO具有的能量高,D錯誤;
O2(g)=CO2(g) H=﹣283kJ/mol,該反應放熱,反應物的總能量高于生成物的總能量,所以等物質的量的CO2和CO,CO具有的能量高,D錯誤;
故選C。


科目:高中化學 來源: 題型:
【題目】化工生產與人類進步緊密相聯。下列有關說法不正確的是
A. 空氣吹出法提取海水中溴通常使用SO2作還原劑
B. 侯氏制堿法工藝流程中利用了物質溶解度的差異
C. 合成氨采用高溫、高壓和催化劑主要是提高氫氣平衡轉化率
D. 工業用乙烯直接氧化法制環氧乙烷體現綠色化學和原子經濟
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表中實線是元素周期表的部分邊界,其中上邊界并未用實線標出。
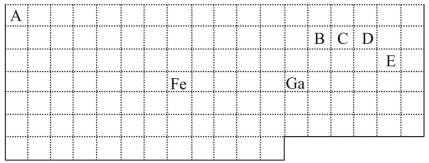
根據信息回答下列問題:
(1)周期表中基態Ga原子的電子排布式為___。
(2)Fe元素位于周期表的___分區;Fe與CO易形成配合物Fe(CO)5,在Fe(CO)5中鐵的化合價為___。
(3)已知:原子數目和電子總數(或價電子總數)相同的微粒互為等電子體,等電子體具有相似的結構特征。與CO分子互為等電子體的分子和離子分別為___和___(填化學式)。在CO、CH3OH中,碳原子采取sp3雜化的分子有___。
(4)根據VSEPR理論預測ED4-離子的空間構型為___。B、C、D、E原子相互化合形成的分子中,所有原子都滿足最外層8電子穩定結構的分子有__(任寫2種化學式)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鑭系為元素周期表中第ⅢB族、原子序數為57~71的元素。
(1)鏑(Dy)的基態原子電子排布式為[Xe]4f106s2,畫出鏑(Dy)原子外圍電子排布圖:___________。
(2)高溫超導材料鑭鋇銅氧化物中含有Cu3+,基態時Cu3+ 的電子排布式為________________。
(3)觀察下面四種鑭系元素的電離能數據,判斷最有可能顯示+3 價的元素是___________(填元素名稱)。幾種鑭系元素的電離能(單位:kJ mol-1)
元素 | I1 | I2 | I3 | I4 |
Yb(鐿) | 604 | 1217 | 4494 | 5014 |
Lu(镥) | 532 | 1390 | 4111 | 4987 |
La(鑭) | 538 | 1067 | 1850 | 5419 |
Ce(鈰) | 527 | 1047 | 1949 | 3547 |
(4)元素鈰(Ce)可以形成配合物(NH4)2[Ce(NO3)6]。
①組成配合物的四種元素,電負性由大到小的順序為________________(用元素符號表示)。
②寫出氮的最簡單氣態氫化物水溶液中存在的氫鍵:__________________(任寫一種)。
③元素Al 也有類似成鍵情況,氣態氯化鋁分子表示為(AlCl3)2,分子中Al 原子雜化方式為_____________,分子中所含化學鍵類型有______________(填字母)。
a.離子鍵 b.極性鍵 C.非極性鍵 d.配位鍵
(5)PrO2(二氧化鐠)的晶體結構與CaF2相似,晶胞中鐠原子位于面心和頂點,則PrO2(二氧化鐠)的晶胞中有________個氧原子;已知晶胞參數為a pm,密度為ρ g· cm-3,NA=_____________ (用含a、ρ的代數式表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是以乙炔(結構簡式為![]() )為主要原料合成聚氯乙烯、聚丙烯腈和氯丁橡膠的轉化關系圖。
)為主要原料合成聚氯乙烯、聚丙烯腈和氯丁橡膠的轉化關系圖。
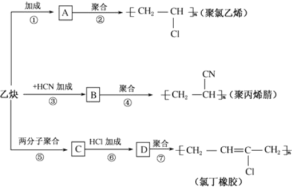
(1)寫出A、B、C、D四種物質的結構簡式:
A:________,B:________,C:________,D:________。
(2)寫出有關反應的化學方程式:
②:____________;
③:_____________;
⑤:___________;
⑦:_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2019年諾貝爾化學獎授予了鋰離子電池開發的三位科學家。一種鋰離子電池的反應式為LixC6+Li1﹣xCoO2![]() 6C+LiCoO2(x<1)其工作原理如圖所示。下列說法不正確的是( )
6C+LiCoO2(x<1)其工作原理如圖所示。下列說法不正確的是( )
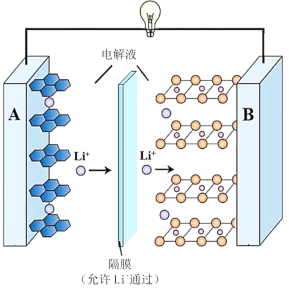
A.放電時A極電極式為:LixC6–xe-=6C+xLi+
B.放電時,若轉移0.3mol電子,石墨電極將減重2.1g
C.充電時,A極接外電源的正極
D.該廢舊電池進行“放電處理”有利于鋰在B極回收
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】孔雀石的主要成分為Cu2(OH)2CO3。某同學設計的從孔雀石中冶煉銅的方案如下(假設孔雀石中雜質不溶于水和稀硫酸):

(1)反應①能觀察到的現象是__________,有關反應的化學方程式為________。
(2)反應②加入的金屬可能是______,有關反應的離子方程式為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在1.0 L恒容密閉容器中放入0.10 mol X,在一定溫度下發生反應:X(g)![]() Y(g)+Z(g) ΔH<0,容器內氣體總壓強p隨反應時間t的變化關系如圖所示。以下分析正確的是 ( )
Y(g)+Z(g) ΔH<0,容器內氣體總壓強p隨反應時間t的變化關系如圖所示。以下分析正確的是 ( )
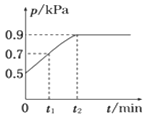
A. 該溫度下此反應的平衡常數K=3.2
B. 從反應開始到t1時的平均反應速率v(X)=0.2/t1 mol·L-1·min-1
C. 欲提高平衡體系中Y的百分含量,可加入一定量的X
D. 其他條件不變,再充入0.1 mol氣體X,平衡正向移動,X的轉化率減少
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學課外小組所做實驗的示意圖如圖所示:圖中“→”表示氣體流向, M是一種純凈而干燥的氣體,Y為另一種氣體,E內有紅棕色氣體產生,實驗所用物質只能由下列物質中選取:Na2CO3、Na2O2、NaCl、Na2O、CaCl2、(NH4)2CO3、堿石灰等固體及蒸餾水。據此實驗,完成下列填空:
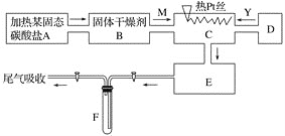
(1)A中所用裝置的主要儀器和藥品是______________________。
(2)B中所選的干燥劑是________,其作用是______________________________。
(3)C中發生的主要反應的化學方程式:________________________________。
(4)制取Y氣體的D裝置所用的主要儀器是__________________________。
制取Y氣體的化學方程式是________________________。
(5)F中發生反應的化學方程式為__________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com