
某校化學小組為探究鐵與濃硫酸反應是否生成SO2,設計了以下裝置進行實驗。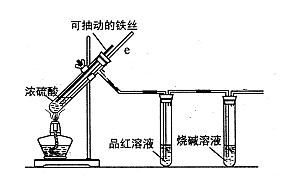
(1)寫出鐵與濃硫酸反應的化學方程式 ;
若在取用濃硫酸的過程中,不慎在皮膚上沾少量濃硫酸,處理的方法是 。
(2)導氣管e有兩個主要作用:一是在反應過程中,因導管插入液面下,可起到“液封”作用阻止SO2氣體逸出而防止污染環境;二是 。
(3)品紅溶液的作用是 。
(4)小組討論后認為:由于常用的鐵絲是鐵碳合金,生成的氣體中還可能含有CO2。寫出生成CO2的化學方程式 。
(1)2Fe + 6H2SO4(濃) 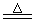 Fe2(SO4)3 + 3SO2↑ + 6H2O (2分)
Fe2(SO4)3 + 3SO2↑ + 6H2O (2分)
立即用大量水沖洗,再涂上3%~5%的NaHCO3溶液 (2分)
(2)停止加熱時,防止倒吸或平衡壓強 (1分)
(3)檢驗是否生成SO2(1分)
(4)C + 2H2SO4 CO2↑+2SO2↑+2H2O(2分)
CO2↑+2SO2↑+2H2O(2分)
解析試題分析: 鐵與濃硫酸在加熱的條件下可反應生成硫酸鐵、二氧化硫和水,濃硫酸具有強氧化性和腐蝕性,故少量的濃硫酸不慎滴在皮膚上應立即用大量水沖洗,再涂上3%~5%的NaHCO3溶液,若是大量的濃硫酸,應先用干布拭擦,再用大量水沖洗,再涂上3%~5%的NaHCO3溶液。導氣管e作用:導管插入液面下,可起到“液封”作用阻止SO2氣體逸出而防止污染環境,停止加熱時,防止倒吸或平衡壓強。二氧化硫可以使品紅溶液褪色,故二氧化硫可以用品紅溶液來檢查產物是否生成二氧化硫。鐵絲是鐵碳合金,含有碳,而濃硫酸具有強氧化性,可以與碳反應生成二氧化碳,二氧化硫和水。
考點:考查濃硫酸與鐵反應的相關知識點。


 全優沖刺100分系列答案
全優沖刺100分系列答案 英才點津系列答案
英才點津系列答案科目:高中化學 來源: 題型:填空題
氫溴酸(HBr)是一種與鹽酸化學性質相似的物質,陽離子相同的溴鹽與氯鹽溶解性也比較相似,現有以下六種物質:Fe、Fe2O3、CO2、Cu(OH)2、CaCO3、Na2SO4,請從中選取物質,寫出能與氫溴酸反應的化學方程式(可不填滿,不反應的寫出倒扣1分,本題扣到0分為止):
(1)
(2)
(3)
(4)
(5)
(6)
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
火電廠排放氣體中含有二氧化硫、氮氧化物等大氣污染物,大氣污染物的研究治理對改善環境具有重要意義。
(1)煤燃燒產生的煙氣(含有氮氧化物、SO2、PM2.5等),直接排放到空氣中,引發的主要環境問題有 (填寫字母編號)
A水體富營養化 B重金屬污染 C霧霾 D酸雨
(2)將含有SO2的廢氣通過裝有石灰石漿液的脫硫裝置可以除去其中的二氧化硫,在廢氣脫硫的過程中,所用的石灰石漿液在進入脫硫裝置前,需通一段時間的二氧化碳,以增加其脫硫效率;脫硫時控制漿液的pH值,此時漿液含有的亞硫酸氫鈣可以被氧氣快速氧化生成硫酸鈣。寫出亞硫酸氫鈣被足量氧氣氧化生成硫酸鈣的化學方程式 。
(3)有人提出了一種利用氯堿工業產品治理含二氧化硫廢氣的方法,工藝流程如下:
A的化學式 ,若生成ag A,理論上可以回收SO2的質量為 g。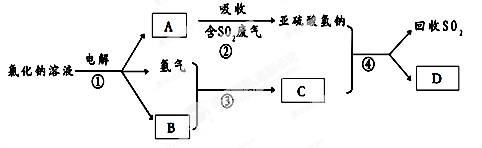
(4)汽車尾氣中含有的氮氧化物(NOx)能形成酸雨,寫出NO2轉化為HNO3的化學方程式 。當尾氣中空氣不足時,NOX在催化轉化器中被還原成N2排出,寫出NO被CO還原的化學方程式 。
(5)工業上常用Na2CO3溶液處理煤燃燒產生的煙氣,寫出SO2、NO與Na2CO3溶液反應生成Na2SO4、N2的離子方程式 。
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
在一只試管中裝入NO2和NO混合氣體a升(常溫常壓,下同。不考慮NO2轉化為N2O4。),倒扣在水槽中,與水充分反應后剩余氣體b升(不含水蒸氣),再通入c 升O2,試管內剛好無氣體剩余。
(1)b的值為 (用只含c的代數式表示)。
(2)填表。
| 表達要求 | 只含b的代數式 | 只含c的代數式 |
| a的取值范圍 | | |
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
在500mL 0.2 mol·L-1的稀硝酸中加入1.92g銅片,讓其充分反應。試求:
(1)產生的氣體在標準狀況下所占的體積為多少?
(2)反應后溶液中H+的物質的量濃度是多少?(溶液體積變化忽略不計)
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
(14分)亞氯酸鈉(NaClO2)是一種重要的含氯消毒劑,主要用于水的消毒以及砂糖、油脂的漂白與殺菌。以下是過氧化氫法生產亞氯酸鈉的工藝流程圖: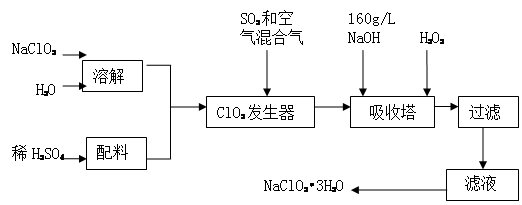
已知:①NaClO2的溶解度隨溫度升高而增大,適當條件下可結晶析出NaClO2?3H2O。
②純ClO2易分解爆炸,一般用稀有氣體或空氣稀釋到10%以下安全。
③160 g/L NaOH溶液是指160 gNaOH固體溶于水所得溶液的體積為1L。
(1) 160 g/L NaOH溶液的物質的量濃度為 。
(2)發生器中鼓入空氣的作用可能是 (選填序號)。
a.將SO2氧化成SO3,增強酸性;
b.稀釋ClO2以防止爆炸;
c.將NaClO3氧化成ClO2
(3)吸收塔內的反應的化學方程式為 。
吸收塔的溫度不能超過20℃,其目的是 。
(4)在堿性溶液中NaClO2比較穩定,所以吸收塔中應維持NaOH稍過量,判斷NaOH是否過量的簡單實驗方法是 。
(5)吸收塔中為防止NaClO2被還原成NaCl,所用還原劑的還原性應適中。除H2O2
外,還可以選擇的還原劑是 (選填序號)。
a.Na2O2 b.Na2S c.FeCl2
(6) 從濾液中得到NaClO2?3H2O粗晶體的實驗操作依次是 (選填序號)。
a.蒸餾 b.蒸發 c.灼燒 d.過濾 e.冷卻結晶
要得到更純的NaClO2?3H2O晶體必須進行的操作是 (填操作名稱)
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
N2在化工生產、農業、醫療、航天航空等領域用途廣泛。現提供以下裝置(連接儀器略去):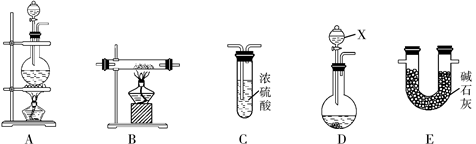
①某化學興趣小組甲同學欲用加熱NaNO2和NH4Cl的濃溶液制得N2,應該選擇的發生裝置是 ,在添加藥品、制取氣體前必須進行的操作是 。
②在加熱條件下,用NH3還原CuO可制得N2,同時獲得銅粉,此反應的化學反應方程式是 。
③乙同學利用②中反應原理制備干燥、純凈的N2,且需要的NH3以生石灰和濃氨水作原料。按氣流從左到右的連接順序是D→E→B→C,其中裝置D中儀器X的名稱是 。裝置C中試劑的作用是 。
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
(22分)黃鐵礦(FeS2)燃燒產生的SO2通過下列工藝過程既能制得H2SO4,又能制得H2。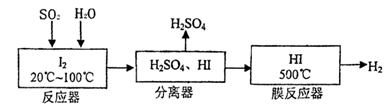
(1)該過程中能循環利用的物質為 。
(2)寫出反應器中發生反應的離子方程式 。
(3)某研究性學習小組欲探究SO2能否與BaCl2溶液反應生成BaSO3沉淀,進行如下實驗。
已知濃硫酸的沸點為338oC,加熱時酒精燈火焰的溫度為400oC~500oC。
①甲同學用裝置I(如下圖)進行實驗,發現BaCl2溶液中出現白色沉淀,且白色沉淀不溶于鹽酸,該實驗結論不能說明SO2能與BaCl2溶液發生反應,請解釋生成該白色沉淀的兩種可能原因(用文字和離子方程式表示):
,
;
②乙同學設計了裝置Ⅱ(夾持裝置和A的加熱裝置略去)進行實驗,發現C中沒有出現白色沉淀。
裝置Ⅱ改進了裝置I的四處不足,請填表說明另外的三處。
| 改進的操作或裝置(注明必要的試劑) | 改進的作用 |
| 使用分液漏斗滴加濃硫酸 | 控制反應速率 |
| | |
| | |
| | |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
實驗探究:探究碳、硅元素的非金屬性的相對強弱
根據要求完成下列各小題
(1)實驗裝置: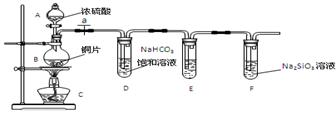
填寫所示儀器名稱A B
(2)實驗步驟:
連接儀器、 、加藥品后,打開a、然后滴入濃硫酸,加熱
(3)問題探究:(已知酸性強弱:亞硫酸 >碳酸)
①銅與濃硫酸反應的化學方程式是 ;裝置E中足量酸性KMnO4溶液的作用是 ;
②能說明碳元素的非金屬性比硅元素非金屬性強的實驗現象是 ;
③依據試管D中的實驗現象,能否證明硫元素的非金屬性強于碳元素的非金屬性 (填“能”或“否”),試管D中發生反應的離子方程式是
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com