
【題目】炭黑是霧霾中的重要顆粒物,研究發現它可以活化氧分子,生成活化氧。活化過程的能量變化模擬計算結果如右圖所示。活化氧可以快速氧化 SO2。下列說法不正確的是
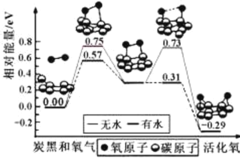
A.每活化一個氧分子放出0.29eV能量
B.水可使氧分子活化反應的活化能降低0.42eV
C.氧分子的活化是O-O的斷裂與C-O鍵的生成過程
D.炭黑顆粒是大氣中SO2轉化為SO3的催化劑
【答案】B
【解析】
A.根據能量變化圖分析,氧氣最終變成活化氧,體系能量降低,則每活化一個氧氣分子放出0.29eV能量,故A正確;
B.反應過程中存在多步反應的活化能,根據能量變化圖分析,整個反應的活化能應是活化能較大的,則沒有水加入的反應活化能E=0.75eV,有水加入反應的活化能E=0.57eV,所以水可以使氧分子活化反應的活化能降低0.75eV-0.57eV=0.18eV,故B錯誤;
C.根據能量變化圖和題意,氧分子活化過程中O-O的斷裂,生成C-O鍵,所以氧分子的活化是O-O的斷裂與C-O鍵的生成過程,故C正確;
D.活化氧可以快速氧化 SO2,而炭黑顆粒可以活化氧分子產生活化氧,所以炭黑顆粒是大氣中SO2轉化為SO3的催化劑,故D正確;
綜上所述,答案為B。


科目:高中化學 來源: 題型:
【題目】金剛烷是一種重要的化工原料,工業上可通過下列途徑制備:

請回答下列問題:
(1)環戊二烯分子中最多有__個原子共平面。
(2)金剛烷的分子式為__,其二氯代物有_種。
(3)已知烯烴能發生如下反應:
 。
。
請寫出下列反應產物的結構簡式:![]()
![]() __。
__。
(4)A是二聚環戊二烯的同分異構體,能使溴的四氯化碳溶液褪色,A經高錳酸鉀酸性溶液加熱氧化可以得到對苯二甲酸提示:苯環上的烷基(—CH3,—CH2R,—CHR2)或烯基側鏈經高錳酸鉀酸性溶液氧化得羧基,寫出A所有可能的結構簡式不考慮立體異構:__。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列表述與示意圖一致的是
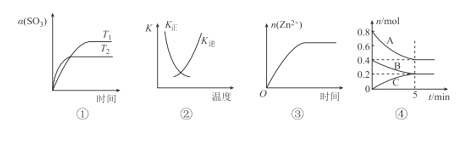
A.圖①表示2SO3(g)=2SO2(g)+O2(g) △H>0,SO3的平衡轉化率隨溫度、時間的變化
B.圖②中曲線表示反應H2(g)+I2(g)=2HI(g) △H<0正、逆反應的平衡常數K隨溫度的變化
C.圖③表示20 mL 0.1 mol/L稀鹽酸與過量鋅粒混合時,n(Zn2+)隨時間的變化
D.圖④反應從開始到平衡的平均反應速率v(B)=0.04molL-1min-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】五氧化二釩用作冶金添加劑,占五氧化二釩總消耗量的 80%以上,其次是用作有機化工的催化劑。為了增加V2O5 的利用率,我們從廢釩催化劑(主要成分V2O5、VOSO4、K2SO4、SiO2 和Fe2O3 等) 中回收 V2O5 的一種生產工藝流程示意圖:
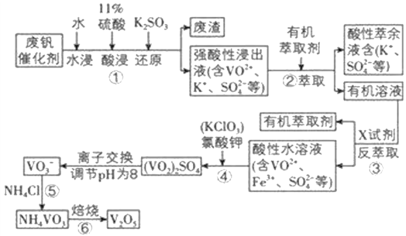
部分含釩物質在水中的溶解性如表所示,回答下列問題:
物質 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
溶解性 | 可溶 | 難溶 | 難溶 | 易溶 |
(1)①中廢渣的主要成分是 __________________________;①中V2O5 發生反應的離子方程式為 ___________________________ 。
(2)②、③中的變化過程可簡化為(下式中的R 表示 VO2+或 Fe3+,HA 表示有機萃取劑的主要成分)R2(SO4)n(水層)+2nHA(有機層) 2RA(有機層)+ nH2SO4(水層)。②中萃取時必須加入適量堿,其原因是 ______________________;實驗室進行萃取操作使用的玻璃儀器為 ______________________。
(3)實驗室用的原料中V2O5 占 6%(原料中的所有釩已換算成 V2O5)。取 100 g 該廢釩催化劑按工業生產的步驟進行實驗,當加入 100 mL 0.1 molL -1 的KClO3 溶液時,溶液中的釩恰好被完全處理,假設以后各步釩沒有損失,則該實驗中釩的回收率是 __________________[M(V2O5)=182 gmol -1]。
(4)25℃時,取樣進行實驗分析,得到釩沉淀率和溶液 pH 之間的關系如表所示:
pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 |
釩沉淀率/% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.6 | 96.4 | 93.1 |
試判斷在實際生產時,⑤中加入 NH4Cl 調節溶液的最佳 pH為____________;若釩沉淀率為 93.1%時不產生 Fe(OH)3 沉淀,則此時溶液中 c(Fe3+)≤____________ (已知:25℃時Ksp[Fe(OH)3]=2.6×10 -39)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】“中和滴定”原理在實際生產生活中應用廣泛。用I2O5可定量測定CO的含量,該反應原理為5CO+I2O5![]() 5CO2+I2。其實驗步驟如下:
5CO2+I2。其實驗步驟如下:
①取250 mL(標準狀況)含有CO的某氣體樣品,通過盛有足量I2O5的干燥管,在170 ℃下充分反應;
②用水-乙醇混合溶液充分溶解產物I2,配制100 mL溶液;
③量取步驟②中溶液25.00 mL于錐形瓶中,然后用0.01 mol·L-1的Na2S2O3標準溶液滴定。
(1)步驟②中配制100 mL待測溶液需要用到的玻璃儀器的名稱是燒杯、量筒、玻璃棒、膠頭滴管和____________________。
(2)Na2S2O3標準液應裝在__________(填字母)中。

(3)指示劑應選用__________,判斷達到滴定終點的現象是____________。(已知:氣體樣品中其他成分不與I2O5反應:2Na2S2O3+I2=2NaI+Na2S4O6)。
(4)下列操作會造成所測CO的體積分數偏大的是________(填字母)。
a.滴定終點俯視讀數
b.錐形瓶用待測溶液潤洗
c.滴定前有氣泡,滴定后沒有氣泡
d.配制100 mL待測溶液時,有少量濺出
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一定溫度下,將氣體X和氣體Y 各0.16mol 充入 10L 恒容密閉容器中,恒容器閉容器中,發生反應X(g)+Y(g) ![]() 2Z(g) △H<0,一段時間后達到平衡,反應過程中測定的數據如表,下列說法正確的是
2Z(g) △H<0,一段時間后達到平衡,反應過程中測定的數據如表,下列說法正確的是
t/min | 2 | 4 | 7 | 9 |
n(Y)mol | 0.12 | 0.11. | 0.10 | 0.10 |
A.反應前 2min 的平均速率 v(Z)=2.0×10-3mol·L-1min-1
B.其他條件不變,向平衡體系中再充入0.16mol 氣體 X,與原平衡相比,達到新平衡時,氣體 Y 的轉化率增大,X 的體積分數增大,Z 的體積分數減少
C.其他條件不變,降低溫度,反應達到新平衡前 v (逆)>v(正)
D.保持其他條件不變,起始時向溶液中充入0.32mol氣體X 和0.32mol 氣體 Y,到達平衡時,n(Z)<0.24mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗裝置能達到實驗目的的是( )
|
|
|
|
A.測定一定時間內生成 H2的反應速率 | B.可以進行中和熱的測定實驗 | C.比較溫度對化學反應速率的影響 | D.比較Cu2+、Fe3+對 H2O2分解速率的影響 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硒(Se)是第四周期第ⅥA族元素,是人體內不可或缺的微量元素,H2Se是制備新型光伏太陽能電池、半導體材料和金屬硒化物的重要原料。
(1)已知:①2H2Se(g)+O2(g)![]() 2Se(s)+2H2O(l) ΔH1=akJ·mol-1
2Se(s)+2H2O(l) ΔH1=akJ·mol-1
②2H2(g)+O2(g)![]() 2H2O(l) ΔH2=bkJ·mol-1
2H2O(l) ΔH2=bkJ·mol-1
反應H2(g)+Se(s)![]() H2Se(g)的ΔH3=__kJ·mol-1(用含a、b的代數式表示)。
H2Se(g)的ΔH3=__kJ·mol-1(用含a、b的代數式表示)。
(2)T℃時,向一恒容密閉容器中加入3molH2和1molSe,發生反應H2(g)+Se(s)![]() H2Se(g)。
H2Se(g)。
①下列情況可判斷反應達到平衡狀態的是__(填字母代號)。
a.氣體的密度不變 b.v(H2)=v(H2Se)
c.氣體的壓強不變 d.氣體的平均摩爾質量不變
②當反應達到平衡后,將平衡混合氣體通入氣體液化分離器使H2Se氣體轉化為H2Se液體,并將分離出的H2再次通入發生反應的密閉容器中繼續與Se反應時,Se的轉化率會提高。請用化學平衡理論解釋:_。
③以5小時內得到的H2Se為產量指標,且溫度、壓強對H2Se產率的影響如圖1、圖2所示:
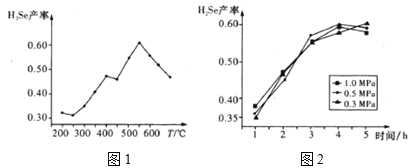
則制備H2Se的最佳溫度和壓強為__。
(3)已知常溫下H2Se的電離平衡常數K1=1.3×10-4、K2=5.0×10-11,則NaHSe溶液呈__(填“酸性”或“堿性”),請通過計算數據說明__。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】碳鋼廣泛應用在石油化工設備管道等領域,隨著深層石油天然氣的開采,石油和天然氣中含有的CO2及水引起的腐蝕問題(俗稱二氧化碳腐蝕)引起了廣泛關注。深井中二氧化碳腐蝕的主要過程如下所示:
負極:![]() (主要)
(主要)
正極:![]() (主要)
(主要)
下列說法不正確的是
A.鋼鐵在CO2水溶液中的腐蝕總反應可表示為![]()
B.深井中二氧化碳對碳鋼的腐蝕主要為化學腐蝕
C.碳鋼管道在深井中的腐蝕與油氣層中鹽份含量有關,鹽份含量高腐蝕速率會加快
D.腐蝕過程表明含有CO2的溶液其腐蝕性比相同pH值的HCl溶液腐蝕性更強
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com