
K、Ki、KW分別表示化學平衡常數、電離常數和水的離子積,下列判斷正確的是( )
| A.在500 ℃、20 MPa、5 L的密閉容器中進行合成氨的反應,使用催化劑后K值增大 |
| B.室溫下K(HCN)<K(CH3COOH),說明CH3COOH的電離度一定比HCN大 |
| C.25 ℃時,pH 均為4的鹽酸和NH4I(aq)中KW不相等 |
D.2SO2+O2 2SO3達平衡后,改變某一條件K值不變,SO2的轉化率可能增大、減小或不變 2SO3達平衡后,改變某一條件K值不變,SO2的轉化率可能增大、減小或不變 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:單選題
有A、B、C三種氣體在一個固定容積的密閉容器中發生反應,體系中各物質濃度隨時間變化的曲線如圖所示。下列說法不正確的是 ( )
A.該反應的化學方程式為
B.若將初始投放的物質濃度增至原來的2倍,則反應物的轉化率增 大,平衡常數不變
C.若第4 min時降低溫度,到7 min時達到了新的平衡,則此反應的△H<0
D.反應在前3 min的平均反應速率v(A)="0." 31 mol
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
利用反應:2NO(g)+2CO(g) 2CO2(g)+N2(g) ΔH ="+746.8" kJ·mol-1,可凈化汽車尾氣,如果要同時提高該反應的速率和NO的轉化率,采取的措施是 ( )
2CO2(g)+N2(g) ΔH ="+746.8" kJ·mol-1,可凈化汽車尾氣,如果要同時提高該反應的速率和NO的轉化率,采取的措施是 ( )
| A.降低溫度 |
| B.增大壓強同時加催化劑 |
| C.升高溫度同時充入N2 |
| D.及時將CO2和N2從反應體系中移走 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在某恒容的密閉容器中,可逆反應A(g)+B(g) xC(g)有如圖所示的關系曲線,下列說法正確的是( )
xC(g)有如圖所示的關系曲線,下列說法正確的是( )
| A.溫度:T1>T2 | B.壓強:p1>p2 |
| C.正反應是吸熱反應 | D.x的值是2 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
為了變廢為寶,控制溫室效應,工業上可用CO2來生產甲醇。一定條件下發生如下反應:CO2(g)+3H2(g)  CH3OH(g)+H2O(g)。如圖表示該反應進行過程中能量(單位為kJ·mol-1)的變化。在體積為1 L的恒容密閉容器中,充入1 mol CO2和3 mol H2,下列措施中不能使c(CH3OH)增大的是 ( )。
CH3OH(g)+H2O(g)。如圖表示該反應進行過程中能量(單位為kJ·mol-1)的變化。在體積為1 L的恒容密閉容器中,充入1 mol CO2和3 mol H2,下列措施中不能使c(CH3OH)增大的是 ( )。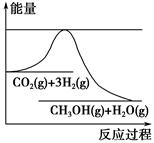
| A.降低溫度 |
| B.充入He(g),使體系壓強增大 |
| C.將H2O(g)從體系中分離出來 |
| D.再充入1 mol CO2和3 mol H2 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在容積為2 L的密閉容器中進行反應:CO(g)+2H2(g) CH3OH(g),其他條件不變,在300 ℃和500 ℃時,甲醇物質的量n(CH3OH)反應時間t的變化曲線如圖所示,下列說法正確的是( )
CH3OH(g),其他條件不變,在300 ℃和500 ℃時,甲醇物質的量n(CH3OH)反應時間t的變化曲線如圖所示,下列說法正確的是( )
| A.該反應的ΔH>0 |
B.其他條件不變,升高溫度反應的平衡常數增大 |
C.300 ℃時,0~t1 min內 CH3OH的平均生成速率為 mol·L-1·min-1 mol·L-1·min-1 |
D.A點的反應體系從300 ℃升高到500 ℃,達到平衡時 減小 減小 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
碘單質難溶于水卻易溶于KI溶液。碘水中加入KI溶液發生反應:I2(aq)+I-(aq) I3—(aq),該反應的平衡常數與溫度的關系如圖,下列說法不正確的是( )
I3—(aq),該反應的平衡常數與溫度的關系如圖,下列說法不正確的是( )
| A.上述正反應為放熱反應 |
| B.上述體系中加入苯,平衡不移動 |
| C.可運用該反應原理除去硫粉中少量的碘單質 |
| D.實驗室配制碘水時,為增大碘單質的溶解度可加入適量KI溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
向一容積為1 L的密閉容器中加入一定量的X、Y,發生反應aX(g)+2Y(s) bZ(g) ΔH<0。如圖是容器中X、Z的物質的量濃度隨時間變化的曲線。
bZ(g) ΔH<0。如圖是容器中X、Z的物質的量濃度隨時間變化的曲線。
根據以上信息,下列說法正確的是 ( )。
| A.用X表示0~10 min內該反應的平均速率為v(X)=0.045 mol·L-1·min-1 |
| B.根據上圖可求得化學方程式中a∶b=1∶3 |
| C.推測在第7 min時曲線變化的原因可能是升溫 |
| D.推測在第13 min時曲線變化的原因可能是降溫 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com