
【題目】在1 L恒容密閉容器中充入X(g)和Y(g),發生反應X(g)+Y(g)![]() M(g)+N(g),所得實驗數據如下表:
M(g)+N(g),所得實驗數據如下表:
實驗編號 | 溫度/℃ | 起始時物質的量/mol | 平衡時物質的量/mol | |
n(X) | n(Y) | n(M) | ||
① | 700 | 0.10 | 0.10 | 0.09 |
② | 800 | 0.20 | 0.20 | 0.10 |
③ | 800 | 0.20 | 0. 30 | a |
④ | 900 | 0.10 | 0.15 | b |
下列說法錯誤的是
A.實驗①中,若5 min時測得n(M) =0.05 mol,則0至5 min時間內,用N表示的平均反應速率v(N) =
0.01 mol/( L·min)
B.實驗②中,該反應的平衡常數K=1.0
C.實驗③中,達到平衡時,X的轉化率為60%
D.實驗④中,達到平衡時,b>0.06
【答案】D
【解析】本題考查了化學反應速率、化學平衡常數、化學平衡的影響因素的相關知識。v(N)=v(M) = =0.01mol/(Lmin),故A正確,不選;根據三段式求解可得:
=0.01mol/(Lmin),故A正確,不選;根據三段式求解可得:

實驗②中,該反應的平衡常數K=![]() =1.0,故B正確,不選;
=1.0,故B正確,不選;

實驗②和③的溫度相同,則平衡常數也相同,所以該反應的平衡常數K=![]() =1.0,解得a=0.12,實驗③中,X的轉化率為:
=1.0,解得a=0.12,實驗③中,X的轉化率為:![]() ×100%=60%,故C正確,不選;
×100%=60%,故C正確,不選;

則700℃時,該反應的平衡常數K=![]() =81,800℃時,該反應的平衡常數K=1.0,溫度升高平衡常數減小,所以該反應為放熱反應,假如實驗④為800℃時,則:
=81,800℃時,該反應的平衡常數K=1.0,溫度升高平衡常數減小,所以該反應為放熱反應,假如實驗④為800℃時,則:

則K=![]() =1.0,解得b=0.06,溫度升高為900℃時,則平衡逆向移動,則M的物質的量小于0.06 mol,故D錯,選D。
=1.0,解得b=0.06,溫度升高為900℃時,則平衡逆向移動,則M的物質的量小于0.06 mol,故D錯,選D。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】A(C2H4)是基本的有機化工原料。用A和常見的有機物可合成一種醚類香料和一種縮醛類香料,具體合成路線如圖所示(部分反應條件略去):

已知:

回答下列問題:
(1)B的分子式是___________,C中含有的官能團名稱是 ____________。
(2)若D為單取代芳香族化合物且能與金屬鈉反應;每個D分子中只含有1個氧原子,D中氧元素的質量分數約為13.1%,則D的結構簡式為___________,⑥的反應類型是________________。
(3)據報道,反應⑦在微波輻射下,以NaHSO4·H2O為催化劑進行,請寫出此反應的化學方程式:____________________________________。
(4)請寫出滿足下列條件的苯乙醛的所有同分異構體的結構簡式:___________________。
i .含有苯環和![]() 結構
結構
ii.核磁共振氫譜有4組峰,且峰面積之比為3∶2∶2∶1
(5)若化合物E為苯甲醚的同系物,且相對分子質量比苯甲醚大14,則能使FeCl3溶液顯色的E的所有同分異構體共有(不考慮立體異構)________________種。
(6)參照 的合成路線,寫出由2-氯丙烷和必要的無機試劑制備
的合成路線,寫出由2-氯丙烷和必要的無機試劑制備 的合成流程圖:_______________________________________
的合成流程圖:_______________________________________
合成流程圖示例如下:CH2 = CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH
CH3CH2OH
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于晶體與非晶體的說法正確的是( )
A.晶體與非晶體的本質區別在于是否有固定的熔沸點
B.晶體有自范性的原因是粒子在微觀空間呈周期有序性排列
C.固體食鹽、水晶、塑料、膽礬、玻璃均屬于晶體
D.區別晶體與非晶體的最科學可靠的方法是檢測其是否具有各向異性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】煤的氣化主要生成CO、H2等,其中CO、H2是用途相當廣泛的化工基礎原料。但煤的氣化獲得的化工原料氣中常含有少量羰基硫(COS),能引起催化劑中毒、大氣污染等。
(1)COS的電子式為_____________________。
(2)下圖是1molCO和lmolNO2反應生成兩種氣態氧化物過程屮能量變化示意圖。已知14克CO參加反應時轉移電子數為NA。寫出該反應的熱化學方程式_______________________。
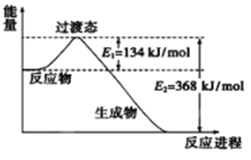
(3)在某一恒溫、恒容的密閉容器中發生以下反應:Ni(S)+4CO(g) ![]() Ni(CO)4(g)。下列說法正確的是__________。
Ni(CO)4(g)。下列說法正確的是__________。
A.該反應的反應熱△H<0
B.增加Ni的量可提高CO的轉化率,Ni的轉化率降低
C.反應達到平衡后,充入CO再次達到平衡時,CO的濃度增大
D.當v正[Ni(CO)4]=4v逆(CO)時或容器中混合氣體密度不變時,都可說明反應已達化學平衝狀態
(4)工業上采用CO與H2反應合成甲醇,反應如下CO(g)+2H2(g)![]() CH3OH(g)。在T℃時,將2molCO和amolH2充入2L的恒容密閉容器中充分反應,l0min后反應達到平衡。已知v(CH3OH)=0.05molL-1min-1,且CO和H2的轉化率相等。
CH3OH(g)。在T℃時,將2molCO和amolH2充入2L的恒容密閉容器中充分反應,l0min后反應達到平衡。已知v(CH3OH)=0.05molL-1min-1,且CO和H2的轉化率相等。
①H2的轉化率為_________________,反應未開始時的容器內氣體壓強P1與反應達平衡時壓強P2的比值為__________________。
②以甲醇燃料電池為電源,熔融鹽電解法制取硅烷原理如圖。陽極的電極反應式為_______________。
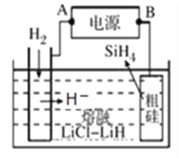
(5)甲醇可制備二甲醚:2CH3OH(g)![]() CH3OCH3(g)+ H2O(g),K =1 (300℃測定)。
CH3OCH3(g)+ H2O(g),K =1 (300℃測定)。
①在300℃時,測得n(CH3OCH3)=2n(CH3OH),此時反應的v正__________v逆(填“〉”、“〈”或“=”〉,你的分析理由是___________________。
②二甲醚催化重整制氫的反應過程,主要包括以下幾個反應(以下數據為25℃、1.01×l05Pa測定):
Ⅰ:CH3OCH3(g)+H2O(1)![]() 2CH3OH(1)△H>0
2CH3OH(1)△H>0
Ⅱ:CH3OH(1)+H2O(1)![]() CO2(g)+3H2(g)△H>0
CO2(g)+3H2(g)△H>0
Ⅲ:CO(g)+H2O(1)![]() CO2(g)+H2(g)△H<0
CO2(g)+H2(g)△H<0
Ⅳ:CH3OH(l)![]() CO(g)-2H2(g)△H>0
CO(g)-2H2(g)△H>0
工業生產中測得不同溫度下各組分體積分數及二甲醚轉化率的關系如下圖所示,
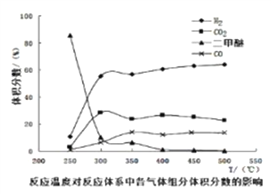

你認為反應控制的最佳溫度應為__________。
A. 300350℃ B. 35040℃ C. 400450℃ D. 450500℃
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在如圖所示的實驗裝置中,當A、B、C、分別為以下不同組合的物質時,回答有關問題:
(1).當A為醋酸、B為石灰石、C為苯酚鈉溶液時,小試管中的現象是__________________________,小試管中發生反應的化學方程式是___________________________________________。整個實驗可得出的結論是_______________________。
(2).當A為飽和食鹽水、B為電石、C為酸性KMnO4溶液時,小試管中的現象是______________;A和B反應的方程式是____________________________。
(3).裝置中D部分的作用是____________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于有機物結構、性質的說法正確的是( )
A. 石油的分餾、裂化和煤的氣化、液化、干餾都是化學變化
B. 乙酸乙酯和油脂互為同系物
C. 甲烷、苯、乙醇、乙酸和乙酸乙酯在一定條件下都能發生取代反應
D. 蔗糖、油脂、蛋白質都能發生水解反應,都屬于天然有機高分子化合物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】CO2經催化加氫可合成乙烯:2CO2(g)+6H2(g)![]() C2H4(g)+4H2O(g)。0.1 MPa時,按n(CO2)∶n(H2)=l∶3投料,測得不同溫度下平衡時體系中各物質濃度的關系如圖。下列敘述不正確的是
C2H4(g)+4H2O(g)。0.1 MPa時,按n(CO2)∶n(H2)=l∶3投料,測得不同溫度下平衡時體系中各物質濃度的關系如圖。下列敘述不正確的是

A.該反應的△H<0
B.曲線b代表H2O
C.N點和M點所處狀態的c(H2)不一樣
D.其他條件不變,T1℃、0.2 MPa下反應達平衡時c(H2)比M點大
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com