
【題目】山西老陳醋是中國四大名醋之一,已有 3000 余年的歷史,素有“天下第一醋”的盛譽。
(1)山西人喜歡吃面食,面食為人體提供的營養物質主要是_______________,它對人體所起的作用是_________________。面食本身偏堿性,吃醋能增加胃液酸度,有助于食物的消化和吸收。
(2)炒菜時,加一點酒和醋能使菜味香可口,原因是(用方程式表示) ___________________,生成的有香味的物質是__________________(填名稱)。
(3)碳酸氫鈉是一種治療胃酸過多的藥物,若病人服用此藥物的同時吃醋,會使藥效大大降低,有關反應的化學方程式是_______________________。
科目:高中化學 來源: 題型:
【題目】海水提鎂的主要流程如下,下列說法正確的是

①試劑M是鹽酸 ②流程中的反應全部都是非氧化還原反應
③操作b只是過濾 ④用海水曬鹽后的飽和溶液加石灰乳制Mg(OH)2
⑤采用電解法冶煉鎂是因為鎂很活潑
A. ①②③④⑤ B. ②③ C. ④⑤ D. ①④⑤
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對塑料的敘述不正確的是 ( )
A.熱塑性塑料具有長鏈狀的線型結構
B.熱固性塑料在形成初期是長鏈狀的
C.熱固性塑料鏈與鏈之間會形成共價鍵,產生一些交聯
D.熱固性塑料在高溫時共價鍵也不斷裂
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用化學原理可以對工廠排放的廢水、廢渣等進行有效檢測與合理處理。某工廠對制革工業污泥中Cr(Ⅲ)的處理工藝流程如下圖所示:
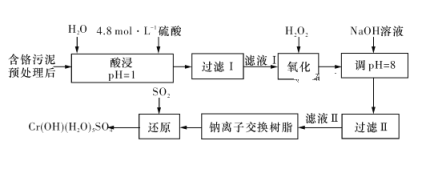
其中硫酸浸取液中的金屬離子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
(1)實驗室用18.4 mol·L-1的濃硫酸配制240 mL 4.8 mol·L-1的硫酸溶液,需量取濃硫酸__________mL;配制時所用玻璃儀器除量筒、燒杯、膠頭滴管和玻璃棒外,還需____________。
(2)“酸浸”時,為了提高浸取率可采取的措施有__________________。
(3)H2O2的作用是將“濾液Ⅰ”中的Cr3+轉化為Cr2O72-,寫出此反應的離子方程式:___________________。
(4)常溫下,部分陽離子以氫氧化物形式沉淀時溶液的pH如下表所示:
陽離子 | Fe3+ | Mg2+ | Al3+ | Cr3+ |
開始沉淀時的pH | 2.7 | — | — | — |
沉淀完全時的pH | 3.7 | 11.1 | 5.4(>8溶解) | 9(>9溶解) |
加入NaOH溶液使溶液呈堿性,Cr2O72-轉化為CrO42-。過濾后“濾液Ⅱ”中的陽離子主要有Na+、Ca2+、Mg2+,但溶液的pH不能超過8,其理由是__________________。
(5)鈉離子交換樹脂的反應原理為Mn++nNaR===MRn+nNa+,利用鈉離子交換樹脂除去“濾液Ⅱ”中的金屬陽離子是________(填離子符號)。
(6)寫出上述流程中用SO2進行還原時發生反應的化學方程式:___________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】H2 和 Cl2 反應的微觀過程可用右圖表示,下列有關說法正確的是
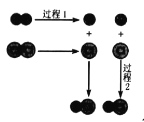
A. 過程 1 釋放能量B. 過程 2 吸收能量
C. 該反應為吸熱反應D. 反應物總能量高于生成物總能量
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(一) 某實驗小組的同學們用下列裝置進行乙醇催化氧化的實驗.(部分夾持儀器已略去)已知:乙醇的沸點為 78℃,易溶于水;乙醛的沸點為 20.8℃,易溶于水。
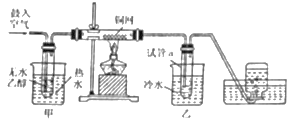
(1) 乙醇催化氧化的化學方程是_________。
(2)裝置甲中熱水的主要作用是_________。
(3)裝置乙中冷水的主要作用是_________,其溫度要求是_________,為達到該溫度,可進行的操作是_________。
(4)實驗開始前,加熱銅網,觀察到的現象是_________,該反應的化學方程式是_________;鼓入空氣和乙醇蒸氣后,銅網處觀察到的現象是_________,此反應中,銅的作用是_________。
(5) 在不斷鼓入空氣的情況下,熄滅酒精燈,反應仍能繼續進行,說明該反應_________(填“吸熱”或“放熱”);集氣瓶中收集到的氣體的主要成分是_________。
(6)實驗結束后,取出裝置乙中的試管,打開橡膠塞,能聞到_________。
(二) 化學興趣小組的同學們設計了如下裝置驗證乙醇催化氧化的產物(加熱儀器、夾持裝置已略
去)。
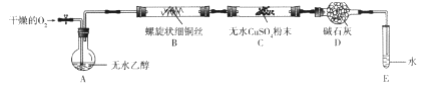
已知: 乙醇的沸點為 78℃, 易溶于水; 乙醛的沸點為 20.8℃, 易溶于水。
(1)乙醇催化氧化的化學方程式是___________。
(2)實驗時上述裝置中需要加熱的是__________(填字母,下同),其中應該先加熱的是_______, 為使裝置A中的乙醇成為蒸氣, 最簡單的加熱方法是_________。
(3)實驗室制取氧氣的化學方程式是___________。
(4)實驗開始后,裝置B中能觀察到的現象是___________;裝置C中能觀察到的現象是__________, 由此得出的結論是_____________。
(5)裝置 E 的作用是________, 能初步判定反應后有乙醛生成的依據是_____________。
(6)裝置 D中的藥品是__________, 其作用是_________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在元素周期表中位于金屬和非金屬元素交界處最容易找到的材料是( )
A.半導體材料B.制催化劑的材料
C.制農藥的材料D.耐高溫、耐腐蝕的合金材料
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是
A. 同溫同壓下甲烷和氧氣的密度之比為2∶1
B. 1 g甲烷和1 g氧氣的原子數之比為5∶1
C. 等物質的量的甲烷和氧氣的質量之比為2∶1
D. 在標準狀況下等質量的甲烷和氧氣的體積之比為1∶2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將質量為1.15 g鈉用刺了孔的鋁箔包裹后放入水中,共收集到1.232 L(標準狀況)氣體。請回答下列問題:
(1)1.15 g鈉與水反應,理論上生成氣體的體積(標準狀況)為__________ L 。
(2)Al和NaOH溶液反應也能生成H2,寫出相應的化學方程式:_____________;
(3)若反應后溶液的體積為100 mL,則溶液中NaOH的物質的量濃度為多少?(寫出計算過程)_______。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com