
小敏對實驗室用石灰石和稀鹽酸制取二氧化碳后的廢液,進行溶質成分鑒定。取廢液上層清液50克,逐滴加入質量分數為26.5%的碳酸鈉溶液,出現氣泡,滴加至10克開始出現白色沉淀。繼續滴加至沉淀不再產生,過濾,測得沉淀的質量為5克,并繪制了圖像。
1)滴加的溶液中溶質屬于 (選填“鹽”或“堿”)。
2)10克碳酸鈉溶液中含有的溶質質量是 克。
3)圖像中的a點數值是 。
4)廢液中含有的溶質是 。 (寫化學式)。
5)通過計算說明,圖像橫坐標中的b點表示的溶液的質量是多少克?
1)鹽 2)2.65 3)1.1 4)HCl、CaCl2 (每空一分) 5)30g
解析試題分析:1)滴加的碳酸鈉屬于鹽類。
2)10g碳酸鈉溶液中含溶質的質量為:10g╳26.5%=2.65g
3)圖中a點表示生成氣體的最大值。可利用二氧化碳與碳酸鈉在反應中的質量關系進行求解。解題過程為:
解:設生成二氧化碳氣體的質量為x
2HCl+Na2CO3= 2NaCl+H2O+CO2↑
106 44
2.65g x
106:44=2.65g:x
x=1.1g
所以a點的數值為1.1
4)反應生成的氣體是碳酸鈉與原來過量的稀鹽酸反應生成的二氧化碳。當不再生成氣體時,再加入碳酸鈉生成白色沉淀,是因為原溶液中的氯化鈣與碳酸鈉反應的原因。所以可說明原溶液中含有稀鹽酸(HCl)和氯化鈣(CaCl2)。
5)b點是生成沉淀的質量為5g時,所加入的碳酸鈉溶液的質量。其質量為和稀鹽酸反應的碳酸鈉溶液(10g)與和氯化鈣反應的碳酸鈉溶液的質量的和。
未知:和氯化鈣反應的碳酸鈉溶液的質量 已知:碳酸鈣沉淀的質量為5g。
解題思路:可利用二者在化學方程式中的質量關系進行求解。
解:設與氯化鈣反應的碳酸鈉溶液中溶質質量為x,
CaCl2+Na2C03= 2NaCl+CaC03↓
106 100
x 5g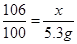
x=5.3g
溶液質量是5.3g÷26.5%=20g
b點質量應標20g+10g=30g
答:b點表示的溶液的質量是30g
考點:根據化學方程式的計算


 名校課堂系列答案
名校課堂系列答案科目:初中化學 來源: 題型:計算題
某同學為了檢驗家里購買的硫酸銨化肥是否合格,他稱取27.5 g化肥樣品與足量濃燒堿溶液加熱,產生的氨氣用100.0g廢硫酸吸收。測得吸收氨氣的溶液總質量m與反應時間t的變化如下圖所示。所涉及的反應為: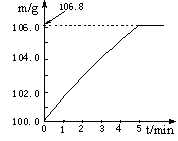
(NH4)2SO4+2NaOH Na2SO4+2H2O+2NH3↑; 2NH3+H2SO4=(NH4)2SO4。
Na2SO4+2H2O+2NH3↑; 2NH3+H2SO4=(NH4)2SO4。
請計算:
(1)完全反應后產生氨氣 g。
(2)該化肥的含氮量為 (精確到0.1%),則這種化肥屬于 (填:“合格”或“不合格”。合格硫酸銨含氮量為20%以上)產品。
(3)請計算廢硫酸中硫酸的質量分數(寫出計算過程)。
(4)若實驗過程中氨氣被完全吸收,但該實驗測得硫酸銨化肥的含氮量高于實際值,其原因是 。
查看答案和解析>>
科目:初中化學 來源: 題型:計算題
“輕鈣”是一種顆粒極細、純度很高的碳酸鈣粉末,有廣泛的用途,如用來制作鈣片、鈣鹽等。我市某輕鈣廠用當地豐富的石灰石,通過如下流程制“輕鈣”:
(1)碳酸鈣中鈣元素的質量分數是____%,食鹽中添加碳酸鈣有助于防止人體缺鈣引起的_______________________(填 “骨骼疏松癥”或“貧血病”)。
(2)石灰石經高溫轉化為A和B,該反應屬于_____________(填基本反應類型)。
(3)沉淀池中得到的塊狀殘渣可能含有未燒透的石灰石。技術人員用鹽酸進行檢驗,觀察到 ,證明殘渣中含有石灰石。
(4)工廠技術人員提出,利用碳酸鈉代替二氧化碳與氫氧化鈣反應,在生成碳酸鈣的同時還可得到氫氧化鈉。請通過計算求:利用這種方法生產50t碳酸鈣時,能得到氫氧化鈉的質量是多少?
查看答案和解析>>
科目:初中化學 來源: 題型:計算題
相同質量的M、N兩種活潑金屬,分別與足量的稀鹽酸在室溫下發生反應(M、N在生成物中的化合價均為+2價),生成H2的質量m和反應時間t的關系如圖所示。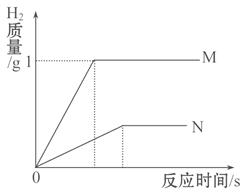
(1)金屬活動性順序是M比N________(填“強”或“弱”);相對原子質量是M比N的________(填“大”或“小”)。
(2)M與稀鹽酸反應結束后,消耗稀鹽酸中溶質的質量為________g。
查看答案和解析>>
科目:初中化學 來源: 題型:計算題
某同學為了檢驗家里購買的硫酸銨化肥是否合格,稱取了27.5 g化肥樣品與足量濃燒堿溶液一起加熱,產生的氨氣用足量的100.0 g廢硫酸吸收,測得吸收氨氣后的溶液總質量為106.8 g,已知合格硫酸銨化肥中含氮量不低于20%。所涉及的反應為:(NH4)2SO4+2NaOH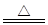 Na2SO4+2NH3↑+2H2O,
Na2SO4+2NH3↑+2H2O,
2NH3+H2SO4=(NH4)2SO4。試計算:
(1)化肥樣品完全反應后產生氨氣_________g。
(2)該化肥的含氮量為____________(精確到0.1%),屬于_____________(填“合格”或“不合格”)產品。
查看答案和解析>>
科目:初中化學 來源: 題型:計算題
向碳酸鈉和氯化鈉的混合物15.6 g中加入100 g稀鹽酸,恰好完全反應后,得到111.2 g溶液。試計算:
(1)產生二氧化碳多少克?
(2)所得溶液中溶質的質量分數是多少?
查看答案和解析>>
科目:初中化學 來源: 題型:計算題
某興趣小組為探究“氧化鐵和銅粉”混合物中銅的質量分數,稱取一定質量的混合物,按照下圖實驗裝置進行實驗: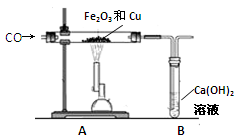
(1)實驗時要“先通一氧化碳氣體,后加熱” 的目的是 。
(2)裝置A中發生反應的方程式為 。
(3)實驗裝置B中的現象是 ,發生反應的化學方程式為 。
(4)該裝置的設計有一明顯不當之處,你的改進方案是 。
[定量分析]
該興趣小組按照科學的方案完成實驗后,對充分反應后的管內固體X進行如下后續實驗探究: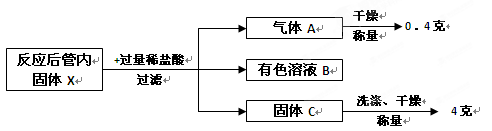
回答下列問題:
(1)寫出固體X與稀鹽酸反應的方程式: 。
(2)有色溶液B中含有的溶質: (填化學式)。
(3)根據以上實驗流程,計算原混合物“氧化鐵和銅粉”中銅的質量分數為 。
查看答案和解析>>
科目:初中化學 來源: 題型:計算題
一化學小組為了測定某銅礦中堿式碳酸銅[Cu2(OH)2CO3]的質量分數.稱取該銅礦樣品30g于燒杯中,逐滴滴入質量分數為10%的稀鹽酸至剛好完全反應,共用去稀鹽酸146g.(假設銅礦中的雜質不與稀鹽酸反應,也不溶于水)
試求:
(1)稀鹽酸中HCl的質量是多少克?
(2)銅礦中堿式碳酸銅的質量是多少克?其質量分數是多少?
(3)反應后所得氯化銅溶液中溶質的質量分數是多少?
(反應的化學方程式為:Cu2(OH)2CO3+4HCl═2CuCl2+CO2↑+3H2O.反應中各物質的相對分子質量:Cu2(OH)2CO3~222
HCl~36.5 CuCl2~135 CO2~44 H2O~18)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com