
 梧州市某中學化學興趣小組的同學到超市購買錫紙用于燒烤,同學們看見商品標簽上標明錫紙的材質為“鋁箔”.
梧州市某中學化學興趣小組的同學到超市購買錫紙用于燒烤,同學們看見商品標簽上標明錫紙的材質為“鋁箔”.| 實驗一:4mL 8% 的CuSO4溶液 | 實驗二:4mL 8% 的CuCl2溶液 | |
| 實驗現象 | 短時間內無變化,一段時間后鋁片上才出現少量紅色的銅. | 鋁片上迅速有紅色的銅出現. |
分析 根據金屬的性質、檢查裝置氣密性的方法、鋁易被氧氣氧化、金屬與鹽溶液反應的特點以及化學方程式的書寫進行分析解答即可.
解答 解:【提出問題】由于錫和鋁都能與鹽酸反應生成氫氣,故不能用加鹽酸的方法鑒別錫和鋁;利用熔點的不同可以采用加熱的方法鑒別,故填:錫和鋁都能與鹽酸反應生成氫氣;加熱;
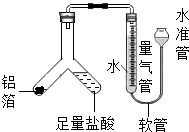
【探究活動一】(1)要檢查該裝置的氣密性,可以從水準管一端注入水,待水準管和量氣管出現較大高度差為止,靜止幾分鐘,兩側高度差不縮小,證明裝置氣密性好,故填:從水準管一端注入水,待水準管和量氣管出現較大高度差為止,靜止幾分鐘,兩側高度差不縮小,證明裝置氣密性好;
(2)產生的氫氣體積為100mL,即0.1L,氫氣的密度為0.09g/L,故氫氣的質量為:0.1L×0.09g/L=0.009g,設鋁的質量為x,則有:
2Al+6HCl═2AlCl3+3H2↑
54 6
x 0.009g
$\frac{54}{x}$=$\frac{6}{0.009g}$
x=0.081g
故填:0.081;
【探究活動二】(1)鋁的化學性質很活潑,易被氧氣氧化生成致密的氧化鋁保護膜,阻止反應的進行,故填:鋁與氧氣反應生成一層致密的氧化鋁薄膜附在鋁的表面,阻止反應的進行;
(2)要使鋁箔燃燒,可以用火柴引燃,然后伸進盛有氧氣的集氣瓶中,故填:將鋁箔卷曲,尖端夾一根火柴,將火柴引燃后,把火柴和鋁箔一起伸入到盛有氧氣的集氣瓶中即可觀察到鋁箔燃燒并發出耀眼的白光;
【探究活動三】(1)鋁與氯化銅反應生成氯化鋁和銅,化學方程式為:2Al+3CuCl2═2AlCl3+3Cu;
(2)對比兩個實驗,氯化銅溶液中能快速出現紅色的物質,說明對鋁與銅鹽溶液的反應可能有促進作用的離子是氯離子;可以才硫酸銅溶液中加入含有氯離子的氯化鈉來進行實驗,故填:Cl-;NaCl.
故答案為:【提出問題】錫和鋁都能與鹽酸反應生成氫氣;加熱;
【探究活動一】(1)從水準管一端注入水,待水準管和量氣管出現較大高度差為止,靜止幾分鐘,兩側高度差不縮小,證明裝置氣密性好;
(2)0.081;
【探究活動二】(1)鋁與氧氣反應生成一層致密的氧化鋁薄膜附在鋁的表面,阻止反應的進行;
(2)將鋁箔卷曲,尖端夾一根火柴,將火柴引燃后,把火柴和鋁箔一起伸入到盛有氧氣的集氣瓶中即可觀察到鋁箔燃燒并發出耀眼的白光;
【探究活動三】(1)2Al+3CuCl2═2AlCl3+3Cu;
(2)Cl-;NaCl.
點評 本題考查的是金屬化學性質的實驗探究,完成此題,可以依據已有的金屬的性質結合物質間反應的實驗現象進行.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:初中化學 來源: 題型:實驗探究題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| 物質 | X | Y | Z | W |
| 反應前質量/g | 10 | 2.2 | 16.2 | 0.9 |
| 反應后質量/g | a | 4.4 | 8.1 | 1.8 |
| A. | a=15 | |
| B. | X、Z是反應物,Y、W是生成物 | |
| C. | Z為化合物 | |
| D. | 反應中Y、W兩種物質變化的質量比為22:9 |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| 選項 | 物質 | 所含雜質 | 除雜質的方法 |
| A | 氯化鈣溶液 | 稀鹽酸 | 加入過量的碳酸鈣、過濾 |
| B | 硫酸鉀溶液 | 氫氧化鉀 | 適量的稀硫酸 |
| C | 二氧化碳 | 氯化氫 | 通過足量的碳酸氫鈉溶液 |
| D | 二氧化錳 | 氯化鉀 | 加水溶解、過濾、蒸發、結晶 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com