
2008年北京市高級中等學校招生考試
化學試卷
可能用到的相對原子質量
H
部分堿和鹽和溶解性表(
陽離子
陰離子







溶
微
不
不
不
不

不
不
微
不
不
不
第Ⅰ卷 (機讀卷 共30分)
一、選擇題(每小題只有一個選項符合題意。共30個小題,每小題1分,共30分。)
1.地殼中含量最多的元素是
A.氧 B.硅 C.鋁 D.鐵
2.天然氣是重要的化石燃料,其主要成分是
A.氧氣 B.氮氣 C.氫氣 D.甲烷
3.下列過程中,屬于化學變化的是

A.蠟燭燃燒 B.冰雪融化 C.菠蘿榨汁 D.透水磚滲水
4.下列物質中,屬于氧化物的是
A. NaCl B. MnO
5.下列金屬中,金屬活動性最強的是
A. Zn B. Mg C. Fe D. Cu
6.下列物質中,含有氧分子的是
A. O2 B. H2O C. CO2 D. SO2
7.為防止骨質疏松,應補充的元素是
A. 鐵 B. 鋅 C. 鈣 D. 碳
8.決定元素種類的是
A.質子數 B.中子數 C.電子數 D.最外層電子數
9.在日常生活中,不作調味品的物質是
A.食鹽 B.蔗糖 C.白醋 D.自來水
10.下列物質中,屬于純凈物的是

11.古人曾有贊美菊花的詩句“沖天香陣透長安”。濃郁的花香遍布長安的原因是
A.分子的質量很小 B.分子間有間隔
C.分子在不斷運動 D.分子由原子構成
12.下列二氧化碳的用途中,不正確的是
A.供給呼吸 B.用作氣體肥料 C.用于滅火 D.生產碳酸飲料
13.下列物質中,不需密封保存的是
A.濃硫酸 B.氫氧化鈉 C.大理石 D.澄清石灰水
14.汽車安全氣囊內的物質能在碰撞后 內迅速反應,生成一種空氣中含量最多的氣體,該氣體是

A. 氧氣 B. 二氧化碳 C. 氮氣 D. 稀有氣體
15.下列化學方程式書寫正確的是
A.
B.
C.
 D.
D. 
16.農作物缺鉀時,抗病蟲害和抗倒伏能力降低,此時應該施用的化肥是
A. B.
B.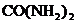 C.
C.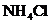 D.
D.
17.北京是極度缺水的城市。作為北京市民,下列生活習慣應該摒棄的是
A.用盆接水洗菜 B.用養魚水澆花草
C.使用節水龍頭 D.丟棄未喝完的礦泉水瓶
18.下列實驗基本操作中,正確的是
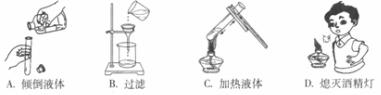
19.下列物質的性質中,屬于化學性質的是
A.鉛具有導電性 B.碳酸氫鈉能與稀鹽酸反應
C.氯化鈉是白色固體 D.常溫下甲烷是無色無味氣體
20.下列是一些物質的,酸堿性最接近中性的是
A.蘋果汁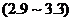 B.蕃茄汁
B.蕃茄汁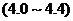
C.玉米粥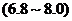 D.肥皂水
D.肥皂水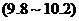
21.除去CO中混有的少量的方法是
A.通入濃硫酸 B.通入氫氧化鈉溶液
C.點燃混合氣體 D.通過灼熱的氧化鐵
22.下圖所示裝置可用于測定空氣中氧氣的含量,實驗前在集氣瓶內加入少量水,并做上記號。下列說法中,不正確的是
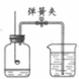
A.實驗時紅磷一定過量
B.點燃紅磷前先用彈簧夾夾緊乳膠管
C.紅磷熄滅后立刻打開彈簧夾
D.最終進入瓶中水的體積約為氧氣的體積
23.下列實際應用中,利用中和反應原理的是
①用生石灰作食品干燥劑 ②用熟石灰和硫酸銅配制波爾多液
③施用熟石灰改良酸性土壤 ④用氫氧化鈉溶液處理泄漏的濃硫酸
A.①② B.③④ C.①④ D.②③
24.下圖為某有機物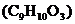 的分子模型,該有機物是一種高效食品防腐劑。下列說法中,不正確的是
的分子模型,該有機物是一種高效食品防腐劑。下列說法中,不正確的是
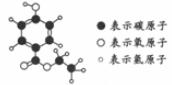
A.該有機物由3種元素組成
B.該有機物能減緩食品變質
C.該有機物分子中碳、氧原子的個數比為3:1
D.該有機物中含氧元素的質量分數最小
25.“三效催化轉換器”可將汽車尾氣中有毒氣體處理為無毒氣體。下圖為該反應的微觀示意圖,其中不同的球代表不同種原子。下列說法中,不正確的是
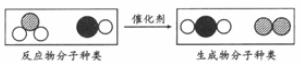
A.分子在化學變化中可分 B.此反應一定有單質生成
C.原子在化學變化中不可分 D.參加反應的兩種分子的個數比為1:1
26.下列連線前后關系不正確的是
A.限制使用塑料袋――減少污染 B.杜絕非法開采礦山――保護資源
C.開采海底石油――開發新能源 D.研制自清潔玻璃――研究新材料
27.為比較4種金屬X、Y、Z、W的金屬活動性,小剛進行了一系列實驗,結果如下表所示。其中能反應的記為“√”,不能反應的記為“-”,無標記的表示未做該實驗。
參加反應的物質
X
Y
Z
W
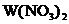 溶液
溶液
-
√
-
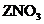 溶液
溶液
√
√
√
稀鹽酸
-
√
-
√
則它們的金屬活動性順序為
A. B.
B.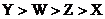
C. D.
D.
28. 新型納米材料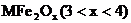 中M表示
中M表示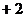 價的金屬元素,在反應中化合價不發生變化。常溫下,
價的金屬元素,在反應中化合價不發生變化。常溫下,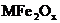 能使工業廢氣中的
能使工業廢氣中的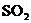 轉化為S,轉化流程如下圖所示:
轉化為S,轉化流程如下圖所示:

已知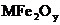 中Fe為
中Fe為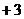 價,下列說法中,不正確的是
價,下列說法中,不正確的是
A.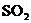 是大氣污染物 B.
是大氣污染物 B.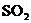 不是該反應的催化劑
不是該反應的催化劑
C.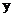 的數值為4 D.
的數值為4 D.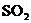 發生了分解反應
發生了分解反應
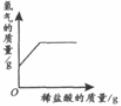
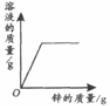
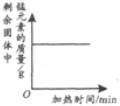
29.下列4個坐標圖分別表示4個實驗過程中某些質量的變化,其中正確的是
A
B
C
D
向一定量鐵粉中滴加稀鹽酸
向一定量硫酸銅溶液中不斷加入鋅粉
加熱一定量高錳酸鉀固體
向一定量氫氧化鈉溶液中滴加稀鹽酸

30.某粗鹽樣品中含有可溶性的氯化鎂、氯化鈣雜質和不溶性的泥沙。常溫下,將140g該粗鹽樣品溶解于水中,過濾得到不足3g泥沙和1000g溶液。取出500g溶液進行測定,其中含有鎂元素1.2g,鈣元素2g,氯元素42.6g。則原粗鹽中氯化鈉的質量分數約為
A. B.
B.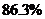 C.
C.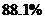 D.
D.
第Ⅱ卷 (非機讀卷 共50分)
二、填空題(共5小題,每空1分,共26分。)
31.(5分)2008年8月8日,第29屆奧運會在北京舉行。
(1)北京奧運場館倍受世人矚目。下列介紹的材料中,屬于有機合成材料的是________(填字母,下同)。

(2) 北京奧運會期間供應的重點菜肴之一是北京烤鴨。食用烤鴨時配以薄餅、大蔥、甜面醬和黃瓜等,營養豐富,其中含有的營養素有油脂、糖類、___________、水、維生素和無機鹽等。
(3)北京奧運村的生活熱水都由太陽能熱水利用系統提供。下列有關太陽能的說法中,正確的是____________________。

A. 取之不盡 B. 是化石燃料 C. 是無污染能源 D. 可轉變為熱能、電能
(4)北京奧運祥云火炬上端的外壁有430個通氣孔。這些孔不僅能把燃燒的廢氣排出去,還能_____________________,以保證燃料的充分燃燒。
(5)北京奧運“藍天計劃”重在改善北京的空氣質量。市政府采取的有效措施之一是冬季用燃燒天然氣代替燃煤取暖,該項措施的作用是 ________。
32.(4分)下列數據是硝酸鉀固體在不同溫度時的溶解度。
溫度/℃
0
20
40
60
80
溶解度/g
13.3
31.6
63.9
110
169
(1)硝酸鉀溶液中的溶劑是__________。
(2)20℃時,向 水中加入 硝酸鉀,充分溶解后得到__________(填“飽和”或“不飽和”)溶液。
(3)20℃時,向 水中加入 硝酸鉀,若使硝酸鉀完全溶解,可以采用的方法是_____________。
(4)如圖所示,小燒杯中盛放的是上述(2)中所得的硝酸鉀溶液。若將少量的下列物質分別小心地加入到大燒杯的水中,不斷攪拌,一定能夠使小燒杯中有固體析出的是___________(填字母)。

A.冰 B.濃硫酸 C.硝酸銨 D.干冰 E.氫氧化鈉 F.氧化鈣
33.(6分)鋼鐵是重要的金屬材料。
(1)下列鐵制品的用途中,利用金屬導熱性的是______________(填字母,下同)。

(2)目前世界上已有50%以上的廢鋼鐵得到回收利用,其目的是___________。
A. 節約金屬資源 B. 合理開采礦物 C. 防止鋼鐵生銹
(3)為防止水龍頭生銹,其表面鍍有一層鉻。鐵生銹的條件是______________。
(4)將生銹的鐵制品放入盛有過量稀鹽酸的洗槽中,觀察到溶液變黃,有無色氣泡逸出。
①寫出發生反應的化學方程式 _____________________________________________
____________________________________。
②氯化鐵溶液可以作凈水劑。欲將上述所得溶液中含鐵的物質以氯化鐵形式回收,加入過氧化氫溶液反應可生成氯化鐵和水。已知每生成162.5g的氯化鐵,就同時生成18g的水。則該反應的反應物的化學式為________________________________________。
34.(5分)消毒劑在公共場所進行衛生防疫時發揮著重要的作用。
(1)氫氧化鈉能殺滅細菌、病毒和寄生蟲卵等,它的俗名為______________。
(2)二氧化氯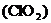 可用于飲用水的殺菌消毒,其中氯元素的化合價為________。
可用于飲用水的殺菌消毒,其中氯元素的化合價為________。
(3)氧化鈣與水反應后生成一種具有消毒能力的物質,該物質的化學式為________。
(4)過氧乙酸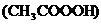 是被廣泛使用的高效消毒劑,它不穩定易分解放出一種常見的氣體單質,并生成醋酸
是被廣泛使用的高效消毒劑,它不穩定易分解放出一種常見的氣體單質,并生成醋酸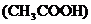 ,該反應的化學方程式為__________________
,該反應的化學方程式為__________________
______________________________________;若一瓶久置的過氧乙酸溶液已完全分解,所得溶液中醋酸的質量分數為12%,則原溶液中過氧乙酸的質量分數為______________%(結果保留一位小數)。
35.(6分)A~G是初中化學常見的7種物質,其中至少有一種物質是無色氣體,且A與G含有相同的金屬元素。它們在一定條件下轉化關系如下圖所示,其中部分反應物或生成物已略去。
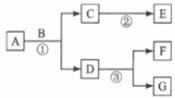
請針對以下兩種情況回答問題。
(1)若A中兩種元素的質量比為 ,F是一種紅色金屬,則F的化學式為________;寫出反應①、③的化學方程式:
①_____________________________________________;
③_____________________________________________。
(2)若F與C常溫下可以反應,②、③屬于同一種基本反應類型,則A的化學式為______;寫出反應①的化學方程式_________________________________________;反應②的基本反應類型是______________。
三、實驗題(共3小題,每空1分,共18分。)
36.(6分)根據下圖所示水、二氧化碳和氧氣的性質實驗,請回答以下問題。
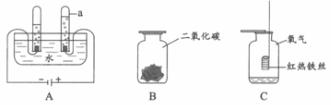
(1)儀器a的名稱是_________________________。A裝置中發生反應的化學方程式為_____
_____________________________________。用帶火星的木條檢驗a中的氣體,觀察到木條復燃,該氣體是__________。
(2)將白色紙花用紫色石蕊試液噴濕,放入集氣瓶B中,觀察到的現象是___________。
(3)集氣瓶C中的現象:鐵絲在氧氣中劇烈燃燒,_______________,放出大量的熱,有黑色固體生成。該反應的化學方程式為_____________________________。
37.(4分)老師用下圖所示裝置為同學們做了一個興趣實驗。A裝置中盛有二氧化錳黑色粉末,B裝置中盛有足量的澄清石灰水,C裝置中盛有足量的稀鹽酸,氣球中裝有少量的碳酸鈉粉末。
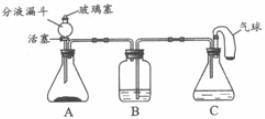
(1)打開分液漏斗的活塞和玻璃塞,使A裝置與大氣相通,將氣球中的碳酸鈉粉末全部倒入稀鹽酸中,可以觀察到C裝置中的現象是_______________________________________。
(2)待上述反應結束后,從分液漏斗注入足量的過氧化氫溶液,關閉活塞和玻璃塞,A裝置中發生反應的化學方程式為___________________________________________。
(3)在整個實驗過程中,B裝置中的現象是______________________________。
(4)C裝置中氣球的作用是___________(填字母)。
a. 收集純凈氣體 b. 添加固體藥品
c. 調節C裝置容積 d. 控制氣體總量
38.(8分)實驗盒中有7種沒有標簽的溶液,老師讓化學實驗小組同學鑒別這些溶液。

(1)調查研究:
①實驗盒中記錄單上登記的7種溶液是: 、
、 、
、 、
、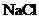 、
、 、
、 和稀鹽酸,其中有顏色的是________
溶液。
和稀鹽酸,其中有顏色的是________
溶液。
②查閱資料:無色有刺激性氣味的氯化氫氣體溶于水得到鹽酸。
③研究方式:從5種無色溶液中任意取出4種為一組進行鑒別。這樣的組合共有______組。
(2)提出假設:同學們從5種無色溶液中取出4種,貼上A、B、C、D標簽,并且假設這一組溶液可能是 、
、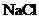 、
、 和稀鹽酸。
和稀鹽酸。
(3)實驗探究:同學們按以下步驟進行鑒別。
第一步:取4支試管,分別加入少量的A、B、C、D溶液,然后依次加入少量鹽酸,實驗現象記錄如下:
溶液
A
B
C
D
加入鹽酸后的現象
無明顯變化
無明顯變化
有氣泡產生
無明顯變化
實驗結論:C是_______________溶液。
第二步:依據下圖裝置進行實驗,其中夾持固定裝置已略去。從長頸漏斗加入鹽酸,可以觀察到C溶液中有氣泡產生,A溶液中有白色沉淀生成,B、D溶液均無明顯變化。
實驗解釋:A溶液中發生反應的化學方程式為_______________________。

第三步:依據下圖裝置進行2個實驗。取少量B溶液倒入蒸發皿,加熱,聞到有刺激性氣味,停止加熱。再取少量D溶液倒入另一蒸發皿,加熱,有白色固體析出,停止加熱。
實驗結論:B是稀鹽酸,D是NaCl溶液。

經過上述三步實驗,同學們認為第5種無色溶液是NaOH溶液。
(4)實驗反思:老師引導同學們討論了上述實驗探究過程。進行了全面反思。
①老師指出:實驗結論仍有不確定性。不能確定的是______________溶液;其鑒別方法是__________________________________________________________________________
②老師提示:鑒別出C溶液后,不需外加試劑,就可以簡便地鑒別出A、B溶液。請完成下列實驗報告。
實驗步驟
實驗現象和結論
四、計算題(共2小題,共6分。)
39.(3分)CO是大氣污染物之一。用氯化鈀 可以測定微量CO的存在,該反應的化學方程式為
可以測定微量CO的存在,該反應的化學方程式為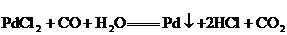 。若反應后得到Pd的質量為1.06g,則測得CO的質量為多少克?(已知Pd的相對原子質量為106)
。若反應后得到Pd的質量為1.06g,則測得CO的質量為多少克?(已知Pd的相對原子質量為106)
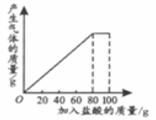
40.(3分)有一種石灰石樣品的成分是CaCO3和SiO2 。課外小組同學將100g鹽酸分5次加入到35g石灰石樣品中(已知SiO2不與鹽酸反應),得到如下部分數據和圖象。
次數
第1次
第2次
第3次
加入鹽酸的質量/g
20
20
20
剩余固體的質量/g
30
a
20
請計算:
(1)第2次加入鹽酸后,a為________________g。
(2)石灰石樣品中鈣元素、碳元素和氧元素的質量比為多少?(結果用最簡整數比表示)(3)10%的CaCl2溶液可作路面保濕劑。欲將第5次實驗后的溶液配成10%的CaCl2溶液,可先向此溶液中加入足量的石灰石粉末,完全反應后過濾,這時還需要向濾液中加入水多少克?(假設實驗過程中溶液損失忽略不計)
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com