
2006-2007學年度第二學期期中考試
八年級化學試題
注意:本次考試根據答題情況(字跡是否工整,卷面是否整潔,答題是否規范)設卷面分。卷面分最大值為5分,采用加分的辦法按0、1、3、5四檔計分。
相對原子質量:H:1 C:12 N:14 O:16 Na:23 Cl:35.5 Ca:40
一、選擇題:(40分)每小題有1~2個正確答案,將正確答案填入題后答題欄中。
1.推理是化學學習中常用的思維方法。以下4個推斷正確的是
A.氧化物都含有氧元素,所以含有氧元素的化合物一定是氧化物
B.實驗室制取氧氣,必需使用含氧元素的化合物進行制取
C.物質與氧氣反應有熱量放出,且都伴隨有火焰或光的現象產生
D.組成物質元素的化合價是定值,因此元素在同一物質中只有一種化合價
2.氧氣是空氣的主要成分之一,有關氧氣說法錯誤的是
A.用帶火星的木條可以檢驗氧氣
B.用加熱高錳酸鉀的方法可以制取氧氣
C.魚類能在水中生活,證明氧氣易溶于水
D.鐵絲能在氧氣中燃燒,火星四濺,產生黑色固體
3.高鐵酸鉀(K2FeO4)是一種具有氧化、吸附、凝聚、殺菌等功能的新型、高效水處理劑。它與水反應的化學方程式為:4K2FeO4+10H2O=4Fe(OH)3↓+8X+3O2↑,則X的化學式為
A.K2O B.KOH C.K D.KH
4.空氣質量日報是環境監測部門對一個地區空氣質量情況所做的監測報告。目前計入空氣主要污染物的是可吸入顆粒物、一氧化碳、二氧化碳、二氧化硫、氮的氧化物。下列情況能直接造成空氣污染的是
A.把煤作為主要燃料 B.隨意丟棄塑料垃圾、廢舊電池
C.大量使用化學肥料 D.利用太陽能、風能、等清潔能源
5.每年春天,我國北方都發生強烈的沙塵暴,大量沙塵不僅降落到北京,甚至遠降韓國,日本也能觀察到沙塵。專家對沙塵褒貶不一,有專家研究表明,沙塵能減弱酸雨的酸性,減弱溫室效應,也有專家研究表明,沙塵是形成酸雨的原因之一。根據上述短文和你所學的知識判斷,下列關于“沙塵”的說法中有錯誤的是
A.沙塵已成為跨國的環境問題
B.飄浮在空氣中的沙塵屬于空氣質量周報時“首要污染物”中的可吸入顆粒物
C.沙塵形成酸雨,可能是沙塵吸收了經過地區被污染空氣中的氮、硫氧化物所致
D.沙塵都可用來改良酸性土壤
6.根據所學化學知識,判斷下列說法中正確的是
A.加碘鹽中的“碘”通常是指碘單質 B.空氣是由幾種單質組成的混合物
C.催化劑在化學反應中都能加快物質的化學反應速率
D.物質發生化學反應時都遵循質量守恒定律
7.檢驗某可燃燒的化合物是否含有氫、碳、氧3種元素,在該物質完全燃燒后還必須進行的實驗是:①用帶火星的木條檢驗;②用無水硫酸銅檢驗;③用澄清石灰水檢驗;④對反應物、生成物進行稱量。以下選項中正確的是
A.①②③④ B.②③④ C.①②③ D.②③
8.從安全、環保、節能、簡便等方面考慮,實驗室制取氧氣的最佳方法是
 A.通電分解水:2H2O 2H2↑
+ O2↑
A.通電分解水:2H2O 2H2↑
+ O2↑
 B.過氧化氫催化分解:2H2O2(溶液) 2H2O+O2↑
B.過氧化氫催化分解:2H2O2(溶液) 2H2O+O2↑
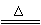
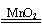 C.氯酸鉀受熱分解:2KClO3 2KCl+3O2↑
C.氯酸鉀受熱分解:2KClO3 2KCl+3O2↑
 D.高錳酸鉀受熱分解:2KMnO4 K2MnO4
+ MnO2 + O2↑
D.高錳酸鉀受熱分解:2KMnO4 K2MnO4
+ MnO2 + O2↑
9.關于一氧化碳在空氣中燃燒 2CO+O2 2CO2的說法正確的是
A.反應過程中吸收大量的熱
B.反應前后分子個數改變
C.參加反應的一氧化碳和氧氣的質量比為2:l
D.化學方程式中反應物的化學計量數之比表示為ν (CO):ν (O2) =2:1
10.下列化學方程式符合題意且書寫正確的是
 A.細鐵絲在氧氣中燃燒 4Fe+3O2 2Fe2O3
A.細鐵絲在氧氣中燃燒 4Fe+3O2 2Fe2O3
B.鹽酸滴到鐵器上 Fe+2HCl=== FeCl2+H2↑
C.胃酸過多的病人服用小蘇打 NaHCO3+HCl=== NaCl+CO2↑+H2O
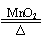 D.氯酸鉀和二氧化錳混合加熱 2KClO3 2KCl+O2↑
D.氯酸鉀和二氧化錳混合加熱 2KClO3 2KCl+O2↑
11.下列關于化學反應"X2十3Y2=2Z”的敘述錯誤的是
A.Z的化學式為XY3
B.若mg X2和ngY2恰好完全反應,則生成(m+n)g Z
C.若X2和Y2的相對分子質量分別為M和N,則Z的相對分子質量為(M+N)
D.若ag X2完全反應生成bg Z,則同時消耗(a一b)g Y2
12.甲、乙、丙、丁是初中化學中常見的四種物質,它們有如下轉化關系:
①甲+丁→H2O ②乙+丁→CO2 ③丙+丁→H2O+CO2。則丙可能為
 A.H2 B.CH4 C.C2H5OH D.CO
A.H2 B.CH4 C.C2H5OH D.CO
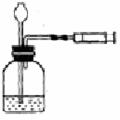
13.用推拉注射器活塞的方法可以檢查右圖裝置的氣密性。當緩慢拉動活塞時,如果裝置氣密性良好,則能觀察到
A.注射器內有液體
B.瓶中液面明顯上升
C.長頸漏斗內液面上升
D.長頸漏斗下端管口產生氣泡
14.新研制的以農作物秸稈為原料的一次性餐盒,廢棄后在自然條件下兩個月就可以分解。下列關于此餐盒的有關說法不正確的是
A.代替塑料餐盒可減少“白色污染”
B.可有效利用秸稈,減少燃燒秸稈產生的空氣污染
C.農作物秸稈屬于化合物
D.這種餐盒是綠色環保產品
15在醫院里給病人輸氧時,常使用右下圖所示裝置。在裝置中盛放大約半瓶蒸餾水,以下幾種說法不正確的是
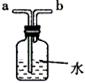 A.b導管連在供氧氣的鋼瓶上
A.b導管連在供氧氣的鋼瓶上
B.b導管連在病人吸氧氣的塑膠管上
C.該裝置可用來觀察是否有氧氣輸出
D.該裝置可用來觀察輸出氧氣的速率
16.NO是大氣污染物,但少量NO在人體內具有擴張血管、增強記憶的功能。實驗室收集NO只能用排水集氣法。對NO的猜想或評價正確的是
A.易溶于水 B.可能極易與氧氣反應
C.易與水反應 D.有害無利
17.鋰電池是新型的高能電池,以質量輕、電容量大,頗受手機、手提電腦等用戶的青睞。某種鋰電池的總反應可表示Li + MnO2 = Li MnO2 。以下說法正確的是
①該反應中Mn的化合價發生了變化②該反應屬于化合反應③Li MnO2為新型的氧化物 ④Li MnO2為鋰、錳、氧的合金
A.①② B.①③ C. ②③ D.③④
18.硅酸鹽礦泉水具有軟化血管的作用,對心臟病、高血壓等疾病患者有良好的醫療保健作用.硅酸鈉的化學式為Na2SiO3,其中硅元素的化合價為
 A.+1 B. +2 C. +3 D. +4
A.+1 B. +2 C. +3 D. +4
19.已知碳酸氫鈉不穩定,受熱易分解2NaHCO3 Na2CO3 +CO2↑+H2O。 現取Na2CO3和NaHCO3的混合物10 g,加熱到質量不再改變為止,剩余固體質量為6.9 g。下列說法正確的是
A.反應后生成CO2的質量為3.1g
B.反應后生成CO2和H2O的質量比為22∶9
C.原混合物中NaHCO3的質量為4.2g
D.原混合物中Na2CO3的質量分數為16%
20.2005年3月,國家質檢局查出一些辣椒醬、番茄醬等食品中含有工業染色劑“蘇丹紅一號”,人食用后可能致癌。“蘇丹紅一號”的化學式為C16H12N2O 。下列有關“蘇丹紅一號”的說法中正確的是
A.“蘇丹紅一號”屬于氧化物
B.“蘇丹紅一號”由30個原子構成
C.“蘇丹紅一號”的相對分子質量為248
D.“蘇丹紅一號”由四種元素組成
二、理解與應用(27分)
21.(4分)完成下列化學反應方程式并標出帶“?”元素的化合價。
+1 +2 -2 +2 -2
H2O2 + BaSO3 = BaSO4↓+
氣體
吸入氣體
呼出氣體
X
78.25%
74.88%
Y
21.05%
15.26%
CO2
0. 04%
3.68%
H2O
0. 66 %
6.18%
22.(4分)右表是小華對自己吸入的氣體和呼出的氣體進行探究的結果(體積分數)
⑴請你判斷:X是_____,Y是____。(填化學式)
⑵請你回答:因參與新陳代謝而被人體消耗的是_____。
⑶請你分析:X氣體在呼吸過程中沒有參與化學反應,但呼出氣體中體積分數卻減少了,原因是:___________________________________________ ____________________________________________。
23.(6分)人類發明并使用氟里昂(主要用作致冷劑)若干年后,科學家發現氟里昂在紫外線的照射下能分解出氯原子破壞臭氧層,其破壞臭氧的循環示意圖如下:
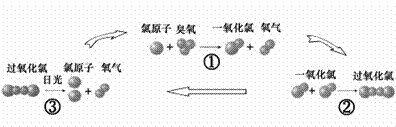 |
⑴請寫出臭氧的化學式_______;
⑵上述反應屬于化合反應的是(填序號)__________;
⑶經過上述①②③的反應過程后,反應物氯原子的個數是否發生變化?______(答:是或否)。
⑷諾貝爾獎金獲得者莫里納博士指出:“少量的氟里昂就能對臭氧層產生巨大的影響”,請你根據循環示意圖論證他的觀點
。
⑸在科學家的建議下,許多國家簽署了停止使用和消費氟里昂的協議,使得大氣中氟里昂的含量得到了控制。請你根據本題提供的信息就怎樣有效保護我們的環境談一點建議或認識:_____________________________________________________。
24.(6分)甲、乙、丙是三個實驗的示意圖,根據圖中所發生的化學反應現象及化學反應原理,進行總結歸納并回答下列問題:
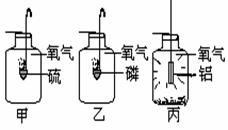 ⑴所發生的三個反應有多
⑴所發生的三個反應有多
個共同的特點,分別是?
① ;
② ;
③ ;
④
⑵甲實驗進行時,燃燒匙中硫的狀態是 。
 ⑶任選上述三個實驗中的一個,寫出反應的化學方程式:
。
⑶任選上述三個實驗中的一個,寫出反應的化學方程式:
。
25.(7分)右圖是費俊龍和聶海勝在“神舟”六號飛船中的照片,請你從化學的視角對神六飛船的有關信息進行思考并作答。
⑴航天員在太空中每人每天大約需要0.9kg氧氣、2.5 L水、0.6 kg食物,排出1.0 kg二氧化碳、1.8kg水蒸氣等。上述的物質中,屬于單質的是____________,屬于化合物的是
___________,屬于混合物的是___________。
⑵為了處理人體排出的CO2,飛船上采用了與氫氧化鈉化學性質相似的氫氧化鋰(LiOH)作為吸收劑。LiOH中鋰元素的化合價是______。
⑶隨著原始大氣中O2緩慢地增加,CH4、NH3、CO等氣體逐漸被氧化而緩慢地減少,使大氣的成分逐漸演化成現代大氣。原始大氣中NH3可轉化為現代大氣中的 。
⑷在神六飛船中有籃球大小的儲氧瓶6個,儲氮瓶2個,它們是航天員的生命之源。艙內空氣一天一換。宇航員說:“艙內的空氣比地面還好。”請你設計:怎樣使得艙內氣體成分大致和地面保持一致?
三、實驗與探究(21分)
 26.(6分)用雙氧水和二氧化錳制氧氣的反應方程式為:2H2O2 2H2O + O2 ↑。某同學做了該實驗后,展開了下列思考與探究:
26.(6分)用雙氧水和二氧化錳制氧氣的反應方程式為:2H2O2 2H2O + O2 ↑。某同學做了該實驗后,展開了下列思考與探究:
⑴催化劑MnO2的用量對反應速率有沒有影響呢?
他做了這樣一組實驗:每次均用30mL10%的H202溶液,采用不同量MnO2粉末做催化劑,測定各次收集到500mL氧氣時所用的時間,結果如下:(其他實驗條件均相同)
實驗次序
1
2
3
4
5
6
7
8
9
10
MnO2粉末用量(克)
0.1
0.2
0.3
0.4
0.5
0.6
0.7
0.8
0.9
1.0
所用時間(秒)
17
8
7
5
4
3
2
2
2
2
請分析表中數據回答:MnO2的用量對反應速率有沒有影響呢?如果有,是怎樣影響的呢?
。
⑵H2O2溶液的溶質質量分數對反應速率有沒有影響呢?
他又做了一組實驗:每次均取5mL30%的H2O2溶液,然后稀釋成不同溶質質量分數的溶液進行實驗。記錄數據如下:(實驗均在20℃室溫下進行,其他實驗條件也均相同)
實驗次序
1
2
3
4
5
6
7
8
H2O2溶液溶質質量分數
1%
3%
5%
10%
15%
20%
25%
30%
MnO2粉末用量(克)
0.2
0.2
0.2
0.2
0.2
0.2
0.2
0.2
收集到540mL氣體時所用時間(秒)
660
220
205
80
25
9
4
3
反應后液體溫度(℃)
24
34
39
56
65
67
69
70
請分析表中數據回答:H2O2溶液的溶質質量分數對反應速率有沒有影響呢?如果有,是怎樣影響的呢?
。
由表中數據還可看出,該反應是個 反應(填“放熱”或“吸熱”)。
⑶還有哪些因素可能影響該反應的速率呢?請說出你的一個猜想: 。
27.(8分)下表列出了空氣、氧氣、二氧化碳、氨氣在標準狀況下的密度和溶解性。
物質
空氣
氧氣
二氧化碳
氨氣
密度(g/L)
1.293
1.429
1.977
0.771
溶解性
/
不易溶
 能溶
能溶
極易溶
已知實驗室可用下列反應制取氨氣:2NH4C1(固)+Ca(OH)2(固) CaCl2+2NH3↑+2H2O。
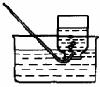
⑴根據上述信息,選擇實驗室制取和收集氧氣、氨氣的裝置,請在相關空格處√。



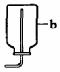
氧氣
氨氣
⑵寫出圖中有標號儀器的名稱:a ;b 。
28.(7分)小明參觀某養魚池時,好奇的發現農民向養魚池中撒一種叫過氧化鈣的淡黃色固體,用來增加魚池中的含氧量。小明剛學完氧氣的實驗室制法,于是他想可否用過氧化鈣來制取氧氣。
[提出問題]過氧化鈣可否用于制取氧氣?
[查閱資料]部分內容如下:過氧化鈣(CaO2)室溫下穩定,在300℃時分解生成氧氣,可作增氧劑、殺菌劑等。
[猜想與驗證]
⑴小明依據 ,提出猜想Ⅰ。
猜想Ⅰ:加熱過氧化鈣可制取氧氣。
實驗裝置
實驗主要過程
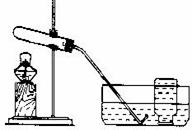
①檢查裝置氣密性。操作如下:先將導管伸入液面下,用手緊握試管,觀察到 ,松開手后,有液體進入導管。
②加入過氧化鈣,加熱,導管口有大量氣泡昌出。
③收集滿一瓶氣體。
④停止加熱。熄滅酒精燈前,應
。
⑤檢驗氣體,方法是
。
實驗結論:加熱過氧化鈣可制取氧氣。
⑵分析與反思:
①雖然沒有快速收集到大量氧氣,由此實驗現象,小明認為農民用過氧化鈣作增氧劑的主要原因是 。
②小明希望對此實驗進行改進,使該反應加快,你能幫他提出建議嗎?
你的合理建議是 。
以上建議是否可行,還需進一步通過實驗驗證。
 四、計算(12分)
四、計算(12分)
31、(4分)實驗室有一瓶未開封的濃鹽酸,部分標簽如右圖所
示。這瓶濃鹽酸中溶液的質量為 g.若用這瓶濃鹽
酸來配制200g溶質質量分數為10%的稀鹽酸,需量取濃鹽酸
的體積是 mL,水的體積是 mL。
32、(8分)家里蒸饅頭用的純堿中含有少量的氯化鈉,課外探究小組的同學欲測定純堿中碳酸鈉的含量。他們取該純堿樣品11.0g,全部溶解在100.0g水中,再加入氯化鈣溶液141.0g,恰好完全反應,化學反應方程式為:Na2CO3+CaCl2=2NaCl+CaCO3↓過濾干燥后,稱得沉淀質量為10.0g。請計算:
⑴純堿樣品中碳酸鈉的質量;
⑵反應后所得濾液中溶質的質量分數。
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com