
【題目】微生物燃料電池的研究已成為治理和消除環境污染的重要課題,其工作原理如圖所示![]() 、B、M、N均為惰性電極
、B、M、N均為惰性電極![]() 。下列說法正確的是
。下列說法正確的是
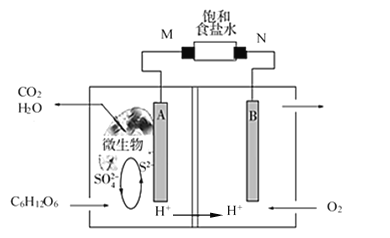
A.該電池負極區發生一個化學反應
B.M電極附近產生黃綠色氣體
C.消耗![]() 時轉移
時轉移![]()
D.升高溫度一定能增大電流
 走進文言文系列答案
走進文言文系列答案科目:高中化學 來源: 題型:
【題目】下列裝置由甲、乙部分組成(如圖所示),甲是將廢水中乙二胺[H2N(CH2)2NH2]氧化為環境友好物質形成的化學電源。當電池工作時,下列說法正確的是

A. 電子的流動方向M→Fe→CuSO4溶液→Cu-N
B. M極電極反應式: H2N(CH2)2NH2+16OH--16e-==2CO2↑+N2↑+12H2O
C. 當N極消耗5.6LO2時,則鐵極增重32g
D. 一段時間后,乙中CuSO4溶液濃度基本保持不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用50mL 0.50mol/L鹽酸與50mL 0.55mol/LNaOH溶液在如圖所示的裝置中進行中和反應.通過測定反應過程中所放出的熱量可計算中和熱.回答下列問題:
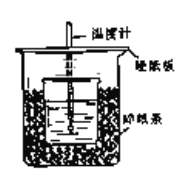
(1)從實驗裝置上看,圖中尚缺少的一種玻璃用品是________________;由圖可知該裝置有不妥之處,應如何改正?___________________________________________________.
(2)燒杯間填滿碎塑料泡沫的作用是__________________________________________.
(3)如果用60mL 0.50mol/L鹽酸與50mL 0.55mol/LNaOH溶液進行反應,與上述實驗相比,所求得的中和熱數值___________(填“相等、不相等”)
(4)用相同濃度和體積的氨水(NH3·H2O)代替NaOH溶液進行上述實驗,測得的中和熱的數值會____________(填“偏大”、“偏小”、“無影響”).
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下,在一恒容密閉容器中,能表示反應 X(g)+2Y(g)![]() 2Z(g) 一定達到化學平衡狀態的是( )
2Z(g) 一定達到化學平衡狀態的是( )
①容器中氣體的密度不再發生變化 ② X、Y、Z的濃度不再發生變化 ③容器中的壓強不再發生變化 ④單位時間內生成n mol Z,同時生成2n mol Y
A.①②B.②③C.③④D.①④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】把8.0g鐵粉投入40mL某HNO3溶液中,充分反應后剩余固體2.4g,產生NO2和NO的混合氣體0.12mol。若不考慮N2O4的存在,則原HNO3溶液的物質的量濃度( )
A.6.0mol·L-1B.7.0mol·L -1C.8.0mol·L -1D.9.0mol·L -1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列指定反應的化學用語表達正確的是( )
A | 質子交換膜氫氧燃料電池的負極反應 | O2+2H2O+4e﹣=4OH﹣ |
B | 用鐵電極電解飽和食鹽水 | 2Cl﹣+2H2O=Cl2↑+H2↑+20H﹣ |
C | 鍋爐水垢中的CaSO4用飽和Na3CO3溶液浸泡 | CO32﹣+CaSO4=CaCO3+SO42﹣ |
D | KClO堿性溶液與Fe(OH)3反應制取K2FeO4 | 3ClO﹣+2Fe(OH)3=2FeO43﹣+3Cl﹣+4H++H2O |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氮(N)、磷(P)、砷(As)等都是ⅤA族的元素,該族元素的化合物在研究和生產中有許多重要用途。回答下列問題:
(1)化合物N2H4的電子式為___________________。
(2)As原子的核外電子排布式為_______________________。
(3)P和S是同一周期的兩種元素,P的第一電離能比S大,原因是_______________。
(4)NH4+中H-N-H的健角比NH3中H-N-H的鍵角大,原因是_________________。
(5)Na3AsO4中含有的化學鍵類型包括________;AsO43-空間構型為________,As4O6的分子結構如圖所示,則在該化合物中As的雜化方式是________________。

(6)白磷(P4)的晶體屬于分子晶體,其晶胞結構如圖(小圓圈表示白磷分子)。己知晶胞的邊長為acm,阿伏加德羅常數為NAmol-1,則該晶胞中含有的P原子的個數為_________,該晶體的密度為_______g·cm-3(用含NA、a的式子表示)。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】電化學原理在生產生活中應用十分廣泛。請回答下列問題:
(1)通過SO2傳感器可監測大氣中SO2的含量,其工作原理如圖1所示。
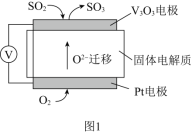
①固體電解質中O2-向______極移動(填“正”或“負”)。
②寫出V2O5電極的電極反應式:_____________。
(2)近期科學家研究發現微生物可將生產廢水中的尿素[CO(NH2)2]直接轉化為對環境友好的兩種物質,其工作原理如圖2所示。回答下列問題:
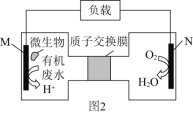
①N極為____極(填“正”或“負”),M電極反應式______________________。
②N極消耗標準狀況下33.6L氣體時,M極理論上處理的尿素的質量為______g。
(3)人工光合系統裝置(如圖)可實現以CO2和H2O合成CH4。下列說法不正確的是__________。
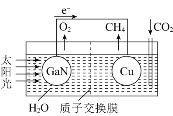
A.該裝置為原電池,且銅為正極
B.電池工作時,H+向Cu電極移動
C.GaN電極表面的電極反應式為2H2O-4e-=O2+4H+
D.反應CO2+2H2O![]() CH4+2O2中每消耗1molCO2轉移4mole-
CH4+2O2中每消耗1molCO2轉移4mole-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某有機物的結構簡式為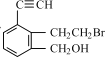 。下列關于該有機物的說法中正確的是
。下列關于該有機物的說法中正確的是
A.能與 HBr 發生取代反應
B.能與 Br2/CCl4 溶液發生加成反應
C.能與 NaOH 的水溶液發生消去反應
D.1 mol 該有機物最多能與 2 mol H2 發生加成反應
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com