
【題目】世上萬物、神奇可測,其性質與變化是物質的組成與結構發生了變化的結果。回答下列問題。
(1)根據雜化軌道理論判斷,下列分子的空間構型是V形的是_____(填字母)。
A.BeCl2 B.H2O C.HCHO D.CS2
(2)原子序數小于36的元素Q和T,在周期表中既位于同一周期又位于同一族,且T的原子序數比Q多2。T的基態原子的外圍電子(價電子)排布式為____,Q2+的未成對電子數是_____。
(3)銅及其合金是人類最早使用的金屬材料,Cu2+能與NH3形成配位數為4的配合物[Cu(NH3)4]SO4。
①制元素在周期表中的位置是______,[Cu(NH3)4]SO4中,N、O、S三種元素的第一電離能由大到小的順序為______。
②[Cu(NH3)4]SO4中,存在的化學鍵的類型有______(填字母)。
A離子鍵 B金屬鍵 C.配位鍵 D.非極性鍵 E極性鍵
③NH3中N原子的雜化軌道類型是______,寫出一種與SO42-互為等電子體的分子的化學式:_ ______。
④[Cu(NH3)4]2+具有對稱的空間構型,[Cu(NH3)4]2+中的兩個NH3被兩個Cl-取代,能得到兩種不同結構的產物.則[Cu(NH3)4]2+的空間構型為_________。
(4)氧與銅形成的某種離子晶體的晶胞如圖所示。則該化合物的化學式為_____,如果該晶體的密度為ρg/cm3,則該晶體內銅離子與氧離子間的最近距離為_____(用含ρ的代數式表示,其中阿伏加德羅常數用NA表示)cm。

【答案】 B 3d84s2 4 第四周期IB族 N>O>S ACE sp3 CCl4(或其他合理答案) 平面正方形 CuO 
【解析】(1)BeCl2分子中,鈹原子含有兩個共價單鍵,不含孤電子對,所以價層電子對數是2,中心原子以sp雜化軌道成鍵,分子的立體構型為直線形,A錯誤;水分子中孤電子對數![]() ,水分子氧原子含有2個共價單鍵,所以價層電子對數是4,中心原子以
,水分子氧原子含有2個共價單鍵,所以價層電子對數是4,中心原子以![]() 雜化軌道成鍵,價層電子對互斥模型為四面體型,含有2對孤對電子,分子的立體構型為V形,B正確; HCHO分子內
雜化軌道成鍵,價層電子對互斥模型為四面體型,含有2對孤對電子,分子的立體構型為V形,B正確; HCHO分子內![]() 碳原子形成3個
碳原子形成3個![]() 鍵,無孤對電子,分子中價層電子對個數
鍵,無孤對電子,分子中價層電子對個數![]() ,雜化方式為
,雜化方式為![]() 雜化,價層電子對互斥模型為平面三角形,沒有孤電子對,分子的立體構型為平面三角形,C錯誤;二硫化碳分子中碳原子含有2個
雜化,價層電子對互斥模型為平面三角形,沒有孤電子對,分子的立體構型為平面三角形,C錯誤;二硫化碳分子中碳原子含有2個![]() 鍵且不含孤電子對,采用sp雜化,其空間構型是直線形,D錯誤;正確選項B。
鍵且不含孤電子對,采用sp雜化,其空間構型是直線形,D錯誤;正確選項B。
(2) 原子序數小于36的元素Q和T,在周期表中既處于同一周期又位于同一族,則Q、T處于第Ⅷ族,且原子序數T比Q多2,則Q為Fe元素,T為Ni元素,Ni元素是28號元素,Ni原子價電子排布式為3d84s2,Fe2+的核外電子排布式為1s24s22p63s23d6,3d能級有4個未成對電子;正確答案:3d84s2 ;4 。
(3) ①銅元素核電荷數為29,在周期表中的位置是第四周期IB族;N、O屬于同一周期,由于N原子的2p軌道處于半充滿狀態,故第一電離能N>O,而O、S在同一主族,同主族元素的第一電離能從上到下依次減小,故第一電離能O>S,則N>O>S;正確答案:N>O>S。
②[Cu(NH3)4]SO4中,SO2-4和[Cu(NH3)4]2+間存在離子鍵,N原子和Cu原子間存在配位鍵,N—H鍵、S—O鍵為極性鍵,選A、C、E;正確答案:A、C、E。
③NH3中N原子的價電子對數=![]() (5-1×3)+3=4,故采取sp3雜化方式,與SO2-4互為等電子體的分子的化學式為CCl4、SiCl4等;正確答案:sp3 ; CCl4。
(5-1×3)+3=4,故采取sp3雜化方式,與SO2-4互為等電子體的分子的化學式為CCl4、SiCl4等;正確答案:sp3 ; CCl4。
④[Cu(NH3)4]2+具有對稱的空間構型,[Cu(NH3)4]2+中的兩個NH3被兩個Cl-取代,能得到兩種不同結構的產物,則[Cu(NH3)4]2+的空間構型為平面正方形;正確答案:平面正方形。
(4) 由均攤法知,1個晶胞中含4個銅離子,氧離子為8×![]() +1+2×
+1+2×![]() +4×
+4×![]() =4個,則該化合物的化學式為CuO;晶體內銅離子與氧離子間的最近距離為晶胞體對角線長的
=4個,則該化合物的化學式為CuO;晶體內銅離子與氧離子間的最近距離為晶胞體對角線長的![]() ;設晶胞的邊長為acm,平均1個晶胞質量m=
;設晶胞的邊長為acm,平均1個晶胞質量m=![]() ×80 g,體積V=a3cm3,則由ρ=
×80 g,體積V=a3cm3,則由ρ=![]() ,可解得a=
,可解得a=![]() 。則晶體內銅離子與氧離子間的最近距離等于
。則晶體內銅離子與氧離子間的最近距離等于![]() a=
a=![]() (cm);正確答案:
(cm);正確答案:![]() 。
。


 輕松課堂單元期中期末專題沖刺100分系列答案
輕松課堂單元期中期末專題沖刺100分系列答案科目:高中化學 來源: 題型:
【題目】已知:
2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ·mol-1
2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(l)ΔH=-1452 kJ·mol-1
H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1
下列說法正確的是 ( )
A. H2(g)的燃燒熱為571.6 kJ·mol-1
B. 同質量的H2(g)和CH3OH(l)完全燃燒,H2(g)放出的熱量多
C. ![]() H2SO4(aq)+
H2SO4(aq)+![]() Ba(OH)2(aq)===
Ba(OH)2(aq)===![]() BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1
BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1
D. 3H2(g)+CO2(g)=CH3OH(l)+H2O(l) ΔH=+135.9 kJ·mol-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25 ℃,有c(CH3COOH)+c(CH3COO-)=0.1 mol·L-1的一組醋酸和醋酸鈉混合溶液,溶液中c(CH3COOH)、c(CH3COO-)與pH的關系如圖所示。下列有關敘述不正確的是( )

A. pH=5.5溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-)
B. 由圖可知該溫度下醋酸的電離常數為1×10-4.75
C. pH=3.5溶液中:c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0.1 mol·L-1
D. 向1 LW點所表示溶液中通入0.05 mol HCl氣體(溶液體積變化可忽略):2c(H+)+c(CH3COOH)=c(CH3COO-)+2c(OH-)+2c(Cl-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】CO、CO2是化石燃料燃燒的主要產物。
(1)將含002molCO2和001molCO的混合氣體通入有足量Na2O2固體的密閉容器中,同時不斷地用電火花點燃,充分反應后,固體質量增加______g。
(2)已知:2CO(g)+O2(g)=2CO2(g) △H=-566.0kJ/mol,鍵能Eo-o=499.0kJ/mol。
①反應:CO(g)+O2(g)![]() CO2(g)+O(g)的△H=______kJ/mol。
CO2(g)+O(g)的△H=______kJ/mol。
②已知2500K時,①中反應的平衡常數為0.40,某時刻該反應體系中各物質濃度滿足:c(CO)·c(O2)=c(CO2) ·c(O),則此時v(正)_____(填“>""<"或"=”)v(逆)。
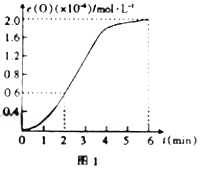
③已知1500℃時,在密閉容器中發生反應:CO2(g)![]() CO(g)+O(g)。反應過程中O(g)的物質的量濃度隨時間的變化如圖1所示,則0~2min內,CO2的平均反應速率v(CO2)=______。
CO(g)+O(g)。反應過程中O(g)的物質的量濃度隨時間的變化如圖1所示,則0~2min內,CO2的平均反應速率v(CO2)=______。
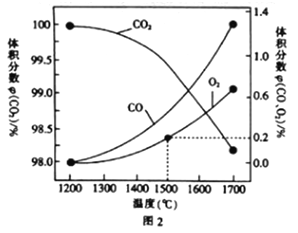
(3)在某密閉容器中發生反應:2CO2(g)![]() 2CO(g)+O2(g),1molCO2在不同溫度下的平衡分解量如圖2所示。
2CO(g)+O2(g),1molCO2在不同溫度下的平衡分解量如圖2所示。
①恒溫恒容條件下,能表示該可逆反應達到平衡狀態的有___(填字母).
A.CO的體積分數保持不變
B.容器內混合氣體的密度保持不變
C.容器內混合氣體的平均摩爾質量保持不變
D.單位時間內,消耗CO的濃度等于生成CO2的濃度
②分析圖2,若1500℃時反應達到平衡狀態,且容器體積為1L,則此時反應的平衡常數K=____(計算結果保留1位小數)。
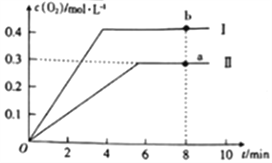
③向2L的恒容密閉容器中充入2molCO2(g),發生反應:2CO2(g)![]() 2CO(g)+O2(g),測得溫度為T℃時,容器內O2的物質的量濃度隨時間的變化如曲線II所示。圖中曲線I表示相對于曲線II僅改變一種反應條件后c(O2)隨時間的變化,則改變的條件是______;a、b兩點用CO濃度變化表示的凈反應速率關系為va(CO)_____(填“>”“<”或“=”)vb(CO)。
2CO(g)+O2(g),測得溫度為T℃時,容器內O2的物質的量濃度隨時間的變化如曲線II所示。圖中曲線I表示相對于曲線II僅改變一種反應條件后c(O2)隨時間的變化,則改變的條件是______;a、b兩點用CO濃度變化表示的凈反應速率關系為va(CO)_____(填“>”“<”或“=”)vb(CO)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)標準狀況下,22.4LH2的質量為____________g。
(2)9.8g H2SO4的物質的量為__________mol,約含有___________個氧原子。
(3)VL Fe2(SO4)3溶液中含有ag SO42-,取此溶液0.5L,用水稀釋至2VL,則稀釋后的溶液中Fe3+的物質的量濃度為_________mol/L。
(4)標準狀況下,16 g某氣態氧化物RO2的體積為5.6 L。該氣體的摩爾質量是________。
(5)b%的硫酸溶液與4b%的硫酸溶液等體積混合后,所得溶液的質量分數______(填 <、>或 = 下同)2.5b%。
(6)在某溫度時,一定量的元素A的氣態氫化物AH3,在一定體積的密閉容器中完全分解成兩種氣體單質,此時壓強增加了75%,則單質A的化學式為____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】歐美三位科學家因“分子機器的設計與合成”研究而榮獲2016年諾貝爾化學獎。納米分子機器研究進程中常見機器的“車輪”組件如下圖所示。下列說法正確的是

A. ①③互為同系物 B. ①②③④均屬于烴
C. ①④的一氯代物均為三種 D. ②④互為同分異構體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如下圖所示,裝置(I)是一種可充電電池,裝置(Ⅱ)為惰性電極的電解池。下列說法正確的是

A. 閉合開關K時,電極B為負極,且電極反應式為:2Brˉ-2eˉ=Br2
B. 裝置(I)放電時,總反應為:2Na2S2+Br2=Na2S4+2NaBr
C. 裝置(I)充電時,Na+從左到右通過陽離子交換膜
D. 該裝置電路中有0.1moleˉ通過時,電極Ⅹ上析出3.2gCu
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】計算并填空:(在標準狀況下15gCO與CO2的混合氣體,體積為11.2L,則:
(1)混合氣體的平均摩爾質量是 ___________________g/mol
(2)CO的體積分數是___________________
(3)CO2與CO的質量比是 ____________________________
(4)混合氣體中所含碳原子的質量是 ___________________ g
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各項敘述中,正確的是( )
A. 元素周期表每一周期元素原子的最外層電子排布均是從ns1 過渡到ns2np6
B. 若某基態原子的外圍電子排布為4d25s2,它是第五周期IVB族元素
C. M層全充滿而N層為4s1的原子和位于第四周期第ⅠA族的原子是同一種元素
D. 鈉原子由1s22s22p63s1→1s22s22p63p1時,原子釋放能量,由基態轉化成激發態
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com