
【題目】今有一混合物的水溶液,只可能含有以下離子中的若干種:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,現取三份100 mL溶液進行如下實驗:
(1)第一份加入AgNO3溶液有沉淀產生;
(2)第二份加足量NaOH溶液加熱后,收集到氣體0.04 mol;
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27 g,經足量鹽酸洗滌、干燥后,沉淀質量為2.33 g。根據上述實驗,以下推測正確的是
A.K+一定存在 B.100 mL溶液中含0.01 mol CO32-
C.Cl-一定不存在 D.Ba2+一定不存在,Mg2+可能存在
【答案】A
【解析】
試題分析:根據題意,Ba2+和SO42-,可發生離子反應生成BaSO4沉淀,因此兩者不能大量共存.Ba2+和CO32-可發生離子反應生成BaCO3沉淀,因此兩者也不能大量共存。第一份加入AgNO3溶液有沉淀產生,可能發生Cl-+Ag+═AgCl↓、CO32-+2Ag+═Ag2CO3↓、SO42-+2Ag+═Ag2SO4↓,所以可能含有Cl-、CO32-、SO42-;第二份加足量NaOH溶液加熱后,收集到氣體0.04mol,能和NaOH溶液加熱產生氣體的只能是NH4+,而沒有沉淀產生說明一定不存在Mg2+(Mg2+可以和OH-反應生產氫氧化鎂沉淀),故可確定一定含有NH4+,一定不存在Mg2+,根據反應NH4++OH-![]() NH3↑+H2O,產生NH3為0.04mol,可得NH4+也為0.04mol;第三份加足量BaCl2溶液后,得干燥沉淀6.27g,經足量鹽酸洗滌.干燥后,沉淀質量為2.33g.部分沉淀溶于鹽酸為BaCO3,部分沉淀不溶于鹽酸為BaSO4,發生反應CO32-+Ba2+═BaCO3↓、SO42-+Ba2+═BaSO4↓,因為BaCO3+2HCl═BaCl2+CO2↑+H2O而使BaCO3溶解.因此溶液中一定存在CO32-、SO42-,一定不存在Ba2+,由條件可知BaSO4為2.33g,物質的量為
NH3↑+H2O,產生NH3為0.04mol,可得NH4+也為0.04mol;第三份加足量BaCl2溶液后,得干燥沉淀6.27g,經足量鹽酸洗滌.干燥后,沉淀質量為2.33g.部分沉淀溶于鹽酸為BaCO3,部分沉淀不溶于鹽酸為BaSO4,發生反應CO32-+Ba2+═BaCO3↓、SO42-+Ba2+═BaSO4↓,因為BaCO3+2HCl═BaCl2+CO2↑+H2O而使BaCO3溶解.因此溶液中一定存在CO32-、SO42-,一定不存在Ba2+,由條件可知BaSO4為2.33g,物質的量為![]() =0.01mol,BaCO3為6.27g-2.33g═3.94g,物質的量為
=0.01mol,BaCO3為6.27g-2.33g═3.94g,物質的量為![]() =0.02mol,則CO32-物質的量為0.02mol,CO32-物質的量濃度為
=0.02mol,則CO32-物質的量為0.02mol,CO32-物質的量濃度為![]() =0.2mol/L,由上述分析可得,溶液中一定存在CO32-、SO42-、NH4+,一定不存在Mg2+、Ba2+.而CO32-、SO42-、NH4+物質的量分別為0.02mol、0.01mol、0.04mol,CO32-、SO42-所帶負電荷分別為0.02mol×2、0.01mol×2,共0.06mol,NH4+所帶正電荷為0.04mol,根據溶液中電荷守恒,可知K+一定存在,故A正確;由上述分析可得,BaCO3為6.27g-2.33g═3.94g,CO32-物質的量為0.02mol,故B錯誤;根據溶液中電荷守恒,可知K+一定存在,且K+物質的量≥0.02mol,當K+物質的量>0.02mol時,溶液中還必須存在Cl-.因此當K+物質的量═0.02mol,溶液中不存在Cl-,當K+物質的量>0.02mol時,溶液中一定存在Cl-,故C錯誤;溶液中一定存在CO32-、SO42-、NH4+,Ba2+和CO32-、SO42-可發生離子反應生成BaCO3↓、BaSO4↓而不共存,因此Ba2+一定不存在,同時第二份加足量NaOH溶液加熱后,收集到氣體,沒有產生沉淀,說明一定不含Mg2+,故D錯誤;故選A。
=0.2mol/L,由上述分析可得,溶液中一定存在CO32-、SO42-、NH4+,一定不存在Mg2+、Ba2+.而CO32-、SO42-、NH4+物質的量分別為0.02mol、0.01mol、0.04mol,CO32-、SO42-所帶負電荷分別為0.02mol×2、0.01mol×2,共0.06mol,NH4+所帶正電荷為0.04mol,根據溶液中電荷守恒,可知K+一定存在,故A正確;由上述分析可得,BaCO3為6.27g-2.33g═3.94g,CO32-物質的量為0.02mol,故B錯誤;根據溶液中電荷守恒,可知K+一定存在,且K+物質的量≥0.02mol,當K+物質的量>0.02mol時,溶液中還必須存在Cl-.因此當K+物質的量═0.02mol,溶液中不存在Cl-,當K+物質的量>0.02mol時,溶液中一定存在Cl-,故C錯誤;溶液中一定存在CO32-、SO42-、NH4+,Ba2+和CO32-、SO42-可發生離子反應生成BaCO3↓、BaSO4↓而不共存,因此Ba2+一定不存在,同時第二份加足量NaOH溶液加熱后,收集到氣體,沒有產生沉淀,說明一定不含Mg2+,故D錯誤;故選A。


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
【題目】在密閉容器中進行可逆反應,A跟B反應生成C,反應速率v(A)、v(B)、v(C)之間存在以下關系:v(B)=3v(A),v(c)=2v(A),3v(C)=2v(B)則該反應可以表示為( )
A. A+BC B. 2A+2B3C C. A+3B2C D. 3A+B2C
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學與生產、生活密切相關,下列說法正確的是
A.利用糧食釀酒經歷了淀粉→葡萄糖→乙醇的化學變化過程
B.淀粉、油脂和蛋白質都是高分子化合物
C.煤經過氣化和液化等物理變化可轉化為清潔燃料
D.聚氯乙烯塑料薄膜可用作食品保鮮膜、一次性食品袋等
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表中a、b、c表示相應儀器中加入的試劑,可用如圖裝置制取、凈化、收集的氣體是:
選項 | 氣體 | a | b | c |
|
A | NH3 | 濃氨水 | 生石灰 | 堿石灰 | |
B | CO2 | 鹽酸 | 碳酸鈣 | 飽和NaHCO3溶液 | |
C | NO | 稀硝酸 | 銅屑 | H2O | |
D | Cl2 | 濃鹽酸 | 二氧化錳 | 飽和NaCl溶液 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列反應的離子方程式書寫正確的是( )
A. 鐵粉溶于稀鹽酸:2Fe+6H+=2Fe3++3H2↑
B. 碳酸鈣溶于稀鹽酸:CO32-+2H+=CO2↑+H2O
C. 氧化銅溶于醋酸:CuO+2CH3COOH =Cu2+ +2CH3COO- +H2O
D. 硫酸銅與氫氧化鋇溶液混合:Ba2++SO42-=BaSO4 ↓
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】⑴合理膳食、均衡營養是保證人體健康和生活質量的重要途徑。
① 人體必需的元素攝入不足會影響人體的正常生理活動。下列做法不能達到目的的是 。
a.補碘——食用加碘鹽
b.補鐵——使用鐵強化醬油
c.補鈣——服用葡萄糖
② 人體內有8種氨基酸必需通過食物攝入,某品牌餅干含有的下列物質中能轉化為氨基酸的是 。
a.纖維素 b.蛋白質 c.油脂
③ 人類歷史上最重要的抗生素是 。
a. 青霉素 b.維生素 c.胡蘿卜素
⑵ 構建人與自然的和諧、營造安全的生態環境已成為全人類的共識。
① 如圖Ⅰ,向兩只250mL的錐形瓶中分別充入CO2和空氣,用白熾燈泡照射一段時間后,其中a瓶中溫度計讀數稍低,則盛放CO2的錐形瓶為 (填“a”或“b”)。

圖Ⅰ 圖Ⅱ
② 為防止白色污染,廢舊的塑料需投入到貼有圖II標志的垃圾桶內,該標志表示的是 。
③ 廢水中鉈(Tl)具有高毒性,治理時常加入NaClO溶液,將Tl+轉變為Tl3+,NaClO作
(填“氧化劑”或“還原劑”),同時加入適量氨水,將Tl3+轉變為難溶物Tl(OH)3,寫出生成Tl(OH)3的離子方程式 。
⑶ 材料是人類社會發展的物質基礎,材料科學的發展離不開化學。
① 黏土是陶瓷的生產原料,其中江蘇宜興的高嶺土是含有雜質較少的高品質黏土,其主要組成可表示為Al2Si2Ox(OH)4,則x= 。
② 2016年奧運會在巴西舉行,場館的建設需大量的建筑材料。其中生產水泥、玻璃共同的原料是 (填名稱),場館內的座椅通常用高密度聚乙烯(HDPE)為原料制得,聚乙烯屬于 塑料(填“熱固性”或“熱塑性”)。
③ 滬通鐵路建設正在積極推進,其中如何防止鐵軌的腐蝕是工程技術人員攻克的難題之一。鐵在發生電化學腐蝕時的負極反應方程式為 。
④ 工業上常用SiCl4與O2在高溫條件下通過置換反應制得SiO2,并于2000℃下拉成光纖細絲。該反應的化學方程式為 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在處于化學平衡狀態的體系中,如果下列量發生變化,其中一定能表明化學平衡移動的是
A.反應混合物的濃度
B.反應體系的壓強
C.正、逆反應的速率
D.反應物的轉化率
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:pOH= -lgc(OH-)。298 K時,向20.00 mL0.10mol·L-1氨水中滴入0.10 mol·L-1的鹽酸,溶液的pH和pOH與加入鹽酸體積關系如圖所示。下列說法正確的是
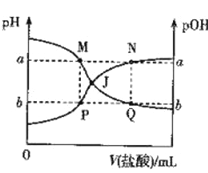
A. 曲線PJN表示溶液中PH的變化
B. M點水的電離程度比Q點大
C. M、P兩點的數值之和a + b = 14
D. pH與pOH交叉點J對應的V(鹽酸)=20.00 mL
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com