
【題目】在水溶液中能大量共存的一組離子是
A. NH4+、CH3COO-、Na+、H+ B. AlO2-、Na+、K+、HCO3-
C. Mg2+、Na+、SO42-、NO3- D. ClO-、Na+、K+、Fe2+
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】堿式碳酸銅是一種用途廣泛的化工原料,明礬是種常見的凈水劑,某校化學興趣小組探究將一廢棄礦石進行處理制備堿式碳酸銅和明礬,從而實現變廢為寶。經查資料:該礦石成分為:Al2Fe4CuSi2O13,該化學小組制定工藝流程如下:

己知:Cu2+溶于足量的濃氨水中可形成銅氨溶液:Cu2++4NH3·H2O![]() Cu(NH3)42++4H2O
Cu(NH3)42++4H2O
回答下列問題:
(1)將Al2Fe4CuSi2O13改寫成氧化物形式___________;
(2)為了步驟②提高酸浸速率,可采取措施有________,_________(任寫兩種);
(3)寫出步驟⑥的離子方程式__________;
(4)用從濾渣2到明礬需先后加入_____、____兩種試劑(按使用順序填寫化學式);
(5)在步驟⑦中,若先加K2CO3溶液,后加KOH溶液,則易發生
CuCO3(s)+2OH-(aq) ![]() Cu(OH)2(s)+CO32-(aq),則該反應平衡常數為:______。(已知:Ksp(CuCO3=2.4×10-10,Ksp(Cu(OH)2=2.2×10-20)。
Cu(OH)2(s)+CO32-(aq),則該反應平衡常數為:______。(已知:Ksp(CuCO3=2.4×10-10,Ksp(Cu(OH)2=2.2×10-20)。
(6)為了檢驗該堿式碳酸銅純度,該小組稱取25g樣品,加入到100mL 3mol/L的鹽酸中進行溶解。充分反應后,微熱排除CO2,冷卻后取出10mL,滴加2滴甲基橙,然后用2mol/L標準KOH溶液進行滴定,共用去5mL。則樣品的純度為_________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】從環己烷可制備1,4—環己二醇的二醋酸酯。下面是有關的8步反應(其中所有無機物都已略去):

其中有3步屬于取代反應,2步屬于消去反應,3步屬于加成反應。
(1)屬于取代反應是______________,屬于加成反應是_______________(填反應序號)。
(2)B、D的結構簡式分別為:B________________,D___________________。
(3)寫出第2步的反應方程式 ________________________________________________ 。
(4)有三種不同的基團,分別為—X、—Y、—Z,若同時分別取代苯環上的三個氫原子,能生成的同分異構體數目是 _____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】O2、CH4和CO的混合氣體在標準狀況下的密度為1.25g/L,這三種氣體的物質的量之比不可能為( )
A. 3:1:2 B. 6:2:3 C. 3:4:6 D. 9:3:7
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用接觸法制5t98%的濃硫酸,在理論上需要含FeS2 75%(雜質不含硫元素)的硫鐵礦為 ( )
A. 4.3t B. 8t C. 4t D. 5.6t
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是( )
A. 可用酸性高錳酸鉀溶液檢驗丙烯醛中是否含有碳碳雙鍵
B. 分子式為CH4O和C2H6O的物質一定互為同系物
C. 乙烯和苯都能與溴水發生反應而使其褪色
D. 甲苯苯環上的一個氫原子被含3個碳原子的烷基取代,所得產物有6種
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】堿性鋅錳電池是日常生活中消耗量最大的電池,其構造如圖所示。
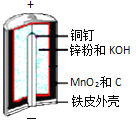
放電時總反應為:Zn + 2H2O + 2MnO2![]() Zn(OH)2 + 2MnOOH
Zn(OH)2 + 2MnOOH
從廢舊堿性鋅錳電池中回收Zn和MnO2的工藝如下:
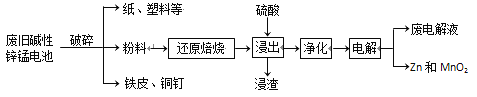
回答下列問題:
(1)MnOOH中,Mn元素的化合價為________。
(2)“還原焙燒”過程中,高價金屬化合物被還原為低價氧化物或金屬單質(其中MnOOH、MnO2被還原成MnO),主要原因是“粉料”中含有________。
(3)“凈化”是為了除去浸出液中的Fe2+,方法是:加入________(填化學式)溶液將Fe2+氧化為Fe3+,再調節pH使Fe3+完全沉淀。(離子濃度小于1×10-5mol·L-1即為沉淀完全)已知浸出液中Mn2+、Zn2+的濃度約為0.1 mol·L-1,根據下列數據計算調節pH的合
理范圍是________至________。
化合物 | Mn(OH)2 | Zn(OH)2 | Fe(OH)3 |
KSP近似值 | 10-13 | 10-17 | 10-38 |
(4)“電解”時,陽極的電極反應式為_____。本工藝中應循環利用的物質是_____(填化學式)。
(5)若將“粉料”直接與鹽酸共熱反應后過濾,濾液的主要成分是ZnCl2和MnCl2。“粉料”中的MnOOH與鹽酸反應的化學方程式為________。
(6)某堿性鋅錳電池維持電流強度0.5A(相當于每秒通過5×10-6 mol電子),連續工作80分鐘即接近失效。如果制造一節電池所需的鋅粉為6 g,則電池失效時仍有________%的金屬鋅未參加反應。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學與生產、生活、社會發展等息息相關。下列說法正確的是( )
A. 做衣服的棉、麻、絲綢灼燒有燒焦羽毛的氣味
B. 糖尿病人應少吃含糖類的食品,可常喝糯米八寶粥
C. 現代工業生產中的芳香烴來源于石油的催化重整和煤的干餾
D. 豆漿中富含大豆蛋白,煮沸后蛋白質即水解生成氨基酸
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】離子方程式BaCO3 + 2H+ = CO2↑ + H2O + Ba2+ 中的H+不能代表的物質是( )
①HCl;②H2SO4;③HNO3;④NaHSO4;⑤CH3COOH
A.①③ B.①④⑤ C.②④⑤ D.①⑤
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com