
 4NO(g)+ 6H2O(g)△H<0。有關(guān)該反應(yīng)的說法正確的是
4NO(g)+ 6H2O(g)△H<0。有關(guān)該反應(yīng)的說法正確的是| A.反應(yīng)達(dá)到平衡后,3ν正(NH3)=2ν逆(H2O) |
| B.反應(yīng)處于平衡狀態(tài)時(shí),c(NH3)·c(O2)=c(NO)·c(H2O) |
| C.其它條件不變,溫度越高,氨的轉(zhuǎn)化率越高 |
| D.增大壓強(qiáng)是加快反應(yīng)速率并提高NO產(chǎn)率的有效措施 |
 閱讀快車系列答案
閱讀快車系列答案
| 年級(jí) | 高中課程 | 年級(jí) | 初中課程 |
| 高一 | 高一免費(fèi)課程推薦! | 初一 | 初一免費(fèi)課程推薦! |
| 高二 | 高二免費(fèi)課程推薦! | 初二 | 初二免費(fèi)課程推薦! |
| 高三 | 高三免費(fèi)課程推薦! | 初三 | 初三免費(fèi)課程推薦! |
科目:高中化學(xué) 來源:不詳 題型:單選題
A.在溴水中存在如下平衡:Br2+H2O  HBr+HBrO當(dāng)加入NaOH溶液后顏色變淺 HBr+HBrO當(dāng)加入NaOH溶液后顏色變淺 |
B.對(duì)   平衡體系增加壓強(qiáng)使顏色變深 平衡體系增加壓強(qiáng)使顏色變深 |
C.反應(yīng)  CO2+NO△H<0升高溫度使平衡向逆方向移動(dòng) CO2+NO△H<0升高溫度使平衡向逆方向移動(dòng) |
D.合成氨反應(yīng):   ,△H<0 為使氨的產(chǎn)率提高,理論上應(yīng)采取低溫高壓的措施 ,△H<0 為使氨的產(chǎn)率提高,理論上應(yīng)采取低溫高壓的措施 |
查看答案和解析>>
科目:高中化學(xué) 來源:不詳 題型:單選題
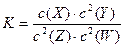 ,有關(guān)該平衡體系的說法正確的是 ( )
,有關(guān)該平衡體系的說法正確的是 ( )| A.升高溫度,平衡常數(shù)K一定增大 |
| B.增大壓強(qiáng),W(g)質(zhì)量分?jǐn)?shù)增加 |
C.該反應(yīng)的化學(xué)反應(yīng)方程式為X+2Y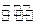 2Z+2W 2Z+2W |
| D.增大X(g)濃度,平衡向逆反應(yīng)方向移動(dòng) |
查看答案和解析>>
科目:高中化學(xué) 來源:不詳 題型:單選題
 2NO2(g);(△H>0)在密閉容器中達(dá)到平衡.下列說法不正確的是
2NO2(g);(△H>0)在密閉容器中達(dá)到平衡.下列說法不正確的是| A.加壓時(shí)(體積變小),將使正反應(yīng)速率增大 |
| B.保持體積不變,加入少許NO2,將使正反應(yīng)速率減小 |
| C.保持體積不變,加入少許N2O4,再達(dá)平衡時(shí)顏色變深 |
| D.保持體積不變,升高溫度,再達(dá)平衡時(shí)顏色變深 |
查看答案和解析>>
科目:高中化學(xué) 來源:不詳 題型:單選題
 R(g)+S(g)在體積和溫度不變的密閉容器中進(jìn)行。下列事實(shí)中,可作為反應(yīng)達(dá)到化學(xué)平衡狀態(tài)的標(biāo)志的是。
R(g)+S(g)在體積和溫度不變的密閉容器中進(jìn)行。下列事實(shí)中,可作為反應(yīng)達(dá)到化學(xué)平衡狀態(tài)的標(biāo)志的是。| A.單位時(shí)間內(nèi)生成n mol Q的同時(shí)生成n mol R |
| B.單位時(shí)間內(nèi)生成n mol R 的同時(shí)生成n mol S |
| C.反應(yīng)器內(nèi)P、Q、R、S四種氣體物質(zhì)的量濃度相等 |
| D.反應(yīng)器內(nèi)P、Q、R、S四種氣體共存 |
查看答案和解析>>
科目:高中化學(xué) 來源:不詳 題型:單選題
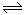 2NH3,下列不能說明反應(yīng)已平衡的是:
2NH3,下列不能說明反應(yīng)已平衡的是:| A.容器內(nèi)的壓強(qiáng)不變 | B.單位時(shí)間內(nèi),消耗1 mol N2的同時(shí),生成2 molNH3 |
| C.混合氣體的相對(duì)分子質(zhì)量不變 | D.混合物的總物質(zhì)的量不變 |
查看答案和解析>>
科目:高中化學(xué) 來源:不詳 題型:單選題
 2Z(g);△H<0,下列有關(guān)該反應(yīng)的說法中
2Z(g);△H<0,下列有關(guān)該反應(yīng)的說法中 正確的是 ( )
正確的是 ( )| A.該反應(yīng)的正反應(yīng)為吸熱反應(yīng) |
| B.當(dāng)各物質(zhì)濃度不再變化時(shí),反應(yīng)達(dá)到平衡狀態(tài) |
| C.若溫度不變,平衡后把容器的體積增大一倍,平衡將不移動(dòng) |
| D.若升高溫度,平衡向正反應(yīng)的方向移動(dòng) |
查看答案和解析>>
科目:高中化學(xué) 來源:不詳 題型:單選題
| 弱酸化學(xué)式 | CH3COOH | HCN | H2S |
| 電離常數(shù)(25℃) | 1.8×10-5 | 4.9×10-10 | K1= 1.3×10-7 K2= 7.1×10-15 |
| A.等物質(zhì)的量濃度的各溶液pH關(guān)系為:pH(CH3COONa)>pH(Na2S)>pH(NaCN) |
| B. a mol/L HCN溶液與b mol/L NaOH溶液等體積混合,所得溶液中c(Na+)> c(CN-),則a一定大于b |
| C. NaHS和Na2S混合溶液中,一定存在c(Na+)+ c(H+)="=" c(OH-)+ c(HS-)+2c(S2-) |
| D.某濃度HCN的水溶液pH=d,則其中c(OH-)=10-d mol/L |
查看答案和解析>>
科目:高中化學(xué) 來源:不詳 題型:填空題
 xC(g),△H<0;在2min時(shí)反應(yīng)達(dá)到平衡狀態(tài)(溫度不變)剩余了0.8molB,并測(cè)得C的濃度為0.4mol·L—1,請(qǐng)?zhí)顚懴铝锌瞻祝?br />(1)從開始反應(yīng)至達(dá)到平衡狀態(tài),生成B的平均反應(yīng)速率為 。
xC(g),△H<0;在2min時(shí)反應(yīng)達(dá)到平衡狀態(tài)(溫度不變)剩余了0.8molB,并測(cè)得C的濃度為0.4mol·L—1,請(qǐng)?zhí)顚懴铝锌瞻祝?br />(1)從開始反應(yīng)至達(dá)到平衡狀態(tài),生成B的平均反應(yīng)速率為 。 3)若繼續(xù)向原平衡混合物的容器中通入少量氦氣(假設(shè)氦氣和A、B、C都不反應(yīng))后,化學(xué)平衡(填字母) 。
3)若繼續(xù)向原平衡混合物的容器中通入少量氦氣(假設(shè)氦氣和A、B、C都不反應(yīng))后,化學(xué)平衡(填字母) 。查看答案和解析>>
國際學(xué)校優(yōu)選 - 練習(xí)冊(cè)列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報(bào)平臺(tái) | 網(wǎng)上有害信息舉報(bào)專區(qū) | 電信詐騙舉報(bào)專區(qū) | 涉歷史虛無主義有害信息舉報(bào)專區(qū) | 涉企侵權(quán)舉報(bào)專區(qū)
違法和不良信息舉報(bào)電話:027-86699610 舉報(bào)郵箱:58377363@163.com