
Cu—Zn稀硫酸組成原電池裝置,當導線中有0.5mol電子通過時,理論上兩極的變化是
①鋅極反應:Zn-2e-=Zn2+,鋅片上產生0.25mol的H2
②銅極反應:2H++2e-=H2↑,鋅片溶解16.25g
③電流由銅極經導線流向鋅極 ④溶液中SO42-移向銅極
| A.①④ | B.③④ | C.②③ | D.①③ |
 尖子生新課堂課時作業系列答案
尖子生新課堂課時作業系列答案 英才計劃同步課時高效訓練系列答案
英才計劃同步課時高效訓練系列答案科目:高中化學 來源: 題型:實驗題
用0.1320 mol/L的HCl溶液滴定未知濃度的NaOH溶液,實驗數據如下表所示,
| 實驗編號 | 待測NaOH溶液的體積/mL | HCl溶液的體積/mL |
| 1 | 25.00 | 24.41 |
| 2 | 25.00 | 24.39 |
| 3 | 25.00 | 22.60 |

查看答案和解析>>
科目:高中化學 來源: 題型:單選題
用石墨電極電解CuCl2溶液(見下圖)。下列分析正確的是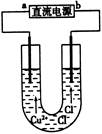
| A.a端是直流電源的負極 |
| B.通電使CuCl2發生電離 |
| C.陽極上發生的反應:Cu2++2e-=Cu |
| D.通電一段時間后,在陰極附近觀察到黃綠色氣體 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
原電池反應是釋放能量的氧化還原反應,下列可設計成原電池的化學反應是
| A.H2O (l)+CaO(s) =Ca(OH)2(s) | B.Ba(OH)2·8H2O+2NH4Cl=BaCl2+2NH3·H2O+8H2O |
C.2KClO3 2KCl+3O2↑ 2KCl+3O2↑ | D.CH4(g)+2O2(g)=CO2(g)+2H2O(l) |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
關于下圖的說法正確的是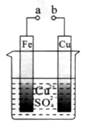
| A.構成原電池時Cu是負極 |
| B.構成電解池時Cu是陰極 |
| C.構成電解池時質量增重的極是陰極 |
D.電池工作時溶液中的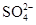 一定移向Cu極 一定移向Cu極 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
關于下圖所示裝置(鹽橋含KCl)的敘述,正確的是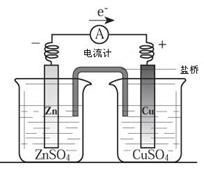
| A.銅離子在銅片表面被氧化 |
| B.銅作陽極,銅片上有氣泡產生 |
| C.電流從鋅片經導線流向銅片 |
| D.右側燒杯中,SO42-的物質的量幾乎不變,K+的數目增多 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
熔融鹽燃料電池具有高的發電效率,因而受到重視。用Li2CO3和Na2CO3的熔融鹽混合物作電解質,一極通CO氣體,另一極通O2和CO2混合氣體,可制得在650℃下工作的燃料電池。已知該電池總反應為:2CO+O2=2CO2。則下列說法中正確的是( )
| A.通CO的一極是電池的正極 |
| B.該電池工作過程中需不斷補充CO和O2,CO2可循環利用 |
| C.負極反應式為:O2+2CO2+4e-==2CO32- |
| D.正極反應式為:2CO+2CO32-—4e-==4CO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
汽車的啟動電源常用鉛蓄電池,該電池在放電時的反應如下:
Pb (s)+ PbO2(s) +2H2SO4(aq) 2PbSO4(s) +2H2O(l),根據此反應判斷下列敘述中正確的是( )
2PbSO4(s) +2H2O(l),根據此反應判斷下列敘述中正確的是( )
| A.PbO2是電池的負極 |
| B.負極的電極反應式為:Pb(s)+SO42-(aq)–2e – = PbSO4(s) |
| C.鉛蓄電池屬于一次電池 |
| D.電池放電時,溶液酸性增強 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下圖所示的電解池I和II中,a、b、c和d均為Pt電極。電解過程中,電極b和d上沒有氣體逸出,但質量均增大,且增重b<d。符合上述實驗結果的鹽溶液是
| 選項 | X | Y |
| A. | MgSO4 | CuSO4 |
| B. | AgNO3 | Pb(NO3)2 |
| C. | FeSO4 | Al2 (SO4)3 |
| D. | CuSO4 | AgNO3 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com