
【題目】(1)有機物的結構可用“鍵線式”簡化表示。如CH3—CH=CH-CH3可簡寫為![]() ,若有機物X的鍵線式為:
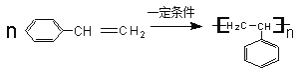
,若有機物X的鍵線式為: ![]() ,則該有機物的分子式為_______,其二氯代物有_______種;Y是X的同分異構體,分子中含有1個苯環,寫出Y的結構簡式________。Y在一定條件下發生加聚反應,寫出其反應的化學方程式:______________________________________。
,則該有機物的分子式為_______,其二氯代物有_______種;Y是X的同分異構體,分子中含有1個苯環,寫出Y的結構簡式________。Y在一定條件下發生加聚反應,寫出其反應的化學方程式:______________________________________。
(2)以乙烯為原料合成化合物C的流程如下所示:
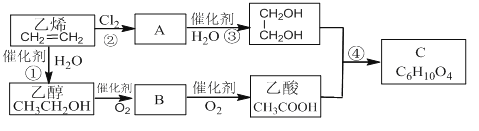
a A和B中所含官能團的名稱分別為________和________。
b B物質的結構簡式為________。
c ① 、④的反應類型分別為________和________。
d 反應②和④的化學方程式分別為:
②______________________________________________________。
④______________________________________________________。
【答案】C8H8 3 ![]()
 氯原子 醛基 CH3CHO 加成反應 取代反應(或酯化反應) CH2=CH2 + Cl2 → CH2ClCH2Cl HOCH2CH2OH + 2 CH3COOH
氯原子 醛基 CH3CHO 加成反應 取代反應(或酯化反應) CH2=CH2 + Cl2 → CH2ClCH2Cl HOCH2CH2OH + 2 CH3COOH ![]()
![]() CH3COOCH2CH2OOCCH3 + 2 H2O
CH3COOCH2CH2OOCCH3 + 2 H2O
【解析】
根據分子的對稱性判斷二氯代物的數目,由分子結構特征推斷其結構。根據合成流程圖中已知物的結構、反應條件等,確定未知物的結構。
(1)按題中“鍵線式”書寫示例,有機物X(![]() )的轉折點都有碳原子,又據碳原子四價原則每個碳原子都連接1個氫原子,該有機物的分子式為C8H8;因分子中心對稱,8個氫原子完全相同,故其一氯代物只有1種,二氯代物有3種(棱邊、面對角、體對角)。Y與X同分異構,分子式也是C8H8,含有1個苯環時可表示為C6H5-C2H3,則結構簡式為
)的轉折點都有碳原子,又據碳原子四價原則每個碳原子都連接1個氫原子,該有機物的分子式為C8H8;因分子中心對稱,8個氫原子完全相同,故其一氯代物只有1種,二氯代物有3種(棱邊、面對角、體對角)。Y與X同分異構,分子式也是C8H8,含有1個苯環時可表示為C6H5-C2H3,則結構簡式為![]() ;加聚反應的化學方程式:
;加聚反應的化學方程式: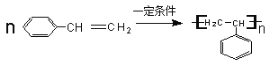 。
。
(2)乙烯(CH2=CH2)經反應②③生成乙二醇(HOCH2CH2OH),碳碳雙鍵變成單鍵、單官能團變成雙官能團,則A為ClCH2CH2Cl;乙醇經兩次氧化生成乙酸,則B為乙醛(CH3CHO);C是乙二醇與乙酸酯化反應生成的,結構簡式為![]() 。
。
a.A和B官能團分別是氯原子、醛基。
b.B的結構簡式為CH3CHO。
c.①、④分別為加成反應和取代反應(酯化反應)。
d.反應②和④的化學方程式分別為:
②CH2=CH2 + Cl2 → CH2ClCH2Cl。
④HOCH2CH2OH + 2CH3COOH ![]() CH3COOCH2CH2OOCCH3 + 2H2O。
CH3COOCH2CH2OOCCH3 + 2H2O。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】ClO2是一種黃綠色或橙黃色的氣體,極易溶于水,可用于水的消毒殺菌、水體中Mn2+等重金屬清除及煙氣的脫硫脫硝。回答下列問題:
(1)將過硫酸鈉(Na2S2O8)溶液加入亞氯酸鈉(NaClO2)中可制備ClO2,該反應中氧化劑和還原劑的物質的量之比為_____。
(2)將ClO2通入MnSO4溶液,溶液中可檢測到Cl-同時有黑色沉淀生成。該反應的離子方程式為__________。
(3)為研究ClO2脫硝的適宜條件,在1L200 mgL-1 ClO2溶液中加NaOH溶液調節pH,通入NO氣體并測定NO的去除率,脫硝后N元素以NO3-形式存在,其關系如下圖所示:
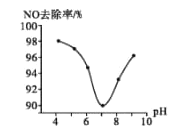
①實驗中使用的ClO2溶液的物質的量濃度為______(保留三位有效數字);要使NO的去除率更高,應控制的條件是_________。
②當溶液pH>7時,NO的去除率增大的原因是ClO2與NaOH溶液反應可生成更強的吸收劑NaClO2,寫出堿性條件下NaClO2脫除NO反應的離子方程式:_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學反應2CaO2(s) ![]() 2CaO(s) + O2(g) 在一密閉的容器中達到平衡。保持溫度不變,縮小容器的容積為原來的一半,重新平衡后,下列敘述正確的是
2CaO(s) + O2(g) 在一密閉的容器中達到平衡。保持溫度不變,縮小容器的容積為原來的一半,重新平衡后,下列敘述正確的是
A. CaO2的量不變B. 平衡常數減小C. 氧氣濃度變小D. CaO的量減少
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫度下,將Cl2緩慢通入水中至飽和,然后再滴加0.1mol/L的NaOH溶液,整個過程中溶液的pH變化曲線如圖所示。下列選項正確的是
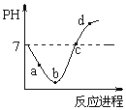
A. a點時,已經滴入NaOH溶液
B. b點所示的溶液中,只存在兩種分子
C. a、b、c、d四個點中,c點水的電離程度最大
D. d點所示的溶液中,鈉元素與氯元素的物質的量相等
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有以下物質①石墨;②鈉;③酒精;④氨氣;⑤硫化氫;⑥碳酸氫鈉固體;⑦氫氧化鋇溶液;⑧純醋酸;⑨氧化鈉固體;⑩液態氯化氫。
(1)其中能導電的是_______;屬于非電解質的是_________。
(2)等質量④和⑤中氫原子的數目之比為_____;若④和⑤中所含氫原子數相等,則④和⑤的質量之比為________。
(3)寫出⑥和⑧在水溶液中的離子反應方程式____________________________。
(4)室溫下,某容積固定的密閉容器由可移動的活塞隔成A、B兩,分別向A、B兩室充入H2、O2的混合氣體和1mol空氣,此時活塞的位置如圖所示。
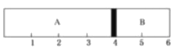
①A室混合氣體所含分子總數約為______________(填數值)
②實驗測得A室混合氣體的質量為34g,則該混合氣體的密度是同溫同壓下氫氣密度的______倍。
③若將A室H2、O2的混合氣體點燃,恢復原溫度后,最終活塞停留的位置在______刻度處。
(5)在標準狀況下,1L2mol/L氫氧化鈉溶液中通入33.6L二氧化碳氣體充分反應,所得溶液溶質的成分是____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對利用甲烷消除NO2污染進行研究,CH4+2NO2 ![]() N2+CO2+2H2O。在1L密閉容器中,控制不同溫度,分別加入0.50molCH4和1.2molNO2,測得n(CH4)隨時間變化的有關實驗數據見下表。
N2+CO2+2H2O。在1L密閉容器中,控制不同溫度,分別加入0.50molCH4和1.2molNO2,測得n(CH4)隨時間變化的有關實驗數據見下表。
組別 | 溫度 | 時間/min n/mol | 0 | 10 | 20 | 40 | 50 |
① | T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
② | T2 | n(CH4) | 0.50 | 0.30 | 0.18 | … | 0.15 |
下列說法正確的是
A. 組別①中,0~20min內,NO2的降解速率為0.0125 mol·L-1·min-1
B. 由實驗數據可知實驗控制的溫度T12
C. 40min時,表格中T2應填的數據為0.18
D. 0~10min內,CH4的降解速率①>②
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有600 mL某種混合物溶液,只可能含有以下離子中的若干種:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,現將此溶液分成三等份,進行如下實驗:
(1)向第一份中加入AgNO3溶液,有沉淀產生;
(2)向第二份中加足量NaOH溶液并加熱后,收集到氣體0.04 mol;
(3)向第三份中加足量BaCl2溶液后,得干燥的沉淀6.27g,經足量鹽酸洗滌、干燥后,沉淀質量為2.33g。 根據上述實驗現象,以下推測正確的是
A. K+不一定存在 B. Ba2+、Mg2+不一定都存在
C. Cl-不一定存在 D. 混合溶液中CO32-的濃度為0.2 mol/L
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)下列選項中互為同系物的是__________;互為同分異構體的是__________;屬于同種物質的是__________。
①H2O與D2O;②1H、2H、3H;③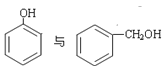 ;④
;④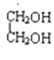 與
與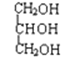 ;⑤
;⑤ ![]() ;⑥戊烯與環戊烷; ⑦
;⑥戊烯與環戊烷; ⑦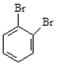 與
與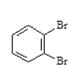
(2)羥基、羧基的性質具有明顯的差異,為實現如圖所示的各步轉化,請在括號內填入適當試劑的化學式。
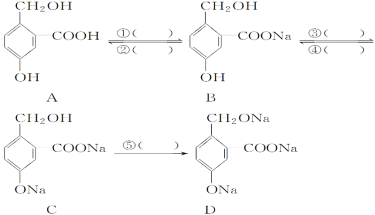
①__________;②__________;③__________;④__________;⑤__________;
(3)聚碳酸酯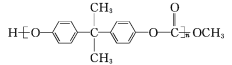 的透光率良好,可制作車、船、飛機的擋風玻璃等。①原來合成聚碳酸酯的一種原料是有毒的光氣(COCl2),現在改用綠色化學原料碳酸二甲酯(
的透光率良好,可制作車、船、飛機的擋風玻璃等。①原來合成聚碳酸酯的一種原料是有毒的光氣(COCl2),現在改用綠色化學原料碳酸二甲酯(![]() )與____(填序號)縮合聚合而成。
)與____(填序號)縮合聚合而成。
A.二鹵代物 B.二酚類 C.二醛類 D.二烯類
②寫出用綠色化學原料合成聚碳酸酯反應的化學方程式____________________________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】40 ℃時,在氨-水體系中不斷通入CO2,各種離子的變化趨勢如下圖所示。下列說法不正確的是
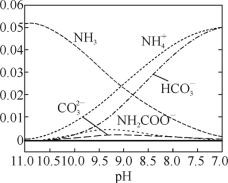
A. 在pH=9.0時,c(NH4+)>c(HCO3-)>c(NH2COO-)>c(CO32-)
B. 隨著CO2的通入,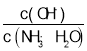 不斷增大
不斷增大
C. 不同pH的溶液中存在關系:c(NH4+)+c(H+)=c(CO32-)+c(HCO3-)+c(NH2COO-)+c(OH-)
D. 在溶液pH不斷降低的過程中,有含NH2COO-的中間產物生成
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com