
【題目】根據如圖所示裝置(部分儀器已略去)回答下列有關問題。
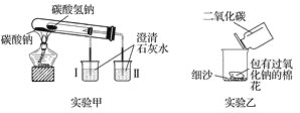
(1)實驗甲在加熱過程中能觀察到產生白色沉淀的燒杯是________(填“Ⅰ”或“Ⅱ”),該燒杯中發生反應的離子方程式是________,通過實驗甲可證明______(填“Na2CO3”或“NaHCO3”)更穩定。
(2)實驗乙用來探究Na2O2與CO2的反應,觀察到的實驗現象為包有Na2O2的棉花著火。寫出Na2O2與CO2反應的化學方程式:_________,棉花著火說明該反應的特點是_________
(3)取10 g碳酸鈉和碳酸氫鈉的混合物充分加熱,將生成的CO2氣體通入足量的澄清石灰水中,測得生成沉淀的質量為4.0 g。則原混合物中碳酸鈉的質量分數為_________。
【答案】Ⅱ Ca2++2OH-+CO2===CaCO3↓+H2O Na2CO3 2Na2O2+2CO2===2Na2CO3+O2 放出大量的熱 32.8%
【解析】
(1)碳酸氫鈉不穩定,易分解成二氧化碳、碳酸鈉和水,而碳酸鈉不分解更加穩定,則甲圖中可觀察到與小試管相連的燒杯Ⅱ中變渾濁,該燒杯中發生反應的離子方程式是Ca2++2OH-+CO2===CaCO3↓+H2O,則由甲圖可比較二者的熱穩定性,故答案為:Ⅱ;Ca2++2OH-+CO2===CaCO3↓+H2O;Na2CO3;
(2)包有Na2O2的棉花著火燃燒,則Na2O2與CO2的反應為放熱反應,且生成氧氣,則該反應為2Na2O2+2CO2═2Na2CO3+O2,說明反應能放出大量的熱;
(3)根據反應關系式:2NaHCO3~CO2~CaCO3,n(CaCO3)= ![]() =0.04mol,原混合物中碳酸氫鈉的質量為:n(NaHCO3)= 2n(CaCO3)=0.08mol,m(NaHCO3)=nM=0.08mol×84g/mol=6.72g,原混合物中碳酸鈉的質量分數為:w(Na2CO3)=
=0.04mol,原混合物中碳酸氫鈉的質量為:n(NaHCO3)= 2n(CaCO3)=0.08mol,m(NaHCO3)=nM=0.08mol×84g/mol=6.72g,原混合物中碳酸鈉的質量分數為:w(Na2CO3)=![]() ×100%=32.8%,故原混合物中碳酸鈉的質量分數為32.8%。
×100%=32.8%,故原混合物中碳酸鈉的質量分數為32.8%。


 名師指導期末沖刺卷系列答案
名師指導期末沖刺卷系列答案 開心蛙口算題卡系列答案
開心蛙口算題卡系列答案科目:高中化學 來源: 題型:
【題目】設NA表示阿伏加德羅常數,下列敘述中正確的是( )
A.常溫常壓下,11.2L二氧化碳含有的原子數等于1.5NA
B.標準狀況下,22.4LCCl4中所含分子數為NA
C.標準狀況下,18g水所含原子數為NA
D.常溫常壓下,48gO2與O3混合物含有的氧原子數為3NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某濃度的氨水中存在下列平衡:NH3·H2O ![]() NH4++OH-,若想增大NH4+的濃度,而不增大OH-的濃度,應采取的措施是( )
NH4++OH-,若想增大NH4+的濃度,而不增大OH-的濃度,應采取的措施是( )
A. 適當升高溫度B. 加入NaCl固體C. 通入NH3D. 加入少量鹽酸
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度下,相同pH的鹽酸和醋酸分別加水稀釋至平衡,pH隨溶液體積變化的曲線如下圖所 示。據圖判斷正確的是

A. Ⅱ為鹽酸稀釋時的pH變化曲線
B. b點溶液的導電性比c點溶液的導電性強
C. a點KW的數值比c點KW的數值大
D. b點酸的總濃度大于a點酸的總濃度
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】pH都等于9的NaOH和CH3COONa兩種溶液中,設由水電離產生的OH-濃度分別為amol·L-1與bmol·L-1,則a和b的關系為
A. a>b B. a=10-4b C. b=10-4a D. a=b
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】霧霾嚴重影響人們的生活與健康。某地區的霧霾中可能含有如下可溶性無機離子:Na+、NH4+、Mg2+、Al3+、SO42-、NO3-、Cl- 。某同學收集了該地區的霧霾,經必要的預處理后試樣溶液,設計并完成了如下的實驗:

已知:3NO3-+ 8Al + 5OH- + 2H2O![]() 3NH3 + 8AlO2-
3NH3 + 8AlO2-
根據以上的實驗操作與現象,該同學得出的結論不正確的是
試樣中肯定存在NH4+、Mg2+、SO42-和NO3-
試樣中一定不含Al3+
試樣中可能存在Na+、Cl-
該霧霾中可能存在NaNO3 、NH4Cl和MgSO4
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學興趣小組用圖甲裝置制備了氯氣,并進行了一系列實驗。
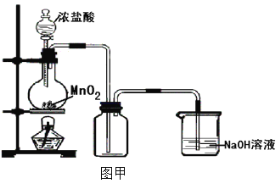
(1)實驗室制備氯氣的反應原理是_______________________
(2)若有87gMnO2參加反應,則被氧化的氯化氫的物質的量為____________;而實際收集的氯氣量準是比理論值小,試寫出其可能的一種原因____________
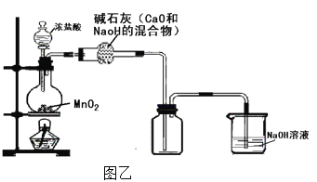
(3)乙同學認為圖甲裝置制備的氯氣不純凈,其中混有HCl氣體和水蒸氣,對裝置進行了如圖乙改進。你認為合理嗎?____________ (合理則填入“合理”二字,如不合理則用文字說明理由)
(4)將圖甲裝置合理改裝后制取并收集一瓶氯氣,將灼熱的鐵絲插到充滿氯氣的集氣瓶中,看到鐵絲在氯氣中繼續燃燒,在集氣瓶內充滿棕色的煙,煙的成分為反應方程式為____________
(5)另收集一瓶氯氣并在集氣瓶中加入水,觀察到液體為淺黃綠色,有此現象的原因是____________;將溶液分成三份,分別加入一-定量的下列溶液,寫出反應的方程式:
Na2CO3溶液____________
AgNO3溶液____________
KI溶液____________
(6)若實驗中有少量的氯氣散發到空氣中,試設計方案將其檢測出____________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有a、b、c、d四個金屬電極,有關的實驗裝置及部分實驗現象如下:
實驗裝 置 |
|
|
|
|
部分實驗現象 | a極質量減小;b極質量增加 | b極有氣體產生;c極無變化 | d極溶解;c極有氣體產生 | 電流從a極流向d極 |
由此可判斷這四種金屬的活動性順序是( )
A.a>b>c>dB.b>c>d>aC.d>a>b>cD.a>b>d>c
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com