
【題目】甲同學認為Ca(OH)2與CO2能反應,而NaOH與CO2不能反應,因為實驗室檢驗CO2用澄清石灰水而不用NaOH溶液。乙同學認為甲同學的說法不完全正確。乙同學怎么通過實驗證明自己的觀點呢?請你與乙同學一起在實驗室完成以下實驗。
【提出假設】NaOH溶液與CO2能反應。
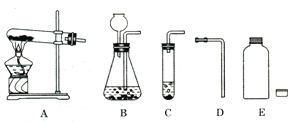
【設計方案】(1)常用 和 反應制取CO2氣體;
(2)請從如圖所示的實驗裝置中選出正確的制取裝置 (填字母),不選擇其它發生裝置的理由是 。
(3)驗證假設:
實驗步驟 | 實驗現象 | 結論 |
第一步:向集滿CO2的塑料瓶中注入少量NaOH溶液,立即旋好蓋子,振蕩 | NaOH溶液吸收了塑料瓶中的CO2氣體 | |
第二步:取上一步中所得溶液,加入鹽酸 | 有關反應的化學方程式為 |
所以,假設成立。
(4)【總結與反思】丙同學認為還應該做一個對比實驗,其理由是 。
【答案】【設計方案】(1)石灰石(或大理石) 稀鹽酸
(2)CDE、固液反應,不需加熱且不漏氣
(3)
塑料瓶變癟 | ||
有氣泡產生 | Na2CO3+2HCl=2NaCl+CO2↑+H2O |
(4)【總結與反思】二氧化碳溶解于水(與水反應)也可使氣壓減小,塑料瓶變癟。(合乎題意即可)
【解析】
試題分析:(1)設計方案:①實驗室制取二氧化碳的反應原理是碳酸鈣和稀鹽酸反應生成氯化鈣、水和二氧化碳,所以常用石灰石和稀鹽酸反應制取CO2氣體
(2)實驗室制CO2氣體用的是固體和液體不加熱制備氣體,根據反應物的狀態和反應條件,應選固液在常溫下的反應,即選擇的裝置為CDE,不選擇其它發生裝置的理由是固液反應,不需加熱且不漏氣。
(3)NaOH溶液吸收了塑料瓶中的CO2氣體會導致瓶內的壓強減小,所以塑料瓶變癟;氫氧化鈉會與二氧化碳反應生成碳酸鈉,碳酸鈉與鹽酸反應會生成二氧化碳氣體,所以現象是有氣泡產生,反應的化學方程式為Na2CO3+2HCl=2NaCl+CO2↑+H2O;
(4)由于二氧化碳溶解于水(與水反應)也可使氣壓減小,塑料瓶也會變癟,所以不能確定氫氧化鈉與二氧化碳發生了化學反應。


科目:高中化學 來源: 題型:
【題目】下列關于鈉的化合物的敘述,錯誤的是:
A.硫酸鈉晶體俗稱芒硝,它是造紙的重要原料
B.澄清的石灰水中滴加碳酸鈉溶液有白色沉淀,滴加碳酸氫鈉無白色沉淀
C.氟化鈉是一種農藥,可殺滅地下害蟲
D.碳酸氫鈉不適合給胃潰瘍病人使用
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學與生活密切相關,下列說法正確的是( )
A.加碘食鹽不能使淀粉溶液變藍
B.凡含有食品添加劑的食物對人體健康均有害,不可食用
C.為防止電池中的重金屬等污染土壤和水體,應集中回收并填埋處理,開發廢電池的綜合利用技術
D.乙醇是不可再生的能源
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是
A.常溫下,PH=9的碳酸鈉溶液中由水電離出的c(OH-)=1×10-9mol·L-1
B.溫度相同時,在弱酸溶液和強堿稀溶液中,水的離子積常數Kw相同
C.將pH=4的醋酸溶液稀釋后,溶液中所有離子的濃度均降低
D.中和等體積pH相同的H2SO4和HCl溶液,消耗NaOH的物質的量為2:1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列是實驗室常見的化學物質,按酸、堿、鹽分類順序排列正確的是
A. 硝酸、純堿、氯化鈉 B. 醋酸、燒堿、硫酸銅
C. 硫酸、熟石灰、苛性鉀 D. 鹽酸、小蘇打、熟石灰
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某鹽的混合物中含有0.2mol Na+、0.4mol Mg2+、0.4mol Cl-、0.1mol Al3+及一定量的SO42-,則其中所含SO42-的物質的量為
A. 0.1mol B. 0.3mol C. 0.5mol D. 0.45mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列轉化關系中,不能通過一步反應實現的是( )
①SiO2→Na2SiO3 ②CuSO4→CuCl2
③SiO2→H2SiO3 ④CuO→Cu(OH)2 ⑤Na2O2→Na2SO4
A.①和② B.③和④ C.②③④ D.②③④⑤
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知,I2(aq)+I﹣(aq)![]() I3﹣(aq).某I2、KI溶液中,c(I3﹣)與溫度(T)的關系如圖所示(曲上任何一點都表示平衡狀態).下列說法正確的是
I3﹣(aq).某I2、KI溶液中,c(I3﹣)與溫度(T)的關系如圖所示(曲上任何一點都表示平衡狀態).下列說法正確的是
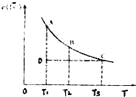
A. 反應I2(aq)+I﹣(aq)![]() I3﹣(aq)△H>0
I3﹣(aq)△H>0
B. 狀態A的c (I2)比狀態D的小
C. A點對應的反應速率大于C點對應的反應速率
D. 其他條件不變,向溶液中加入KI固體,平衡由C點移動到D點
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學利用下列實驗探究金屬鋁與銅鹽溶液反應:下列說法正確的是( )
A. 由實驗1 可以得出結論:金屬鋁的活潑性弱于金屬銅
B. 實驗2 中生成紅色物質的離子方程式:Al+Cu2+═Al3++Cu
C. 溶液中陰離子種類不同是導致實驗1、2 出現不同現象的原因
D. 由上述實驗可推知:用砂紙打磨后的鋁片分別與濃度均為0.2molL﹣1的鹽酸和硫酸反應,后者更劇烈
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com