
下列關于熱化學反應的描述中正確的是( )
A.500℃、30MPa下,將0.5mol N2和1.5molH2置于密閉的容器中充分反應生成NH3(g),放熱19.3kJ,其熱化學方程式為:N2(g) + 3H2(g) 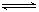 2NH3(g) △H=-38.6kJ·mol-1 2NH3(g) △H=-38.6kJ·mol-1 |
| B.HCl和NaOH反應的中和熱ΔH=-57.3 kJ·mol-1,則H2SO4和Ca(OH)2反應的中和熱ΔH=2×(-57.3)kJ·mol-1 |
| C.CO(g)的燃燒熱是283.0 kJ·mol-1,則2CO2(g) =2CO(g)+O2(g)反應的ΔH=+2×283.0 kJ·mol-1 |
| D.1 mol甲烷燃燒生成氣態水和二氧化碳所放出的熱量是甲烷的燃燒熱 |
C
解析試題分析:可逆反應中的反應熱是指完全生成產物放出的熱量,A項錯誤;中和熱是指生成1mol水放出的熱量,B項錯誤;1 mol甲烷燃燒生成液態水和二氧化碳所放出的熱量是甲烷的燃燒熱,D項錯誤。答案選C。
考點:熱化學方程式書寫判斷
點評:熱化學方程式是表示化學反應與反應熱關系的方程式。書寫和應用熱化學方程式時必須注意以下幾點:①明確寫出反應的計量方程式,各物質化學式前的化學計量系數可以是整數,也可以是分數。②各物質化學式右側用圓括弧()表明物質的聚集狀態。可以用g、l、s分別代表氣態、液態、固態。溶液中的反應物質,則須注明其濃度,以aq代表水溶液,(aq) 代表無限稀釋水溶液。③反應熱與反應方程式相互對應。若反應式的書寫形式不同,則相應的化學計量系數不同,故反應熱亦不同。④熱化學方程式必須標明反應的濃度、溫度和壓力等條件,若在常溫常壓時可省略。


湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com