
【題目】甲、乙是兩種常見的化合物,X、Y、Z是三種常見的單質。下表所列各組物質之間通過一步反應不能實現如圖所示轉化的是( )
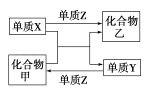
選項 | X | Y | Z | 甲 | 乙 |
A | C | H2 | O2 | H2O | CO |
B | Zn | Fe | Cl2 | FeCl2 | ZnCl2 |
C | Mg | C | O2 | CO2 | MgO |
D | H2 | Si | Cl2 | SiCl4 | HCl |
A.AB.BC.CD.D
科目:高中化學 來源: 題型:
【題目】以粉煤灰(主要含Al2O3、SiO2,還有少量的Fe2O3)為原料制取Al2O3的流程如下:
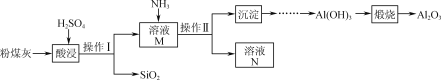
(1)操作Ⅰ的名稱是________;溶液N中的溶質主要是____________(填化學式)。
(2)用H2SO4“酸浸”時的離子方程式為__________________________________(任寫一個)。
(3)“煅燒”時的化學方程式為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】基態原子由原子核和繞核運動的電子組成,下列有關核外電子說法正確的是
A.基態原子的核外電子填充的能層數與元素所在的周期數相等
B.基態原子的核外電子填充的軌道總數一定大于或等于![]() (m表示原子核外電子數)
(m表示原子核外電子數)
C.基態原子的核外電子填充的能級總數為![]() (n為原子的電子層數)
(n為原子的電子層數)
D.基態原子的核外電子運動都有順時針和逆時針兩種自旋狀態
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】由下列實驗及現象不能得出相應結論的是( )
實驗 | 現象 | 結論 | |
A | 向濃度均為 |
| 非金屬性: |
B. | 向含有酚酞的 | 觀察到紅色變淺 | 證明 |
C | 室溫下,用pH試紙測 |
|
|
D. | 向盛有10滴 | 有黃色沉淀生成 |
|
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據下列物質的轉化關系,回答問題:
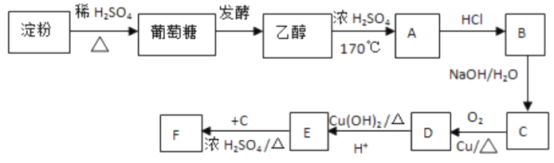
(I)淀粉屬于___。
A.多糖 B.酯類 C.高分子化合物 D.單糖
(2)葡萄糖常用于水壺膽鍍銀,說明它有___(寫出官能團名稱);
(3)完成下列方程式:C6H12O6![]() 2C2H5OH+2___
2C2H5OH+2___
(4)寫出B的結構簡式:___;
(5)寫出下列化學方程式:
①C→D:___;
②E+C→F:___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】研究水體中碘的存在形態及其轉化是近年的科研熱點。I-與I2在水體和大氣中的部分轉化如下圖所示。
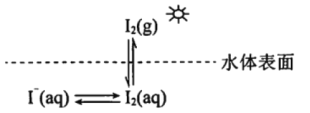
(1) I2的電子式為______________。
(2)水體中的I-在非酸性條件下難于被空氣中的![]() 氧化。原因是
氧化。原因是![]() 的反應速率慢,反應程度小。
的反應速率慢,反應程度小。
①I-在酸性條件下與![]() 反應的離子方程式是_____________________________________。
反應的離子方程式是_____________________________________。
②在酸性條件下I-易被![]() 氧化的可能的原因是______________________________________。
氧化的可能的原因是______________________________________。
(3)有資料顯示:水體中若含有![]() ,會對
,會對![]() 氧化I-產生影響。為檢驗這一結論,進行如下探究實驗:分別將等量的
氧化I-產生影響。為檢驗這一結論,進行如下探究實驗:分別將等量的![]() 通入到
通入到![]() 下列試劑中,一段時間后,記錄實驗現象與結果。己知:每
下列試劑中,一段時間后,記錄實驗現象與結果。己知:每![]() 參與反應,生成
參與反應,生成![]() 。
。
序號 | 試劑組成 | 反應前溶液的 | 反應后溶液的 |
|
|
甲 |
| 5.3 | 11.0 | 約10% | |
乙 |
| 5.1 | 4.1 | 約100% | 大量 |
丙 |
| 5.2 | 3.5 | —— | 少量 |
①![]() _______________________。
_______________________。
②甲中反應為可逆反應,其離子方程式是________________________。
③比較甲、乙、丙實驗,說明![]() 在實驗乙中的作用并解釋_______________________。
在實驗乙中的作用并解釋_______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】乙醇和乙酸是生活中兩種常見的有機物。請回答下列問題:
(1)乙醇的結構簡式為CH3CH2OH,乙醇的官能團名稱為__________;乙酸的結構簡式為CH3COOH,乙酸的官能團名稱為__________;生活中常用食醋除去暖瓶內的水垢(主要成分是CaCO3),反應的化學方程式為2CH3COOH+CaCO3=(CH3COO)2Ca+CO2↑+H2O。通過這個事實,你得出醋酸與碳酸的酸性強弱關系是:醋酸_____碳酸(填“>”或“<”);
(2)在濃硫酸的催化作用下,加熱乙酸和乙醇的混合溶液,可發生酯化反應。請完成化學方程式:CH3COOH + CH3CH2OH CH3COOCH2CH3+________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鈷酸鋰(LiCoO2)電池是一種應用廣泛的新型電源,電池中含有少量的鋁、鐵、碳等單質。實驗室嘗試對廢舊鈷酸鋰電池回收再利用。實驗過程如下:
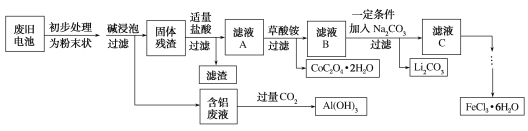
已知:①還原性:Cl->Co2+;
②Fe3+和![]() 結合生成較穩定的[Fe(C2O4)3]3-,在強酸性條件下分解重新生成Fe3+。回答下列問題:
結合生成較穩定的[Fe(C2O4)3]3-,在強酸性條件下分解重新生成Fe3+。回答下列問題:
(1)廢舊電池初步處理為粉末狀的目的是________。
(2)從含鋁廢液得到Al(OH)3的離子方程式為___________
(3)濾液A中的溶質除HCl、LiCl外還有________(填化學式)。寫出LiCoO2和鹽酸反應的化學方程式____________
(4)濾渣的主要成分為_______(填化學式)。
(5)在空氣中加熱一定質量的CoC2O4·2H2O固體樣品時,其固體失重率數據見下表,請補充完整表中問題。
已知:①CoC2O4在空氣中加熱時的氣體產物為CO2。
②固體失重率=對應溫度下樣品失重的質量/樣品的初始質量。
序號 | 溫度范圍/℃ | 化學方程式 | 固體失重率 |
Ⅰ | 120~220 | CoC2O4·2H2O CoC2O4+2H2O | 19.67% |
Ⅱ | 300~350 | ______ | 59.02% |
(6)已知Li2CO3的溶度積常數Ksp=8.64×10-4,將濃度為0.02 mol·L-1的Li2SO4和濃度為0.02 mol·L-1的Na2CO3溶液等體積混合,則溶液中的Li+濃度為________ mol·L-1。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】丙烯是石油化學工業的重要基礎原料,我國科學家利用甲醇轉化制丙烯反應過程如下:
3CH3OH +H3AlO6 →3![]() +
+![]() +3H2O
+3H2O
3![]() +
+![]() →H3AlO6 + 3C○↑↓H2
→H3AlO6 + 3C○↑↓H2
3C○↑↓H2 → CH2=CHCH3
下列敘述錯誤的是
A.甲醇轉化制丙烯反應的方程式為3CH3OH→CH2=CHCH3+3H2O
B.甲醇轉化制丙烯反應的過程中H3AlO6作催化劑
C.1.4 g C○↑↓H2所含的電子的物質的量為1 mol
D.甲基碳正離子![]() 的電子式為
的電子式為![]()
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com