
在t℃時,AgBr在水中的沉淀溶解平衡曲線如圖所示。又知t℃時AgCl的Ksp=4×10-10,下列說法不正確的是 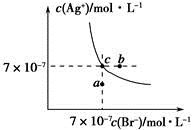
| A.在t℃時,AgBr的Ksp為4.9×10-13 |
| B.在AgBr飽和溶液中加入NaBr固體,可使溶液由c點到b點 |
| C.圖中a點對應的是AgBr的不飽和溶液 |
D.在t℃時,AgCl(s)+Br-(aq)  AgBr(s)+Cl-(aq)平衡常數K≈816 AgBr(s)+Cl-(aq)平衡常數K≈816 |
科目:高中化學 來源: 題型:單選題
25℃時,由弱酸(HA)及其鹽(NaA)組成的混合溶液,起始濃度均為1mol·L-1。下圖為向該溶液中通入HCl氣體或加入NaOH固體時,溶液pH隨加入H+或OH-的物質的量而變化的曲線。下列說法中,正確的是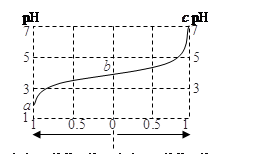
A.加NaOH,HA電離平衡常數增大
B.通入HCl,溶液中陰離子濃度之和減小
C.溶液中水的電離程度a>b>c
D.b點溶液中,c(HA)<c(A-)
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列有關實驗的敘述正確的是
| A.已知Cu2O+2H+=Cu2++Cu+H2O,氫氣還原氧化銅后生成的紅色固體能完全溶于稀硝酸,說明還原產物是銅 |
| B.在中和熱測定的實驗中,將NaOH溶液和鹽酸混合反應后的冷卻溫度作為末溫度 |
| C.僅用淀粉溶液、稀硫酸、碘水、新制氫氧化銅四種試劑可完成淀粉水解產物及水解程度檢驗的探究實驗 |
| D.向盛有少量Mg(OH )2懸濁液的試管中滴加氯化銨溶液,可以看到沉淀溶解 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
相同體積的pH=3的強酸溶液和弱酸溶液分別跟足量的鎂完全反應
| A.強酸溶液產生較多的氫氣 | B.兩者產生等量的氫氣 |
| C.無法比較兩者產生氫氣的量 | D.弱酸溶液產生較多的氫氣 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
有25℃時0.1 mol/L的①氯化銨、②氯化鈉、③醋酸鈉三種溶液。下列有關判斷不正確的是
| A.①與②比較:c(Na+)>c(NH4+) |
| B.①中離子濃度的大小關系是:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| C.①和②等體積混合的溶液中:c(Cl-)=c(Na+)+c(NH4+)+c(NH3·H2O) |
| D.向③中滴加適量醋酸溶液,使溶液pH=7,則:c(CH3COO-)>c(Na+) |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
牙齒表面覆蓋的牙釉質是人體中最堅硬的部分,起著保護牙齒的作用,其主要成分為羥基磷酸鈣[Ca5(PO4)3OH]。在牙齒表面存在著如下平衡:Ca5(PO4)3OH(s) 5Ca2+(aq)+3PO43-(aq)+OH-(aq) Ksp = 6.8×10-37
5Ca2+(aq)+3PO43-(aq)+OH-(aq) Ksp = 6.8×10-37
下列說法錯誤的是( )
| A.殘留在牙齒上的糖發酵會產生H+,經常吃糖易造成齲齒 |
| B.由上述平衡可知,小孩長牙時要少吃糖多補鈣 |
| C.若減小OH-的濃度,上述平衡將向右移動,Ksp的值相應增大 |
| D.使用含氟牙膏能防止齲齒,是因為Ca5(PO4)3OH(s)轉化為更難溶的Ca5(PO4)3F(s) |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列有關說法正確的是
A.0.1 mol/L NH4C1溶液加蒸餾水稀釋,溶液的pH不斷減小
B.常溫下,pH=2的CH3COOH溶液與pH=12的NaOH溶液等體積混合后,溶液的pH<7
C. 水的離子積常數Kw隨著溫度的升高而增大,說明水的電離是放熱反應
D.0.1 mol/L的NaHA溶液,其pH=4: c(HA-) > c(H+)> c(H2A) > c(A2-)
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
常溫下,物質的量濃度為0.01 mol·L-1的醋酸溶液和鹽酸,下列說法正確的是
| A.溶液的pH相同 |
| B.分別加入足量鋅片,鹽酸生成的H2體積大 |
| C.分別稀釋100倍后,醋酸濃度與鹽酸濃度相等 |
| D.由水電離出的氫離子濃度均為1×10-12 mol·L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
有關電解質溶液的敘述,下列說法中正確的是
A.0.2 mol·L-1氨水中,c(OH-)與c(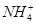 )相等 )相等 |
| B.10 mL 0.02 mol·L-1 HCl溶液與10 mL 0.02 mol·L-1 Ba(OH)2溶液充分混合,若混合后溶液的體積為20 mL,則溶液的pH=12 |
| C.0.1 mol/L的Na2S溶液中,c(OH-)=c(H+)+c(HS-)+c(H2S) |
| D.pH=3的一元酸和pH=11的一元堿等體積混和后的溶液中一定是c(OH-)=c(H+) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com