
計算:
Ⅰ、(1)0.3 mol NH3分子中所含氫原子數與_______NA個H2O分子中所含氫原子數相等。
(2)在標準狀況下36 克CO和CO2的混合氣體的體積為22.4L,則此混合氣體中CO物質的量為 ;CO2的質量為 g 。
(3)將標準狀況下224 L HCl氣體溶于635 mL水中(ρ=1 g/cm3),所得鹽酸的密度為1.18 g/cm3。則此鹽酸的物質的量濃度為 。
(結果保留至小數點后1位)
Ⅱ、某同學設計了測定氣體摩爾體積的探究實驗,利用氯酸鉀分解制O2。
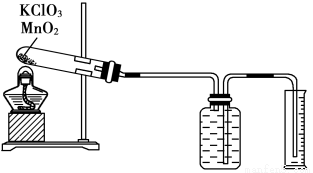
(1)實驗步驟如下:
①連接好實驗裝置,檢查裝置的氣密性。
②把適量的氯酸鉀粉末和少量二氧化錳粉末混合均勻,放入干燥的試管中,準確稱量試管和藥品的總質量為15.95 g。
③加熱,開始反應,直到不再有氣體產生為止。
④測量排入量筒中水的體積為285.0 mL,換算成T℃,101kPa氧氣的體積為360.0 mL。
⑤準確稱量試管和殘留物的質量為15.55 g。
(2)利用以上數據,本實驗測得T℃,101kPa的氣體摩爾體積為
(結果保留至小數點后1位)
Ⅰ、(1)0.45(2分) (2)0.5mol(2分);22(2分) (3)11.8 mol/L(2分)
Ⅱ、(2)28.8 L/mol(2分) n=m/M=V/Vm=N/NA
【解析】
試題分析:Ⅰ(1)根據原子個數之比等于原子的物質的量之比,要想使NH3和H2O的氫原子個數相等,也就是氫原子的物質的量相等,0.3mol NH3中所含氫原子物質的量為0.9mol,則H2O中氫原子的物質的量也為0.9mol,則水分子的物質的量為0.45mol,分子數為0.45NA;(2)標準狀況下,混合氣體22.4L,物質的量為1mol,設CO的物質的量為x,CO2的物質的量為y,則:x?28g/mol+y?44g/mol=36g,x+y=1mol解得:x=0.5mol,y=0.5mol,則:m(CO2)=0.5mol×44g/mol=22g,即CO的物質的量為0.5mol,CO2質量為22g;(3)根據n= V/Vm計算224L氯化氫氣體物質的量為10mol,再根據m=nM計算HCl的質量為365g,根據m=ρV計算水的質量為635g,鹽酸的質量為1000g,根據V=m/ρ計算鹽酸的體積,再根據c=n/v計算的鹽酸的濃度為11.8 mol/L;Ⅱ分析題給數據得m(O2)=15.95 g—15.55 g=0.40g,根據n=m/M計算n(O2)=0.0125mol,根據Vm=V/n將數據代入計算,Vm=28.8L。
考點:考查以物質的量為中心的計算。


科目:高中化學 來源:2016屆廣東省高一上學期期中考試化學試卷(解析版) 題型:填空題
(1)在K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O反應中,_________是氧化劑, _______是還原劑,HCl表現的性質是_______和________,1mol K2Cr2O7反應轉移電子的物質的量是_________。
(2)下列物質中①食鹽水②NaOH ③Cu ④HCl氣體⑤空氣 ⑥酒精 ⑦CO2 ⑧KNO3屬于電解質的是 (填序號,下同);屬于非電解質的是 。
查看答案和解析>>
科目:高中化學 來源:2016屆廣東省梅州市高一上學期質檢化學試卷(解析版) 題型:計算題
實驗室常用鹽酸的質量分數為36.5%,密度為1.20g/㎝3。
⑴此濃鹽酸的物質的量濃度是多少?(列式計算)
⑵配制100mL3.00mol/L的鹽酸,需以上濃鹽酸多少mL?(列式計算)
⑶用濃鹽酸配制該稀鹽酸需要以下哪些步驟(按操作順序填寫序號): 。
①計算 ②裝瓶③用50 mL量筒量取一定體積的濃鹽酸④洗滌⑤移液⑥稀釋⑦定容⑧搖勻
查看答案和解析>>
科目:高中化學 來源:2016屆廣東省梅州市高一上學期質檢化學試卷(解析版) 題型:選擇題
已知X、Y均為1~18號之間的元素,X、Y可形成化合物X2Y和X2Y2,又知Y的原子序數小于X的原子序數,則兩種元素的原子序數之和為( )
A.19 B.18 C.27 D.9
查看答案和解析>>
科目:高中化學 來源:2016屆廣東省高一上學期期中考試化學試卷(解析版) 題型:選擇題
下列各組混合物的分離或提純方法正確的是
A.提純NaCl和KNO3的混合物中的KNO3:加熱蒸發、冷卻結晶,過濾
B.除去CO2中混有的少量CO:混合氣體依次通過NaOH溶液和濃硫酸
C.除去鹽酸中混有的少量CaCl2:加入過量CaCO3粉末,過濾
D.除去NaCl溶液中混有的少量I2:向混合溶液中加入適量CCl4,充分振蕩,分液
查看答案和解析>>
科目:高中化學 來源:2016屆廣東省高一上學期期中考試化學試卷(解析版) 題型:選擇題
下列各物質所含原子數目,按由大到小順序排列的是
①0.5mol NH3 ②標準狀況下22.4L He ③4℃ 9mL水(ρ=1g/mL) ④0.2mol H3PO4
A.④③②① B.①④②③ C.①④③② D.②③④①
查看答案和解析>>
科目:高中化學 來源:2016屆廣東省佛山市質量檢測化學試卷(解析版) 題型:選擇題
下列有關離子的檢驗方法和判斷正確的是
A.向某溶液中加入Na2CO3溶液,若有白色沉淀生成,證明一定含有Ca2+
B.向某固體中加入稀鹽酸,產生了無色氣體,證明該固體一定含有CO32—
C.向某溶液中滴加KSCN溶液,若溶液出現紅色則說明原溶液中含Fe3+
D.向某溶液中先加稀硝酸,再加BaC12溶液,生成白色沉淀,證明一定含有SO42—
查看答案和解析>>
科目:高中化學 來源:2016屆山西省朔州市高一上學期第四次月考化學試卷(解析版) 題型:填空題
實驗室可以用KMnO4固體和濃鹽酸反應制取氯氣,反應方程式如下:
2KMnO4+16HCl(濃)=2KCl+2MnCl2+5Cl2↑+8H2O。
①請用“雙線橋”標出電子轉移的方向和數目;(2分)
②該反應中被氧化和未被氧化的HCl的物質的量之比是 _______。(1分)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com