
【題目】短周期主族元素X、Y、Z、W的原子序數依次增大。X原子最外層比次外層多3個電子;Y、Z均為金屬,Y是同周期中原子半徑最大的元素,Z的簡單離子半徑在同周期元素中最小;W的最高價氧化物在無機含氧酸中酸性最強。下列說法正確的是( )
A. X的氣態氫化物的熱穩定性比O(氧)的強
B. 元素Z、W的簡單離子具有相同的電子層結構
C. Y、Z、W的最高價氧化物對應的水化物之間能相互反應
D. 等質量的Y和Z單質分別與足量稀鹽酸反應,前者產生的氫氣多
【答案】C
【解析】
短周期主族元素X、Y、Z、W的原子序數依次增大.X原子最外層比次外層多3個電子,則X為N元素;Y、Z均為金屬,Y是同周期中原子半徑最大的元素,Y為Na元素,Z的簡單離子半徑在同周期元素中最小,Z為Al元素;W的最高價氧化物在無機含氧酸中酸性最強,W為Cl元素.由上述分析可知,X為N,Y為Na,Z為Al,W為Cl。A.非金屬性越強,對應氫化物越穩定,則X的氣態氫化物的熱穩定性比O(氧)的弱,故A錯誤;B.元素Z、W的簡單離子具有相同的電子層結構不同,分別為10電子、18電子結構,故B錯誤;C.Z的氫氧化物具有兩性,與NaOH、高氯酸均反應,則Y、Z、W的最高價氧化物對應的水化物之間能相互反應,故C正確;D.等質量的Y和Z單質分別與足量稀鹽酸反應,由![]() 、
、![]() ×3可知,轉移電子不同,后者生成氫氣多,故D錯誤;故選C。
×3可知,轉移電子不同,后者生成氫氣多,故D錯誤;故選C。


科目:高中化學 來源: 題型:
【題目】下列各組離子能大量共存的是
A. Na+、Mg2+、CO32-、I-
B. H+ NO3-、Fe2+、Br-
C. NH4+、K+、SO42-、Cl-
D. Na+、S2-、Cu2+、SO32-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】選擇適宜的材料和試劑設計一個原電池,完成下列反應:
Zn + CuSO4= ZnSO4+ Cu
(1)畫出裝置圖,并標明各部分材料名稱_______。
(2)負極材料____,正極材料_______,電解質溶液是______。
(3)寫出電極反應式:
負極:_____________________;
正極:__________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化合物F是合成抗過敏藥孟魯斯特鈉的重要中間體,其合成過程如下:

請回答下列問題:
(1)化合物C中含有氧官能團為________、________(填名稱)。
(2)化合物B的分子式為C16H13O3Br,B的結構簡式為________。
(3)由C→D、E→F的反應類型依次為________、________。
(4)寫出符合下列條件C的一種同分異構體的結構簡式________。
Ⅰ、屬于芳香族化合物,且分子中含有2個苯環
Ⅱ、能夠發生銀鏡反應
Ⅲ、分子中有5種不同環境的氫原子.
(5)已知:RCl![]() RMgCl,寫出CH3CH2OH、
RMgCl,寫出CH3CH2OH、![]() 為原料制備
為原料制備 的合成路線流程圖(乙醚溶劑及無機試劑任用);________
的合成路線流程圖(乙醚溶劑及無機試劑任用);________
合成路線流程圖示例如下:H2C=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH.
CH3CH2OH.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】從金屬利用的歷史來看,先是青銅器時代,而后是鐵器時代,鋁的利用是近百年的事。這個先后順序跟下列有關的是:
①地殼中的金屬元素的含量;②金屬活動性;③金屬的導電性;④金屬冶煉的難易程度;⑤金屬的延展性;
A. ①③ B. ②⑤ C. ③⑤ D. ②④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將4molA氣體和2molB氣體在2L的密閉容器中混合并在一定條件下發生如下反應2A(g)+B(g)![]() 2C(g);△H<0。4s(秒)后反應達到平衡狀態,此時測得C的濃度為0.6mol·L-1。下列說法中正確的是
2C(g);△H<0。4s(秒)后反應達到平衡狀態,此時測得C的濃度為0.6mol·L-1。下列說法中正確的是
A.4s(秒)時B的濃度為0.3mol·L-1
B.4s內用物質A表示的反應速率為0.075mol·L-1·s-1
C.達平衡后B的轉化率為30%
D.達平衡后若通入一定量氦氣,A的轉化率降低
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列圖示與對應的敘述相符的是( )
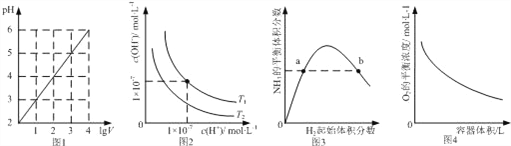
A. 圖1表示1 LpH=2的CH3COOH溶液加水稀釋至V L,pH隨lgV的變化
B. 圖2表示不同溫度下水溶液中H+和OH﹣濃度的變化的曲線,圖中溫度T2>T1
C. 圖3表示一定條件下的合成氨反應中,NH3的平衡體積分數隨H2起始體積分數(N2的起始量恒定)的變化,圖中a點N2的轉化率小于b點
D. 圖4表示同一溫度下,在不同容積的容器中進行反應2BaO2(s)![]() 2BaO(s)+O2(g),O2的平衡濃度與容器容積的關系
2BaO(s)+O2(g),O2的平衡濃度與容器容積的關系
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將10℃的0.2molN2O4置于2L密閉的燒瓶中,然后將燒瓶放入100℃的恒溫槽中,燒瓶內的氣體逐漸變為紅棕色:N2O4(g)![]() 2NO2(g)。下列結論能說明上述反應在該條件下已經達到平衡狀態的是( )
2NO2(g)。下列結論能說明上述反應在該條件下已經達到平衡狀態的是( )
①燒瓶內氣體的平均相對分子質量不再變化
②NO2的物質的量濃度不再改變
③燒瓶內氣體的壓強不再變化
④燒瓶內氣體的質量不再變化
⑤燒瓶內氣體的顏色不再加深
⑥N2O4的消耗速率與NO2的生成速率之比為1:2
⑦NO2生成速率與NO2消耗速率相等
⑧燒瓶內氣體的密度不再變化。
A. ①②③⑤⑦ B. ①②③⑤⑥⑦ C. ①②③④ D. ②③⑦⑧
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一定溫度下的定容密閉容器中,當下列物理量不再變化時,不能表明反應:A(s)+2B(g)![]() C(g)+D(g)已達平衡的是( )
C(g)+D(g)已達平衡的是( )
A.混合氣體的壓強 B.混合氣體的密度
C.B的物質的量濃度 D.混合氣體的平均分子量
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com