
【題目】右圖是溫度和壓強對反應:X+Y ![]() 2Z 影響的示意圖。圖中橫坐標表示溫度,縱坐標表示平衡混合氣體中Z的體積分數。下列敘述正確的是
2Z 影響的示意圖。圖中橫坐標表示溫度,縱坐標表示平衡混合氣體中Z的體積分數。下列敘述正確的是
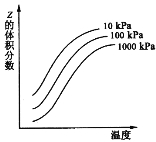
A.上述可逆反應的正反應為放熱反應
B.X、Y、Z均為氣態
C.X和Y只有一種為氣態,Z為氣態
D.上述反應的逆反應的△H>0
科目:高中化學 來源: 題型:
【題目】MnO2用途很廣,它是一種廣泛應用的氧化劑。例如將它加入熔態的玻璃中,可以除去帶色的雜質(硫化物或亞鐵鹽),稱為普通玻璃的“漂白劑”。在錳-鋅干電池中用作去極劑,以氧化在電極上產生的氫。
(1)Zn- MnO2干電池應用廣泛,其電解質溶液是ZnCl2-NH4Cl混合溶液。其電解質溶液呈________性(填“酸”、“堿”或“中”),原因是_________________、________________(用離子方程式表示);該電池工作時,電子流向__________極(填“正”或 “負”)。
(2)工業上,常以菱錳礦(主要成分MnCO3,常含有少量鐵、鈣、鋅等元素)為原料,用電解法可以制備MnO2。其制備過程如下:

寫出酸浸的主要化學方程式:______________________。
②下圖可以看出,從MnSO4和ZnSO4混合溶液中結晶MnSO4·H2O晶體,需要控制的溫度范圍為______________(填字母)。
A.0~40℃ B.40~60℃ C.60℃以上
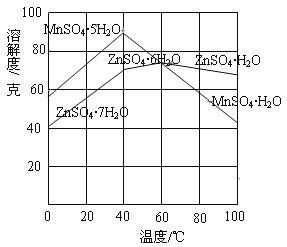
③請寫出用惰性電極電解MnSO4溶液制備MnO2的陽極反應:___________________。
④該工藝產生的廢水中含有較多的Mn2+,通常用H2S或者Na2S溶液處理。25 ℃,在0.10 mol·L-1 H2S溶液中,通入HCl氣體或加入NaOH固體以調節溶液pH,溶液pH與c(S2-)關系如圖(忽略溶液體積的變化、H2S的揮發)。
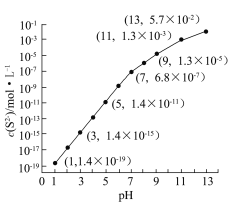
i.pH=13時,溶液中的c(H2S)+c(HS-)=__________mol·L-1;
ii.某溶液含x mol·L-1 Mn2+、0.10 mol·L-1 H2S,當調節溶液pH=5時,Mn2+開始沉淀,則x= 。[已知:Ksp(MnS)=2.8×10-13]
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是
A.植物油氫化過程中發生了加成反應
B.淀粉和纖維素互為同分異構體
C.環己烷與苯可用酸性KMnO4溶液鑒別
D.水可以用來分離溴苯和苯的混合物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列反應的離子方程式正確的是
A.石灰石溶于稀鹽酸:CaCO3+2H+=Ca2++CO2↑+H2O
B.硫酸銅溶液與氫氧化鋇溶液反應:Ba2++SO42-=BaSO4↓
C.氧化鎂與稀硫酸:MgO+2H+=Mg2++H2O
D.常溫下,將銅片插入硝酸銀溶液中:Cu+Ag+=Cu2++Ag
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列敘述正確的是
A. 目前加碘食鹽中主要添加的是KIO3
B. 日常生活中和醫院常用無水乙醇殺菌消毒
C. 綠色食品是指不含任何化學物質的食品
D. 在空氣質量日報中CO2含量屬于空氣污染指數
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】反應N2+O2![]() 2NO在恒容密閉容器中進行,達到平衡后,充入N2,下列說法正確的是
2NO在恒容密閉容器中進行,達到平衡后,充入N2,下列說法正確的是
A. 平衡向逆反應方向移動,N2和O2的轉化率都減小
B. 平衡向正反應方向移動,N2和O2的轉化率都增大
C. 壓強增大平衡不移動,N2的轉化率不變
D. 平衡向正反應方向移動,N2的轉化率減小,O2的轉化率增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一定條件下,向體積為2L的密閉容器中加入2 mol N2和10 mol H2發生如下反應:N2+3H2![]() 2NH3,2 min時測得剩余的N2為1mol,則化學反應速率的表示不正確的是
2NH3,2 min時測得剩余的N2為1mol,則化學反應速率的表示不正確的是
A.v(N2)=0.25 mol·L-1·min-1 B.v (H2)=0.0125 mol·L-1·s-1
C.v(NH3)=1.0 mol·L-1·min-1 D.v (H2)=0.75 mol·L-1·min-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】甲、乙、丙、丁、是由H+、Na+、Al3+、Ba2+、OH—、Cl—、HCO3—離子中的兩種組成,可以發生如圖轉化,下列說法不正確的是
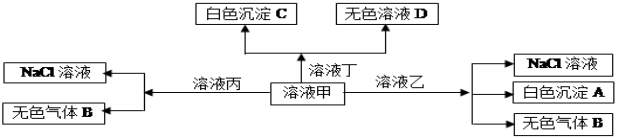
A.在丁中滴加甲開始反應的離子方程式:HCO3—+ Ba2++OH—= BaCO3↓+ H2O。
B.溶液丙中還可以大量共存的離子有:Fe2+、NO3—、SO42—
C.白色沉淀A可能溶解在溶液D中
D.甲為NaHCO3,乙為AlCl3
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com