
【題目】某化學教師為“氯氣與金屬鈉反應”設計了如圖裝置的實驗。實驗操作:先給鈉預熱,等鈉熔融成圓球時,撤火,通入氯氣,即可見鈉著火燃燒,生成大量白煙。以下敘述中錯誤的是
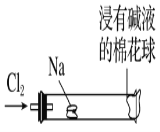
A.反應生成的大量白煙是氯化鈉晶體
B.玻璃管尾部塞一團浸有NaOH溶液的棉球是用于吸收過量的氯氣
C.鈉著火產生黃色火焰,自然界中存在游離態鈉
D.若在棉花球外沿滴一滴石蕊溶液,據其顏色變化判斷氯氣是否被堿液完全吸收
科目:高中化學 來源: 題型:
【題目】固體界面上強酸的吸附和離解是多相化學在環境、催化、材料科學等領域研究的重要課題。下圖為少量HCl氣體分子在253 K冰表面吸附和溶解過程的示意圖。下列敘述錯誤的是

A. 冰表面第一層中,HCl以分子形式存在
B. 冰表面第二層中,H+濃度為5×103 mol·L1(設冰的密度為0.9 g·cm3)
C. 冰表面第三層中,冰的氫鍵網格結構保持不變
D. 冰表面各層之間,均存在可逆反應HCl![]() H++Cl
H++Cl
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】亞硝酸鈉(NaNO2)是一種具有咸味、有毒,且價格比食鹽(NaCl)便宜的工業用鹽,常被誤作食鹽使用,導致多起中毒事故發生。它的部分性質見右圖,下列說法錯誤的是

A.可用淀粉碘化鉀試紙和食醋鑒別食鹽(NaCl)與亞硝酸鈉(NaNO2)
B.N2H4極易溶于水,因為它是極性分子且與水分子之間易形成氫鍵
C.NaNO2與N2H4生成NaN3的反應方程式為:NaNO2+N2H4 = NaN3 + 2H2O
D.上圖所涉及到的化學反應都是氧化還原反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】按下圖裝置進行實驗,并回答下列問題:

(1)判斷裝置的名稱:A池為___________ ;B池為______________;
(2)鋅極為________極,電極反應式為___________________________________;銅極為________極,電極反應式為___________________________________;石墨棒C1為______極,電極反應式為__________________________________;石墨棒C2附近發生的實驗現象為______________________________________;
(3)當C2極析出224mL氣體(標準狀態)時,鋅的質量變化_________(變大、不變或變小)了________g,CuSO4溶液的質量_________(增加、不變或減少)_________g。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知Cl2在70℃的NaOH水溶液中,能發生氧化還原反應后可生成NaClO與NaClO3現有63.9g Cl2,將其通入到足量70℃的NaOH水溶液中,反應完全后測得溶液中NaClO與NaClO3的物質的量比為4:1,并得到500mL溶液。
(1)寫出Cl2在70℃的NaOH水溶液中發生上述反應的化學方程式______。
(2)計算完全反應后溶液中NaClO、NaClO3物質的量濃度____、______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列內容與結論相對應的是
選項 | 內容 | 結論 |
A | H2O(g)變成H2O(l) | △S>0 |
B | 硝酸銨溶于水可自發進行 | 因為△S>0 |
C | 一個反應的△H>0,△S>0 | 反應一定不自發進行 |
D | H2(g)+F2(g)=2HF(g),△H=-271kJ/mol △S=8J/(mol·K) | 反應在任意外界條件下均可自發進行 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一定體積的密閉容器中,進行如下化學反應:CO2(g)+H2(g)CO(g)+H2O(g),其化學平衡常數K和溫度t的關系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列問題:
(1)該反應的化學平衡常數表達式為K= ______
(2)該反應為 ______ 反應(選填“吸熱”“放熱”).
(3)能判斷該反應是否達到化學平衡狀態的依據是 ______ .
A.容器中壓強不變 B.混合氣體中c(CO)不變
C.v正(H2)=v逆(H2O) D.c(CO2)=c(CO)
(4)某溫度下,平衡濃度符合c(CO2)c(H2)=c(CO)c(H2O),試判斷此時的溫度為 ______ ℃.在此溫度下2L密閉容器中進行反應CO2(g)+H2(g)CO(g)+H2O(g),CO2(g)和H2(g)的起始量均為2.0mol,達到平衡時CO2的轉化率為 ______ .
(5)在密閉容器中進行反應①Fe(s)+CO2(g)FeO(s)+CO(g)△H1=akJmol-1
反應②2CO(g)+O2(g)2CO2(g)△H2=b kJmol-1
反應③2Fe(s)+O2(g)2FeO(s)△H3
則△H3= ______ (用含a、b的代數式表示).
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)某同學用托盤天平稱量燒杯的質量,天平平衡后的狀態如圖。由圖中可以看出,該同學在操作時的一個錯誤是__,燒杯的實際質量為__(最小砝碼為5g)。

(2)已知某“84”消毒液瓶體部分標簽如圖所示,該“84”消毒液通常稀釋100倍(體積之比)后使用。請回答下列問題:
有效成分 | NaClO |
規格 | 1000mL |
質量分數 | 25% |
密度 | 1.19g·cm-1 |
①該“84”消毒液物質的量濃度約____ mol·L-1(保留一位小數)。
②某同學取20mL該“84”消毒液,稀釋后用于消毒,稀釋后的溶液中c(Na+)=__mol·L-1。
③“84”消毒液與稀硫酸混合使用可增強消毒能力,某消毒小組人員用濃硫酸配制稀硫酸用于增強“84”消毒液的消毒能力,下列操作使所配制的硫酸溶液濃度偏低的是__。
a.量取濃硫酸時,俯視量筒刻度線 b.未經冷卻就將溶液轉移至容量瓶
c.溶液定容搖勻后,有少量流出 d.沒有洗滌量取濃硫酸的量筒
e.定容時仰視容量瓶刻度線 f.容量瓶內殘留一定量蒸餾水
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】最近科學家利用下列裝置圖成功地實現了CO2和H2O合成CH4。下列敘述錯誤的是( )
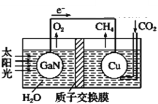
A. 電池工作時,實現了將太陽能轉化為電能
B. 銅電極為正極,電極反應式為CO2+4e-+8H+=CH4+2H2O
C. 電池內 H+ 透過質子交換膜從左向右移動
D. 為提高該人工光合系統的工作效率,可向裝置中加入少量稀硫酸
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com