
【題目】用 1~18 號元素及其形成的化合物的化學式填空.
(1)原子半徑最小的元素是_____.
(2)除稀有氣體外,原子半徑最大的元素是_____,它的原子結構示意圖 是_____.
(3)與水反應最劇烈的金屬是_____.
(4)最高價氧化物的水化物堿性最強的是_____.
(5)最高價氧化物的水化物為兩性氫氧化物的是_____.
(6)氣態氫化物的水溶液呈堿性的元素是_____.
(7)最穩定的氣態氫化物是_____.
(8)金屬性最強的元素是_____,非金屬性最強的元素是_____.
【答案】HNa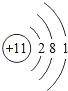 NaNaOHAl(OH)3NH3HFNaF
NaNaOHAl(OH)3NH3HFNaF
【解析】
(1)原子的電子層數越少,其原子半徑越小,同一周期元素中,原子半徑隨著原子序數增大而減小;(2)原子的電子層數越少,其原子半徑越小,同一周期元素中,原子半徑隨著原子序數增大而減小;(3)金屬性最強的元素是Na元素;(4)元素的金屬性越強,其最高價氧化物的水化物堿性越強;(5)最高價氧化物的水化物為兩性氫氧化物的是氫氧化鋁;(6)氣態氫化物的水溶液呈堿性的氣體是NH3;(7)非金屬性越強,氣態氫化物越穩定;(8)同周期,從左到右,金屬性減弱,同主族,從上到下,非金屬性減弱。
(1)原子的電子層數越少,其原子半徑越小,同一周期元素中,原子半徑隨著原子序數增大而減小,原子半徑最小的是H元素,故答案為:H;(2)原子的電子層數越少,其原子半徑越小,同一周期元素中,原子半徑隨著 原子序數增大而減小,最大的是Na元素,鈉原子結構示意圖為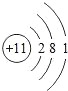 ,故答案為:Na;
,故答案為:Na; ;(3)金屬性最強的元素是 Na 元素,金屬性越強,性質越活潑,與水反應越劇 烈,故答案為:Na;(4)Na的金屬性最強,則NaOH 的堿性最強,故答案為:NaOH;(5)最高價氧化物的水化物為兩性氫氧化物的是氫氧化鋁;故答案為:Al(OH)3;(6)氣態氫化物的水溶液呈堿性的氣體是NH3;故答案為:NH3;(7)非金屬性越強,氣態氫化物越穩定,F 元素的非金屬性最強,故氟化氫最 穩定,故答案為:HF;(8)同周期,從左到右,金屬性減弱,同主族,從上到下,非金屬性減弱,故 金屬性最強的為鈉,非金屬性最強的元素是氟元素,故答案為:Na;F。
;(3)金屬性最強的元素是 Na 元素,金屬性越強,性質越活潑,與水反應越劇 烈,故答案為:Na;(4)Na的金屬性最強,則NaOH 的堿性最強,故答案為:NaOH;(5)最高價氧化物的水化物為兩性氫氧化物的是氫氧化鋁;故答案為:Al(OH)3;(6)氣態氫化物的水溶液呈堿性的氣體是NH3;故答案為:NH3;(7)非金屬性越強,氣態氫化物越穩定,F 元素的非金屬性最強,故氟化氫最 穩定,故答案為:HF;(8)同周期,從左到右,金屬性減弱,同主族,從上到下,非金屬性減弱,故 金屬性最強的為鈉,非金屬性最強的元素是氟元素,故答案為:Na;F。


 新題型全程檢測期末沖刺100分系列答案
新題型全程檢測期末沖刺100分系列答案科目:高中化學 來源: 題型:
【題目】有機物G是一種常用的植物調味油,可按如下路線合成:
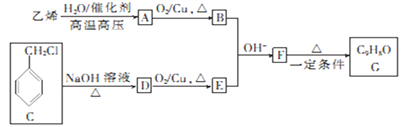
已知:![]()
回答下列問題:
(1)下列關于乙烯的說法不正確的是_________(填字母)。
a.分子中所有原子共平面
b.能發生氧化反應,不能發生還原反應
c.能發生加聚反應生成高分子
d.能使酸性高錳酸鉀溶液褪色
(2)由F生成G的反應類型為_________________________。
(3)C中官能團的名稱為___________,由C生成D的反應類型為___________。
(4)D的化學名稱為___________,由D生成E的化學方程式為___________。
(5)苯環上含有兩個取代基,且分子中含有酯基的F的同分異構體有_________種,其中核磁共振氫譜顯示有四組峰,且峰面積之比為3:2:2:3的是__________(填結構簡式)。
(6)參照上述合成路線,設計以B為原料(無極試劑任選)制備高吸水性樹脂![]() 的合成路線:________________。
的合成路線:________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列離子方程式書寫正確的是
A. 稀硝酸與鐵屑反應:2Fe+6H+=2Fe3++3H2↑
B. 往NH4HCO3溶液中加過量的NaOH溶液并加熱:NH4++OH-=NH3↑+H2O
C. 往酸性碘化鉀溶液中滴加適量的雙氧水:2I-+2H++H2O2=I2+2H2O
D. HS-的電離:HS-+H2O![]() OH-+HS-
OH-+HS-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X、Y、Z、M、W為五種短周期元素.X、Y、Z是原子序數依次遞增的同周期元素,且最外層電子數之和為15,X與Z可形成XZ2分子;Y與M形成的氣態化合物在標準狀況下的密度為0.76g/L;W的質子數是X、Y、Z、M四種元素質子數之和的一半。下列說法正確的是()
A. 原子半徑:W>Z>Y>X>M
B. 將XZ2通入W單質與水反應后的溶液中,一定只生成碳酸鈉
C. 由X、Y、Z、M四種元素形成的化合物中一定有共價鍵可能有離子鍵
D. CaX2、CaM2、CaZ2等3種化合物中,陽離子和陰離子個數比均為1:2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】信息時代產生的大量電子垃圾對環境構成了極大的威脅。某“變廢為寶”學生探究小組將一批廢棄的線路板簡單處理后,得到紅色金屬M和金屬E并進行如下框圖所示轉化,獲得高效凈水劑K2EO4。
(答題時,化學式及化學方程式中的M、E均用所對應的元素符號表示):
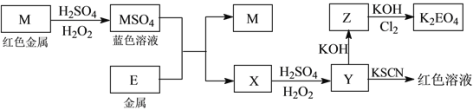
(1)寫出M溶于稀H2SO4和H2O2混合液的離子方程式:_______________________________。
(2)檢驗X中陽離子的方法和現象是__________________________________________________。
(3)某同學取X的溶液在空氣中放置后,酸化并加入KI和淀粉溶液,溶液變為藍色。寫出與上述變化過程相關的離子方程式:_______________________________、____________________________________。
(4)由MSO4的藍色溶液經一系列操作可以獲得藍色晶體,這些操作中用到的實驗儀器除了酒精燈、蒸發皿、鐵架臺外,還需要用到的玻璃儀器有________、________、 __________(填寫儀器名稱)。
(5)某同學利用H2還原MO來測定M的相對原子質量,下圖是測定裝置示意圖,A中試劑是鹽酸。
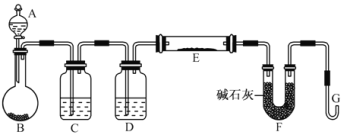
①儀器B中應裝入___________,裝置D的作用_________________________;
②連接好裝置并檢驗裝置的氣密性后,應首先“加熱反應管E”還是“從A瓶中逐滴加入液體” ?
___________________________在這兩步之間還應進行的操作是_________________________;
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列溶液中粒子的物質的量濃度關系正確的是( )
A. 0.1![]()
![]() 溶液與0.1
溶液與0.1![]()
![]() 溶液等體積混合,所得溶液中:
溶液等體積混合,所得溶液中:![]()
B. 20![]() 0.1
0.1![]()
![]() 溶液與10
溶液與10![]() 0.1
0.1![]()
![]() 溶液混合后溶液呈酸性,所得溶液中:
溶液混合后溶液呈酸性,所得溶液中:![]()
C. 室溫下,![]() 的鹽酸與
的鹽酸與![]() 的氨水等體積混合,所得溶液中:
的氨水等體積混合,所得溶液中:![]()
D. 0.1![]()
![]() 溶液與0.1
溶液與0.1![]()
![]() 溶液等體積混合,所得溶液中:
溶液等體積混合,所得溶液中:![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定溫度下,向容積固定為a L的密閉容器中充入1 mol X氣體和2 mol Y氣體,發生反應X(g)+2Y(g) ![]() 2Z(g),此反應達到平衡狀態的標志是( )
2Z(g),此反應達到平衡狀態的標志是( )
A. 容器內氣體密度不隨時間變化 B. 容器內各物質的濃度不隨時間變化
C. 容器內X、Y、Z的濃度之比為1∶2∶2 D. 單位時間內消耗0.1 mol X,同時生成0.2 mol Z
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】恒溫條件下,可逆反應:2NO(g)+O2(g) ![]() 2NO2(g)在體積固定的密閉容器中進行,達到平衡狀態的標志的是
2NO2(g)在體積固定的密閉容器中進行,達到平衡狀態的標志的是
①NO的體積分數不再改變的狀態 ②單位時間內生成n mol O2的同時生成2n mol NO
③混合氣體的顏色不再改變的狀態 ④混合氣體的密度不再改變的狀態
⑤混合氣體的平均相對分子質量不再改變的狀態
A. ①③⑤ B. ②③⑤ C. ①④⑤ D. 全部
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com