
【題目】有機化合物G常用作香料,合成G的一種路線如下:

已知以下信息:
①A的分子式為C5H8O,核磁共振氫譜顯示其有兩種不同化學環境的氫
②CH3CH2CH=CH2![]() CH3CHBrCH=CH2
CH3CHBrCH=CH2
③![]()
回答下列問題:
(1)A的結構簡式為____________,D中官能團的名稱為____________。
(2)B→C的反應類型為__________。
(3)D→E反應的化學方程式為__________________________________________。
(4)檢驗M是否已完全轉化為N的實驗操作是_____________________________________________________________________________________________________________。
(5)滿足下列條件的L的同分異構體有____________種(不考慮立體異構),①能發生銀鏡反應 ②能發生水解反應,③屬于芳香族化合物,其中核磁共振氫譜中有5組峰,且峰面積之比為1:2:2:2:3的所有可能結構的結構簡式____________________________________。
(6)參照上述合成路線,設計一條以1-丁醇和NBS為原料制備順丁橡膠
![]() 的合成路線:_____________________
的合成路線:_____________________
【答案】![]() 碳碳雙鍵、氯原子消去反應
碳碳雙鍵、氯原子消去反應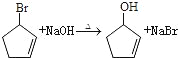 取少量試樣于試管中,滴加稀NaOH至溶液呈堿性,再加入新制Cu(OH)2加熱至沸,若沒有磚紅色沉淀產生,說明M已完全轉化為N,否則M未完全轉化為N14
取少量試樣于試管中,滴加稀NaOH至溶液呈堿性,再加入新制Cu(OH)2加熱至沸,若沒有磚紅色沉淀產生,說明M已完全轉化為N,否則M未完全轉化為N14![]() CH3CH2CH2CH2OH
CH3CH2CH2CH2OH![]() CH3CH2CH=CH2
CH3CH2CH=CH2![]() CH3CHBrCH=CH2
CH3CHBrCH=CH2![]() CH2=CHCH=CH2
CH2=CHCH=CH2![]()
![]()
【解析】由G的結構簡式可知E、N分別為![]() 、
、![]() 中的一種,K發生信息③中的轉化得到M,M發生催化氧化生成N為羧酸,故N為
中的一種,K發生信息③中的轉化得到M,M發生催化氧化生成N為羧酸,故N為![]() ,E為
,E為![]() ,逆推可知M為
,逆推可知M為![]() ,L為
,L為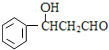 ,K為
,K為![]() .A的分子式為C5H8O,核磁共振氫譜顯示其有兩種不同化學環境的氫,能與氫氣發生加成反應,系列轉化得到E,可知A為
.A的分子式為C5H8O,核磁共振氫譜顯示其有兩種不同化學環境的氫,能與氫氣發生加成反應,系列轉化得到E,可知A為![]() ,則B為
,則B為![]() ,結合信息②可知,B發生消去反應生成C為
,結合信息②可知,B發生消去反應生成C為![]() ,C與NBS發生取代反應生成D為
,C與NBS發生取代反應生成D為![]() ,D在氫氧化鈉水溶液、加熱條件下發生水解反應生成E.
,D在氫氧化鈉水溶液、加熱條件下發生水解反應生成E.
(1)由上述分析可知,A的結構簡式為![]() ,D為
,D為![]() ,D中官能團的名稱為:碳碳雙鍵、氯原子;
,D中官能團的名稱為:碳碳雙鍵、氯原子;
(2)由上述分析可知,B→C的反應類型為消去反應;
(3)D→E反應的化學方程式為: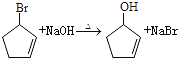 ;
;
(4)M轉化為N是醛基轉化為羧基,可以檢驗反應后物質是否含有醛基判斷M是否已完全轉化為N,實驗操作是:取少量試樣于試管中,滴加稀NaOH至溶液呈堿性,再加入新制Cu(OH)2加熱至沸,若沒有磚紅色沉淀產生,說明M已完全轉化為N,否則M未完全轉化為N;
(5)滿足下列條件的L(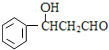 )的同分異構體:①能發生銀鏡反應,說明含有醛基,②能發生水解反應,含有甲酸形成的酯基,③屬于芳香族化合物,含有苯環,含有一個取代基為-CH2CH2OOCH,或者為-CH(CH3)OOCH,含有2個取代基為-CH3、-CH2OOCH,或者為-CH2CH3、-OOCH,各有鄰、間、對3種,可以含有3個取代基為2個-CH3、1個-OOCH,2個-CH3有鄰、間、對3種,對應的-OOCH分別有2種、3種、1種位置,故符合條件的同分異構體共有14種,其中核磁共振氫譜中有5組峰,且峰面積之比為1:2:2:2:3的結構簡式為
)的同分異構體:①能發生銀鏡反應,說明含有醛基,②能發生水解反應,含有甲酸形成的酯基,③屬于芳香族化合物,含有苯環,含有一個取代基為-CH2CH2OOCH,或者為-CH(CH3)OOCH,含有2個取代基為-CH3、-CH2OOCH,或者為-CH2CH3、-OOCH,各有鄰、間、對3種,可以含有3個取代基為2個-CH3、1個-OOCH,2個-CH3有鄰、間、對3種,對應的-OOCH分別有2種、3種、1種位置,故符合條件的同分異構體共有14種,其中核磁共振氫譜中有5組峰,且峰面積之比為1:2:2:2:3的結構簡式為![]() ;
;
(6)參照上述合成路線,設計一條以1-丁醇和NBS為原料制備順丁橡膠(![]() )的合成路線:CH3CH2CH2CH2OH
)的合成路線:CH3CH2CH2CH2OH![]() CH3CH2CH=CH2
CH3CH2CH=CH2![]() CH3CHBrCH=CH2
CH3CHBrCH=CH2![]() CH2=CHCH=CH2
CH2=CHCH=CH2![]()
![]() 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】氯化亞銅(CuCl)常用作有機合成工業中的催化劑。有關資料為:
①CuCl為微溶于水的白色固體,在空氣中可被迅速氧化
②CuOH為難溶于水的黃色固體,易分解為紅色的Cu2O
③Cu+可與濃氨水反應生成Cu(NH3)2+(無色),該無色物質在空氣中易被氧化為藍色
I. 甲小組同學用如下裝置電解食鹽水,并對電解產物進行研究。
實驗裝置 | 電解質溶液 | 實驗現象 | |
| 5mol/L NaCl溶液 | a極附近 | b極附近 |
開始時,產生白色渾濁并逐漸增加,當沉入U型管底部時部分沉淀變為橙黃色;隨后a極附近沉淀自下而上也變為橙黃色 | 產生無色氣泡 | ||
(1)若a極附近生成的白色渾濁是CuCl,則銅絲a應與電源的________極相連,銅絲a的電極反應式是____。
(2)b極附近溶液的pH_________(填“增大”、“減小”或“不變”)。
(3)橙黃色沉淀中含有Cu2O,則CuCl轉化為Cu2O的原因是_____________(用方程式表示)。
(4)a極附近沉淀自下而上變為橙黃色原因是____________。
II. 乙小組同學通過以下方案制取CuCl并對其組成進行研究。
將Na2SO3的水溶液逐滴加入CuCl2的水溶液中,再加入少量濃鹽酸調節到pH=3左右,即可得到白色沉淀CuCl。
(1)寫出產生CuCl的離子方程式______________。
(2)為了提高CuCl的產率,可采用________法快速過濾,生產過程中調節溶液的pH不能過大的原因是___。
(3)為探究白色沉淀的化學組成,將制得的白色沉淀溶于濃氨水,得到無色溶液,將無色溶液分成兩份,一份放置于空氣中,一段時間后溶液變為藍色;另一份的實驗方法及現象為_____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列離子方程式正確的是
A. 碳酸氫銨溶液與足量氫氧化鈉溶液混合后加熱:NH4++OH-![]() NH3↑+H2O
NH3↑+H2O
B. 將少量氯化鐵溶液滴入硫化鈉溶液中:2Fe3++S2-=2Fe2++S↓
C. 向Fe(NO3)2稀溶液中加入鹽酸:3Fe2++4H+ + NO3-=3Fe3++2H2O+NO↑
D. 次氯酸鈣溶液中通入過量二氧化碳:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】次磷酸(H3PO2)是一元中強酸,具有較強還原性,下列有關說法正確的是( )
A. 次磷酸的電離方程式為:H3PO2=H++H2PO2-
B. NaH2PO2是次磷酸的正鹽,其水溶液呈中性
C. 白磷與氫氧化鈉溶液反應可得次磷酸鹽,反應的化學方程式為:
P4+9NaOH=3Na2PO2+PH3↑+3H2O
D. 利用(H3PO2)進行化學鍍銀反應中,1mol H3PO2最多還原4mol Ag+離子
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數的值。下列說法正確的是( )
A. 136g熔融的KHSO4中含有2NA個陽離子
B. 40gH218O與40gD2O所含的中子數均為20NA
C. 1molFe分別與足量的稀硫酸和稀硝酸反應轉移電子數均為2NA
D. 標準狀況下,22.4LNO和11.2LO2混合后氣體的分子總數為NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知反應X+Y=M+N為放熱反應,對該反應的下列說法中正確的是
A. X的能量一定高于M
B. Y的能量一定高于N
C. X和Y的總能量一定高于M和N的總能量
D. 因該反應為放熱反應,故不必加熱就可發生
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向一定量的Fe、FeO、Fe3O4的混合物中加入100mL1molL﹣1的鹽酸,恰好使混合物完全溶解,放出224mL(標準狀況)的氣體,在所得溶液中加入KSCN溶液無血紅色出現.若用足量的CO在高溫下還原相同質量的此混合物,能得到鐵的質量是( )
A.11.2g B.5.6g C.2.8g D.無法計算
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com