
【題目】化合物X是一種藥物合成的中間體,其結構簡式如圖所示。下列有關化合物X的說法正確的是( )
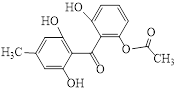
A. 化合物X的分子式為C16H16O6
B. 能發生加成反應、取代反應、消去反應
C. 1mol化合物X最多可與5molNaOH、7mol H2、4molBr2發生反應
D. 可與FeCl3溶液發生顯色反應,但不能發生氧化反應
 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
【題目】碳及其化合物在研究和生產中有許多重要用途.請回答下列問題:
(1)基態碳原子核外電子有__種空間運動狀態,其價電子排布圖為__.
(2)光氣的分子式為COCl2,又稱碳酰氯,是一種重要的含碳化合物,判斷其分子立體構型為__,其碳原子雜化軌道類型為_____雜化.
(3)碳酸鹽在一定溫度下會發生分解,實驗證明碳酸鹽的陽離子不同,分解溫度不同,如下表所示:
碳酸鹽 | MgCO3 | CaCO3 | BaCO3 | SrCO3 |
熱分解溫度/℃ | 402 | 900 | 1172 | 1360 |
陽離子半徑/pm | 66 | 99 | 112 | 135 |
試解釋為什么隨著陽離子半徑的增大,碳酸鹽的分解溫度逐步升高?。 ______________
(4)碳的一種同素異形體﹣﹣C60,又名足球烯,是一種高度對稱的球碳分子.立方烷(分子式:C8H8結構是立方體:![]() 是比C60約早20年合成出的一種對稱型烴類分子,而現如今已合成出一種立方烷與C60的復合型分子晶體,該晶體的晶胞結構如圖所示,立方烷分子填充在原C60晶體的分子間八面體空隙中.則該復合型分子晶體的組成用二者的分子式可表示為__。
是比C60約早20年合成出的一種對稱型烴類分子,而現如今已合成出一種立方烷與C60的復合型分子晶體,該晶體的晶胞結構如圖所示,立方烷分子填充在原C60晶體的分子間八面體空隙中.則該復合型分子晶體的組成用二者的分子式可表示為__。

(5)碳的另一種同素異形體——石墨,其晶體結構如圖所示,則石墨晶胞含碳原子個數為__個.已知石墨的密度為ρg·cm﹣3,C﹣C鍵長為rcm,阿伏加德羅常數的值為NA,計算石墨晶體的層間距為__cm.
(6)金剛石和石墨的物理性質差異很大,其中:熔點較高的是___________,試從結構分析___________;硬度大的是___________,其結構原因是___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)溫室效應是導致海平面上升的主要原因,引起溫室效應的人為因素主要是 。
(2)為了控制溫室效應,各國科學家提出了不少方法和設想。有人根據液態CO2密度大于海水密度的事實,設想將CO2液化后,送入深海海底,以減小大氣中CO2的濃度。為使CO2液化,可采用的措施是 (填字母)。
A.減壓、升溫 B.增壓、升溫
C.減壓、降溫 D.增壓、降溫
(3)科學家致力于二氧化碳的“組合轉化”技術研究,把過多的二氧化碳轉化為有益于人類的物質。如將CO2和H2以1∶4的比例混合,通入反應器。在適當的條件下反應,可獲得一種重要的能源。請完成以下化學方程式CO2+4H2![]() +2H2O。 若將CO2與H2混合,在一定條件下以1∶3的比例發生反應,可生成某種重要的化工原料和水,該化工原料可能是 (填字母)。
+2H2O。 若將CO2與H2混合,在一定條件下以1∶3的比例發生反應,可生成某種重要的化工原料和水,該化工原料可能是 (填字母)。
A.甲烷 B.乙烯 C.乙醇 D.苯
(4)下列措施能快速、有效地減緩大氣中CO2增加的是 。
A.使用天然氣等燃料
B.控制全球人口增長
C.植樹造林,保護森林
D.立即減少煤和石油的燃燒
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列敘述合理的是( )
A. 金屬材料都是導體,非金屬材料都是絕緣體
B. 棉、麻、絲、毛及合成纖維完全燃燒都只生成CO2和H2O
C. 水電站把機械能轉化成電能,而核電站把化學能轉化成電能
D. 我國規定自2008年6月1日起,商家不得無償提供塑料袋,目的是減少“白色污染”
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列五種烴:①正丁烷②異丁烷③丙烷④辛烷⑤乙烷,按它們的沸點由高到低的順序排列為
A. ④①②③⑤ B. ①④②③⑤ C. ⑤③②①④ D. ④①③⑤②
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某元素的一種核素X 的質量數為A,含N個中子,它與1H 原子組成HmX 分子。在a g HmX中所含質子的物質的量是
A. ![]() mol B.
mol B. ![]() mol
mol
C. ![]() mol D.
mol D. ![]() mol
mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】空氣吹出法工藝,是目前“海水提溴”的最主要方法之一。其工藝流程如下:

(1)步驟③的離子方程式:_________________________________。
(2)步驟⑤中溴蒸氣冷凝后得到液溴與溴水的混合物,可利用它們的相對密度相差很大的特點進行分離。分離儀器的名稱是________。
(3)溴水混合物Ⅱ中溶有一定量的氯氣,因此在步驟⑤中可將蒸餾產生的氣體通過________(填試劑名稱)溶液,以除去氯氣。
(4)步驟⑤的蒸餾過程中,溫度應控制在80~90 ℃。溫度過高或過低都不利于生產,請解釋原因:___________________________。
(5)步驟①中用硫酸酸化可提高Cl2的利用率,理由是_______________________。
(6)提取溴單質,采用蒸餾“溴水混合物Ⅱ”而不是蒸餾“溴水混合物Ⅰ”,請說明原因:
______________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫酸鎳晶體(NiSO47H2O)可用于電鍍工業,可用含鎳廢催化劑為原料來制備。已知某化工廠的含鎳廢催化劑主要含有Ni,還含有Al、Fe的單質及其他不溶雜質(不溶于酸堿)。某小組通過查閱資料,設計了如下圖所示的制備流程:

已知: Ksp[Fe(OH)3]=4.0×10-38 ,Ksp[Ni(OH)2]=1.2×10-15
(1)“堿浸”過程中發生反應的離子方程式是_______________________________。
(2)操作a所用到的玻璃儀器有燒杯、________、________;操作c的名稱為____________、____________、過濾、洗滌。
(3)固體①是______________;加H2O2的目的是(用離子方程式表示)_____________。
(4)調pH為2-3時所加的酸是________。
(5)操作b為調節溶液的pH,若經過操作b后溶液中c(Ni2+)=2mol·L-1,當鐵離子恰好完全沉淀溶液中c(Fe3+)=1.0×10-5mol·L-1時,溶液中是否有Ni(OH)2沉淀生成?________(填“是”或“否”)。
(6)NiSO47H2O可用于制備鎳氫電池(NiMH),鎳氫電池目前已經成為混合動力汽車的一種主要電池類型.NiMH中的M表示儲氫金屬或合金.該電池在放電過程中總反應的化學方程式是NiOOH+MH=Ni(OH)2+M,則NiMH電池充電過程中,陽極的電極反應式為_______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:D為烴;E分子中碳元素與氫元素的質量之比6∶1,相對分子質量為44,其燃燒產物只有CO2和H2O。A的最簡式與F相同,且能發生銀鏡反應,可由淀粉水解得到。

(1)A的結構簡式為__________________。
(2)寫出D→E的化學方程式:_______________________。
(3)下列說法正確的是____。
A.有機物F能使石蕊溶液變紅
B.用新制的氫氧化銅無法區分有機物C、E、F的水溶液
C.等物質的量的C和D分別完全燃燒消耗氧氣的量相等
D.可用飽和碳酸鈉溶液除去有機物B中混有的少量C、F
E. B的同分異構體中能發生銀鏡反應的酯類共有2種
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com