
【題目】有關如圖所示裝置的敘述不正確的是( ) 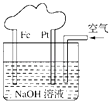
A.這是一個原電池裝置
B.該裝置中Pt為正極,電極反應為:O2+2H2O+4e﹣═4OH﹣
C.該裝置中Fe為負極,電極反應為:Fe﹣2e﹣+2OH﹣═Fe(OH)2
D.這是電解NaOH溶液的裝置
科目:高中化學 來源: 題型:
【題目】我國宋代《夢溪筆談》中記敘了膽礬和銅的煉制過程:“信州鉛山縣有苦泉,煮之則得膽礬。熬膽礬鐵釜,久之亦化為銅。”該煉制過程中沒有涉及到的變化是( )
A. 復分解反應B. 氧化還原反應C. 置換反應D. 蒸發結晶
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硝酸是一種重要的化工原料,工業上生產硝酸的過程如下:
(1)以氮氣、氫氣為原料合成氨①下列措施可以提高H2的轉化率是(填選項序號) .
a.選擇適當的催化劑 b.增大壓強 c.及時分離生成的NH3d.升高溫度
②一定溫度下,在密閉容器中充入1molN2和3molH2發生反應.若容器容積恒定,達到平衡狀態時,容器內的壓強是原來的 ![]() ,則N2的轉化率a1=;
,則N2的轉化率a1=;
若容器壓強恒定,達到平衡狀態時,N2的轉化率為a2 , 則a2a1(填“>”、“<”或“=”)
(2)以氨氣、空氣為主要原料制硝酸.在容積恒定的密閉容器中進行反應2NO(g)+O2(g)2NO2(g)△H>0
該反應的反應速率(v)隨時間(t)變化的關系如下圖所示.若t2、t4時刻只改變一個條件,下列說法正確的是(填選項序號) . 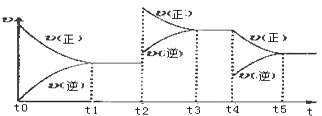
a.在t1~t2時,可依據容器內氣體的壓強保持不變判斷反應已達到平衡狀態
b.在t2時,采取的措施一定是升高溫度
c.在t3~t4時,可依據容器內氣體的密度保持不變判斷反應已達到平衡狀態
d.在t0~t5時,容器內NO2的體積分數在t3時值的最大
(3)硝酸廠常用如下2種方法處理尾氣.①催化還原法:催化劑存在時用H2將NO2還原為N2 .
已知:2H2(g)+O2(g)=2H2O(g)△H=﹣483.6kJ/mol
N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ/mol
則H2還原NO2生成水蒸氣反應的熱化學方程式是 .
②堿液吸收法:用Na2CO3溶液吸收NO2生成CO2 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】W、X、Y、Z是四種常見的短周期主族元素,其原子半徑隨原子序數的變化如圖所示。
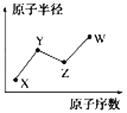
已知Y、Z兩種元素的單質是空氣的主要成分,W原子的最外層電子數與Ne原子的最外層電子數相差1。請回答下列問題:
(1)寫出四種元素的元素符號:W________;X________;Y________;Z________。
(2)四種元素的所有化合價中,最低負化合價為________價,最高正化合價為________價。
(3)甲和乙分別是由W、X、Y、Z四種元素中的三種元素組成的常見化合物,化合物甲具有消毒殺菌作用,其化學式為________;化合物乙是一種常見的化肥,其化學式為________。
(4)HYO3的酸性比HWO強,有人據此認為Y的非金屬性強于W,你認為這種看法是否正確,說明理由:________ 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X、Z、Q、R、T、U分別代表原子序數依次增大的短周期元素,周期表的全部元素中X的原子半徑最小,X與R的最外層電子數相等;Z的內層電子數是最外層電子數的一半,U的最高化合價和最低化合物的代數和為6;R和Q可形原子數之比為1:1和2:1的兩種化合物;R、T、U三者的最高價氧化物對應的水化物兩兩之間能發生化學反應.請回答下列問題:
(1)T元素在期表中的位置是________;由上述元素中的四種元素形成的既含有離子鍵又含有共價鍵的化合物為________(寫出其中一種物質的名稱).
(2)X、Z、Q三種元素的原子半徑由小到大順序為________(填元素符號).
(3)T、U兩元素最高價氧化物對應的水化物反應的離子方程式為________.
(4)下列可以判斷R和T金屬性強弱的是________(填序號).
a.單質的熔點R比T低 b.單質與酸反應時,失電子數R比T少
c.單質與水反應R比T劇烈 d.最高價氧化物的水化物的堿性R比T強
(5)某同學用Q、R兩元素的單質反應生成固體物質R2Q2,R2Q2屬于離子化合物,且能與化合物X2Q反應生成Q的單質.R2Q2的電子式為________;R2Q2與X2Q反應的化學方程式為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于下圖實驗裝置的說法正確的是( )
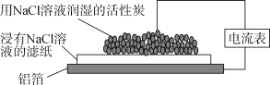
A.該裝置電流表中沒有電流通過
B.鋁箔是正極
C.總反應為4Al+3O2+6H2O===4Al(OH)3
D.電子從鋁箔流出,經電流表、活性炭、濾紙回到鋁箔
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有前四周期A、B、C、D、E、X六種元素,已知B、C、D、E、A五種非金屬元素原子半徑依次減小,其中B的s能級上電子總數等于p能級上電子總數的2倍.X原子的M能層上有4個未成對電子.請回答下列問題: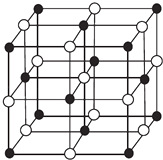
(1)寫出C、D、E三種原子第一電離能由大到小的順序為 . (用元素符號表示)
(2)A原子與B、C、D原子形成最簡單化合物的穩定性由強到弱的順序為(用分子式表示),根據價層電子對互斥理論預測BA2D的分子構型為 .
(3)某藍色晶體,其結構特點是X2+、X3+離子分別占據六面體互不相鄰的頂點,而六面體的每條棱上均有一個BC﹣ . 與A同族且相隔兩個周期的元素R的離子位于立方體的恰當位置上.根據其結構特點可知該晶體的化學式為(用最簡正整數表示) .
(4)科學家通過X射線探明,KCl、MgO、CaO、TiN的晶體結構與NaCl的晶體結構相似(如圖所示),其中3種離子晶體的晶格能數據如下表:
離子晶體 | NaCl | KCl | CaO |
晶格能/kJmol﹣1 | 786 | 715 | 3401 |
根據表格中的數據:判斷KCl、MgO、TiN三種離子晶體熔點從高到低的順序是 . MgO晶體中一個Mg2+周圍和它最鄰近且等距離的O2﹣有個.
(5)研究物質磁性表明:金屬陽離子含未成對電子越多,則磁性越大,磁記錄性能越好.離子型氧化物V2O5和Cr2O3中,適合作錄音帶磁粉原料的是 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知氯化銀、溴化銀的溶解度分別是1.5×10﹣4g和8.4×10﹣6g,將氯化銀和溴化銀的飽和溶液等體積混合,再加入足量濃硝酸銀溶液,則發生的反應為( )
A.只有溴化銀沉淀生成
B.氯化銀河溴化銀沉淀等量生成
C.氯化銀沉淀多于溴化銀沉淀
D.氯化銀沉淀少于溴化銀沉淀
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com