
【題目】亞硝酸氯(ClNO)是有機合成中的重要試劑。亞硝酸氯可由NO與Cl2在通常條件下反應得到,化學方程式為2NO(g)+Cl2(g)![]() 2ClNO(g)。
2ClNO(g)。
(1)氮氧化物與懸浮在大氣中的海鹽粒子相互作用時會生成亞硝酸氯,涉及如下反應:
①4NO2(g)+2NaCl(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g) K1
2NaNO3(s)+2NO(g)+Cl2(g) K1
②2NO2(g)+NaCl(s)![]() NaNO3(s)+ClNO(g) K2
NaNO3(s)+ClNO(g) K2
③2NO(g)+Cl2(g)![]() 2ClNO(g) K3
2ClNO(g) K3
則K1,K2,K3之間的關系為K3=______________。
(2)T℃時,2NO(g)+Cl2(g)![]() 2ClNO(g)的正反應速率表達式為v正= k cn(ClNO),測得速率和濃度的關系如下表:
2ClNO(g)的正反應速率表達式為v正= k cn(ClNO),測得速率和濃度的關系如下表:
序號 | c(ClNO)/mol·L-1 | v/mol·L-1·s-1 |
① | 0.30 | 3.6×10-8 |
② | 0.60 | 1.44×10-7 |
③ | 0.90 | 3.24×10-7 |
n=____________;k=____________(注明單位)。
(3)在2L的恒容密閉容器中充入4molNO(g)和2molCl2(g),在不同溫度下測得c(ClNO)與時間的關系如圖A:


①溫度為T1時,能作為該反應達到平衡的標志的有 ;
a.容器體積保持不變
b.容器壓強保持不變
c.平衡常數K保持不變
d.氣體顏色保持不變
e.v(ClNO)= v(NO)
f.NO與 ClNO的物質的量比值保持不變
②反應開始到10min時Cl2的平均反應速率v(Cl2
③溫度為T2時,10min已經達到平衡,該反應的平衡常數K=____________(注明單位)。
(4)一定條件下在恒溫恒容的密閉容器中按一定比例充入NO(g)和Cl2(g),平衡時ClNO的體積分數φ隨n(NO)/n(Cl2)的變化圖象如圖B,則A、B、C三狀態中,NO的轉化率最小的是__________點,當n(NO)/n(Cl2)=2.8時,達到平衡狀態ClNO的體積分數φ可能是D、E、F三點中的_________點。
【答案】(1)K22/K1
(2)n=2;k=4.0×10-7mol-1·L·s-1(注明單位)。
(3)①bdf;②0.05mol·L-1·min-1;③2L/mol(注明單位)。
(4)C點 F點。
【解析】
試題分析:
(1)已知:①4NO2(g)+2NaCl(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g)
2NaNO3(s)+2NO(g)+Cl2(g)
②2NO2(g)+NaCl(s)![]() NaNO3(s)+ClNO(g)
NaNO3(s)+ClNO(g)
將②×2-①可得③:2NO(g)+Cl2(g)![]() 2ClNO(g),平衡常數K3=K22/K1。
2ClNO(g),平衡常數K3=K22/K1。
(2)根據數據,結合正反應速率表達式為v正=k·cn(ClNO)可知,3.60×10-8mo1/(L·s)=k×(0.3mo1/L)n,1.44×10-7mo1/(L·s)=k×(0.6mo1/L)n,解得n=2,k=4.0×10-7L/(mo1·s);
(3)根據圖A可知,溫度越高,c(ClNO)越小,說明2NO(g)+Cl2(g)![]() 2ClNO(g)為放熱反應,且正反應方向的氣體系數減小。
2ClNO(g)為放熱反應,且正反應方向的氣體系數減小。
①a.2L的恒容密閉容器,容器體積始終保持不變,不能作為該反應達到平衡的標志;b.隨著反應進行,容器總壓強逐漸減小,當容器壓強保持不變時,說明反應已經達到平衡狀態;c.平衡常數K只與溫度有關,溫度為T1時,K保持不變,不能作為該反應達到平衡的標志;d.氣體顏色保持不變,即說明c(Cl2)保持不變,反應已經達到平衡狀態;e.NO和ClNO的系數相同,則有任何時候v(ClNO)= v(NO),不能作為該反應達到平衡的標志;f.NO與 ClNO的物質的量比值保持不變,說明反應已經達到平衡狀態;故選bdf。
②反應開始到10min時,c(C1NO)=1mol/L,則v(C1NO)= ![]() =0.1mol/(L·min),則Cl2的平均反應速率v(Cl2)=
=0.1mol/(L·min),則Cl2的平均反應速率v(Cl2)=![]() v(C1NO)=0.05mol/(L·min);
v(C1NO)=0.05mol/(L·min);
③ 2NO(g)+Cl2(g)![]() 2ClNO(g)
2ClNO(g)
起始(mol/L) 2 1 0
反應(mol/L) 1 0.5 1
平衡(mol/L) 1 0.5 1
T2時該反應的平衡常數K=![]() =
=![]() =2L/mol;
=2L/mol;
(4)n(NO)/n(C12)的比值越大,NO的轉化率越小,NO的轉化率最小的是C點。根據曲線的變化趨勢,當n(NO)/n(C12)=2.8,達到平衡狀態ClNO的體積分數是F。


 快樂暑假暑假能力自測中西書局系列答案
快樂暑假暑假能力自測中西書局系列答案科目:高中化學 來源: 題型:
【題目】下列有關水和無機鹽的敘述,不正確的是
A. 參與運輸營養物質和代謝廢物的水為自由水
B. 生物體內許多化學反應需要水的參與,結合水是細胞結構的組成成分之一
C. Mg2+是葉綠素、血紅蛋白等分子的組成成分
D. 細胞中大多數無機鹽以離子形式存在
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】圖為鐵在稀硫酸中被腐蝕時的不同情況,其中腐蝕速率由慢到快的順序是( )
A.①②③⑤⑥④ B.⑤②①⑥③④ C.⑤②③⑥①④ D.④③⑥②①⑤
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1,下列說法正確的是( )
A.CO的燃燒熱為-283 kJ·mol-1
B.CO的燃燒熱為566 kJ·mol-1
C.CO的燃燒熱ΔH=-283 kJ·mol-1
D.如圖可表示由CO生成CO2的反應過程和能量關系
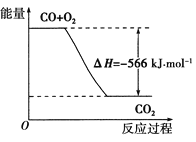
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ.某溫度時,在2 L容器中,某一化學反應中A、B的物質的量隨時間變化的曲線如圖所示,由圖中數據分析得:

(1)在4 min末時,A、B的物質的量濃度c(A)________c(B),從0~4 min內A、B的物質的量濃度變化量Δc(A)________Δc(B)(以上填“>”“<”或“=”)。
(2)從反應開始至4 min時,A的平均反應速率為________。
(3)該反應的化學方程式為__________________。
Ⅱ.將等物質的量的A、B混合放于2 L的密閉容器中,發生反應3A(g)+B(g)==X C(g)+2D(g)。經5 min后測得D的濃度為0.5 mol·L-1,c(A)∶c(B)=3∶5,v(C)=0.1 mol·L-1·min-1。
則:(1)X=________。
(2)前5 min內B的反應速率v(B)=________。5 min時A的轉化率為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】 常溫下,將pH=3 的硫酸與pH=9的NaOH 溶液混合,若要得到PH = 7 的溶液,混合時硫酸酸與NaOH 溶液的體積比為
A.1: 200 B.200 : 1 C.100 : 1 D.1:100
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知碳元素的單質有金剛石、石墨和足球烯(C60)等,含氧元素的單質有O2、O3,下列說法不正確的是( )
A.一種元素可以形成兩種或兩種以上不同的單質
B.單質的種類一定多于元素的種類
C.只含有一種元素的物質不一定是純凈物
D.只含有碳元素的物質在氧氣中燃燒只能生成一種物質
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關組成生物體化學元素的論述,正確的是( )
A. 人、動物與植物所含的化學元素的種類差異很大
B. 不同生物體內各種化學元素的含量比例基本相似
C. 組成生物體的化學元素在無機自然界都可以找到
D. 組成生物體和組成無機自然界的化學元素中,碳元素的含量最多
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用下圖裝置,進行NH3與金屬氧化物MxOy反應生成M、N2、H2O,通過測量生成水的質量來測定M的相對原子質量。a中試劑是濃氨水。


(1)儀器a的名稱為 ,儀器b中裝入的試劑可以是 。
(2)按氣流方向正確的裝置連接順序為(填序號,裝置可重復使用): 。
(3)裝置C的作用: 。
(4)實驗結束時,應首先 (填序號);這樣做的原因是 。
Ⅰ.熄滅A裝置的酒精燈 Ⅱ.停止從a中滴加液體
(5)若金屬氧化物為CuO,反應的化學方程式為 。
(6)若實驗中準確稱取金屬氧化物的質量為m g,完全反應后,測得生成水的質量為n g,則M的相對原子質量為 (用含x、y、m、n的式子表示)。
(7)某同學仔細分析上述裝置后認為仍存在缺陷,你認為該如何改進? 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com