
【題目】I、為測定金屬鈉樣品(表面有 Na2O)中鈉單質的質量分數,設計了如下實驗(反應裝置如右圖 所示):
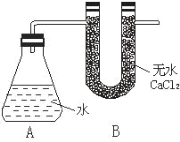
①稱量 A、B 的總質量
②稱取一定質量的鈉樣品
③將鈉樣品投入錐形瓶中,迅速塞緊帶 U 形干燥管(內含無水 CaCl2 干燥 劑)的橡皮塞 有關數據是:稱取的金屬鈉樣品質量為 a g,A、B 反應前總質量為 b g,反應后 A、B 的總質量為 c g。 請根據題意回答下列問題:
(1)A 中鈉和水反應過程可看到鈉熔成閃亮的小球,產生這一現象原因是:_____________
(2)用 a、b、c 表示的鈉單質的質量分數為_______________
(3)如果沒有 B 裝置對實驗結果有何影響___________。(填“偏大”或“偏小”“不影響”)
II、現用金屬鈉和空氣制備純度較高的 Na2O2,可利用的裝置如下圖。回答下列問題:
(提示:Na2O2 可以與 H2O、CO2 反應)
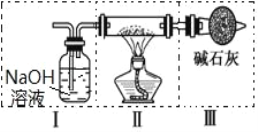
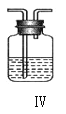
(4)上述裝置Ⅳ中盛放的試劑是_____,為完成實驗應將裝置Ⅳ接在_____(填寫字母號)。
A.I 之前 B. I 和 II 之間 C. II 和 III 之間 D. III 之后
(5)點燃酒精燈后,觀察到裝置 II 中的現象為_____。
(6)裝置 II 中 Na 生成 Na2O2 的化學反應方程式為_____。
【答案】該反應為放熱,鈉的熔點低23(a+b-c)/a偏大濃硫酸B鈉熔化成光亮的小球,劇烈燃燒產生黃色火焰,生成淡黃色固體2Na+O2![]() Na2O2
Na2O2
【解析】
Ⅰ. 測定金屬鈉樣品(表面有 Na2O)中鈉單質的質量分數,利用鈉和水反應放出氫氣,而Na2O與水反應生成氫氧化鈉不放出氫氣,反應前A、B 總質量(b g)與金屬鈉樣品質量(a g)之和與反應后 A、B 的總質量( c g)的差,即是生成氫氣的質量,根據鈉和水反應的化學方程式列比例式計算可求出金屬鈉樣品中鈉的質量,然后根據鈉的質量和樣品的質量計算鈉的質量分數;B裝置中無水氯化鈣的作用是吸收氫氣中混有的水蒸氣,減少實驗誤差。
II.用金屬鈉和空氣制備 Na2O2,化學方程是為2Na+O2![]() Na2O2,現象為熔化成光亮的小球,劇烈燃燒產生黃色火焰,生成淡黃色過氧化鈉固體。因為Na2O2 可以與 H2O、CO2 反應,設計裝置I用氫氧化鈉溶液吸收CO2,用裝置IV裝有濃硫酸干燥氧氣,裝置III中盛有堿石灰可防止空氣中水蒸氣進入反應裝置II,據此分析。
Na2O2,現象為熔化成光亮的小球,劇烈燃燒產生黃色火焰,生成淡黃色過氧化鈉固體。因為Na2O2 可以與 H2O、CO2 反應,設計裝置I用氫氧化鈉溶液吸收CO2,用裝置IV裝有濃硫酸干燥氧氣,裝置III中盛有堿石灰可防止空氣中水蒸氣進入反應裝置II,據此分析。
Ⅰ.(1)因為與水反應放熱以及鈉的熔點低,所以鈉熔化成閃亮的小球,
故答案為:該反應為放熱,鈉的熔點低;
(2)設Na的質量為xg,則
2Na+2H2O=2NaOH+H2↑
46 2
xg a+b-c
![]() =
=![]() ,
,
則x=23(a+b-c)
則其質量分數為![]() 100%,
100%,
故答案為:![]() 100%;
100%;
(3)沒有B裝置,生成的氫氣會帶走一部分水蒸氣,造成c減小,使質量分數增大,
故答案為:偏大;
Ⅱ.(4)裝置Ⅳ裝有濃硫酸,用途為吸收反應氣體中的水蒸氣,由于水和二氧化碳與過氧化鈉反應,而要求制得較純的過氧化鈉,則Ⅰ為吸二氧化碳,Ⅳ為吸水蒸氣,應將Ⅳ接在Ⅰ與Ⅱ之間,并長進短出,故選B,
故答案為:濃硫酸;B;
(5)鈉在氧氣中燃燒的現象為熔化成光亮的小球,劇烈燃燒產生黃色火焰,生成淡黃色過氧化鈉固體,
故答案為:鈉熔化成光亮的小球,劇烈燃燒產生黃色火焰,生成淡黃色固體;
(6)鈉與氧氣反應生成過氧化鈉,反應為:2Na+O2![]() Na2O2,
Na2O2,
故答案為:2Na+O2![]() Na2O2。
Na2O2。


 新課標同步訓練系列答案
新課標同步訓練系列答案 一線名師口算應用題天天練一本全系列答案
一線名師口算應用題天天練一本全系列答案科目:高中化學 來源: 題型:
【題目】在標準狀況下,將 V L 氣體 A(摩爾質量為 Mg·mol-1)溶于 0.1L 水中,所得溶液密度為dg·cm-3,則該溶液的物質的量濃度為
A. 1000Vd/(MV+2240)mol·L-1 B. Vd/(MV+2240)mol·L-1
C. 1000VdM/(MV+2240)mol·L-1 D. MV/[22.4(V+0.1)d]mol·L-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】綠色化學又稱環境友好化學,它的主要特點之一是提高原子的利用率,使原料中所有的原子全部 轉化到產品中,實現“零排放”。下列反應符合綠色化學這一特點的是
A. 工業冶煉 Fe2O3+3CO ![]() 2Fe+3CO2
2Fe+3CO2
B. 用生石灰制熟石灰 CaO+H2O=Ca(OH)2
C. 實驗室制取二氧化碳 CaCO3+2HCl=CaCl2+H2O+CO2↑
D. 實驗室制取氫氣 Zn+H2SO4=ZnSO4+H2↑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】全釩氧化還原電池是一種新型可充電池,不同價態的含釩離子作為正極和負極的活性物質,分別儲存在各自的酸性電解液儲罐中。其結構原理如圖所示,該電池放電時,右槽中的電極反應為:V2+-e-=V3+,下列說法正確的是

A. 放電時,右槽發生還原反應
B. 放電時,左槽的電極反應式:VO2++2H++e-=VO2++H2O
C. 充電時,每轉移1mol電子,n(H+)的變化量為1mol
D. 充電時,陰極電解液pH升高
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一定體積的密閉容器中,進行如下化學反應:![]()
![]()
![]() ,其化學平衡常數
,其化學平衡常數![]() 與溫度的關系如下表:
與溫度的關系如下表:
℃ | 700 | 800 | 830 | 1000 | 1200 |
| 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
請回答下列問題:
(1)該反應的化學平衡常數表達式為![]() ________.
________.
(2)該反應的逆反應為________反應(選填“吸熱”或“放熱”).
(3)能判斷該反應是否達到化學平衡狀態的依據是________.
a.容器內壓強不變
b.混合氣體中![]() 不變
不變
c.![]()
d.![]()
(4)某溫度下,平衡濃度符合![]() ,試判斷此時的溫度為________℃.
,試判斷此時的溫度為________℃.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學欲配制符合下列條件的溶液,其中可能實現的是
A. 只含0.1 mol Na+、0.2mol Mg2+、0.1 mol Cl-和0.1 mol NO3-的溶液
B. 只含0.1mol NH4+、0.1 mol Ca2+、0.1 mol CO32-和0.1mol Cl-的溶液
C. 在標準狀況下,將VL氣體(摩爾質量是M g/mol)溶于0.1L水中,所得溶液的密度為d g/mL,則此溶液的物質的量濃度為1000Vd/(2240+VM)mol/L
D. 可用1000mL容量瓶、燒杯、玻璃棒、量筒、58.5gNaCl固體和水配制1L1mol/L的NaCl溶液
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列反應屬于吸熱反應的是( )
A.鋅粒與稀H2SO4反應B.鹽酸與氫氧化鈉溶液反應
C.甲烷在空氣中燃燒D.Ba(OH)2·H2O晶體與NH4Cl晶體的反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】熏衣草醇( 結構如圖) 可以用于高級化妝品及香水的香料。下列有關熏衣草醇的說法正確的是
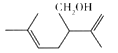
A. 熏衣草醇的分子式為C10H16O
B. 薰衣草醇能發生加成反應和酯化反應
C. 熏衣草醇分子中所有碳原子可能處于同一個平面
D. 熏衣草醇使溴水和酸性KMnO4 溶液褪色的原理相同
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com