
【題目】某課外活動小組用如圖裝置進行實驗,試回答下列問題:

(1)若開始時開關K與a連接,則B極的電極反應為____________________。
(2)若開始時開關K與b連接,則B極的電極反應為____________________,總反應的離子方程式為____________________。
(3)有關上述實驗,下列說法正確的是______。
A.溶液中Na+向A極移動
B.從A極處逸出的氣體能使濕潤的KI淀粉試紙變藍
C.反應一段時間后加適量鹽酸可恢復到電解前電解質的濃度
D.若標準狀況下B極產生2.24 L氣體,則溶液中轉移0.2 mol電子
(4)該小組同學認為,如果模擬工業上離子交換膜法制燒堿的方法,那么可以設想用如圖裝置電解硫酸鉀溶液來制取氫氣、氧氣、硫酸和氫氧化鉀。
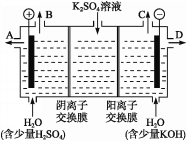
①該電解槽的陽極反應為______________。 此時通過陰離子交換膜的離子數_____(填“大于”“小于”或“等于”)通過陽離子交換膜的離子數。
②制得的氫氧化鉀溶液從出口(填“A”、“B”、“C”或 “D”)________導出。
③電解過程中陰極區堿性明顯增強,用平衡移動原理解釋原因__________________________。
【答案】 Fe-2e- = Fe2+ 2H++2e- = H2↑ 2Cl-+2H2O![]() 2OH-+ H2↑+ Cl2↑ B 2H2O-4e- = 4H++ O2↑ 小于 D H2O
2OH-+ H2↑+ Cl2↑ B 2H2O-4e- = 4H++ O2↑ 小于 D H2O![]() H++ OH-,H+在陰極附近放電,引起水的電離平衡向右移動,使c(OH-)>c(H+)
H++ OH-,H+在陰極附近放電,引起水的電離平衡向右移動,使c(OH-)>c(H+)
【解析】試題分析:
(1) 開關K與a連接時,裝置為原電池,鐵為負極,發生吸氧腐蝕,即電極反應為Fe-2e-=Fe2+。
(2) 開關K與b連接時,裝置為電解池,電解食鹽水,此時陽極A發生2Cl--2e-=Cl2↑,陰極B發生2H++2e-H2↑,總反應的離子方程式為2Cl-+2H2O![]() 2OH-+ H2↑+ Cl2↑。
2OH-+ H2↑+ Cl2↑。
(3)陽離子向陰極移動,A錯誤;陽極A處產生的是Cl2,能使濕潤的KI淀粉試紙變藍,B正確;C應該通入HCl,不能加鹽酸,因為鹽酸是HCl的水溶液,錯誤;D電子不能在溶液中移動,錯誤。
(4))溶液中的OH-在陽極失電子產生O2:4OH--4e-=2H2O+O2↑,所以在B口放出O2,從A口導出H2SO4。溶液中的H+在陰極得到電子產生H2:2H++2e-=H2↑,則從C口放出H2,從D口導出KOH溶液。依據電荷守恒,通過陽離子交換膜的K+是通過陰離子交換膜的SO42-的2倍,所以通過陽離子交換膜的離子數大于通過陰離子交換膜的離子數。③電解過程中,H+在陰極附近放電,引起水的電離平衡向右移動,使c(OH-)>c(H+),故陰極區堿性明顯增強。


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
【題目】(1)物質的量表示______的集合體。
(2)物質的量的符號______;單位______;阿伏加德羅常數的符號______;單位______;通常用______表示。
(3)摩爾質量的符號______;常用單位______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某元素B的核電荷數為Z,已知Bn﹣和Am+的核外具有相同的電子層結構,則A元素的原子序數用Z、n、m來表示,應為( )
A.Z+n﹣m
B.Z+m+n
C.Z﹣n﹣m
D.Z﹣n+m
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】金屬(M)-空氣電池(如圖)具有原料易得、能量密度高等優點,有望成為新能源汽車和移動設備的電源。該類電池在堿性環境下的總反應方程式為:4M+nO2+2nH2O=4M(OH)n。已知:電池的“理論比能量”指單位質量電極材料理論上釋放出的最大電能。下列說法不正確的是( )
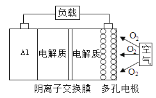
A. 采用多孔電極的目的是提高電極與電解質溶液的接觸面積,并有利于氧氣擴散至電極表面
B. 比較Mg、Al、Zn三種金屬-空氣電池,Al-空氣電池的理論比能量最高
C. M-空氣電池放電過程的正極反應式:4Mn++nO2+2nH2O+4ne–=4M(OH)n
D. 消耗氧氣22.4 L(標準狀況),有4 molOH-從右往左通過陰離子交換膜
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于氯氣的敘述中正確的是( )
A.若氯氣發生泄漏,應立即向下風地區轉移
B.氯氣、氯水和液氯是同一種物質
C.氯氣不能溶于水,所以可用排水法收集
D.用管子把氯氣通入老鼠洞中可以滅鼠
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度時,一定壓強下的密閉容器中發生反應:aX(g)+bY(g) ![]() cZ(g)+dW(g),達平衡后,保持溫度不變壓強增大至原來的2倍,當再達到平衡時,W的濃度為原平衡狀態的1.8倍,下列敘述正確是
cZ(g)+dW(g),達平衡后,保持溫度不變壓強增大至原來的2倍,當再達到平衡時,W的濃度為原平衡狀態的1.8倍,下列敘述正確是
A. 平衡正移 B. Z的體積分數變小
C. (a+b)>(c+d) D. X的轉化率變大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上用鋁土礦(主要成分為Al2O3,含Fe2O3雜質)為原料冶煉鋁的工藝流程如下:

下列敘述正確的是( )
A. 試劑X可以是氫氧化鈉溶液,也可以是鹽酸
B. 反應①過濾后所得沉淀為氫氧化鐵
C. 電解法制取鋁單質時也可以采用電解氯化鋁以降低成本
D. 反應②的化學方程式為NaAlO2+CO2+2H2O===Al(OH)3↓+NaHCO3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在標準狀況下,與16g O2的體積相等的N2為( )
A.體積為22.4LB.分子數為6.02×1024
C.質量為14gD.物質的量為1mol
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com