
【題目】下列各組給定原子序數的元素,不能形成原子數之比為1∶1穩定化合物的是
A.3和17B.1和8C.11和8D.7和12
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】鈦酸鋇是一種強介電化合物材料,具有高介電常數和低介電損耗,是電子陶瓷中使用最廣泛的材料之一,被譽為“電子陶瓷工業的支柱”,工業制取方法如下,先獲得不溶性草酸氧鈦鋇晶體[BaTiO(C2O4)2·4H2O],煅燒后可獲得鈦酸鋇粉體。

(1)酸浸時發生的反應的離子方程式為__________________;
(2)配制TiCl4溶液時通常將TiCl4固體溶于濃鹽酸再加水稀釋,其目的是_________________________;
(3)加入H2C2O4溶液時,發生反應的化學方程式為____________________;可循環使用的物質X是________(填化學式),設計實驗方案驗證草酸氧鈦鋇晶體是否洗滌干凈:_______________________;
(4)煅燒草酸氧鈦鋇晶體得到BaTiO3的同時,生成高溫下的氣體產物有CO、_______和_________;
(5)工業上用飽和Na2CO3溶液處理重晶石(主要成分是BaSO4),待達到平衡后,移走上層清液,重復多次操作,將其轉化為易溶于酸的BaCO3,再由BaCO3制備其它鋇鹽。已知常溫下:Ksp(BaSO4)=1.0×10-10,Ksp(BaCO3)=2.58×10-9,請問至少需要______ mol·L-1的碳酸鈉溶液浸泡才能實現上述轉化(忽略CO32-的水解)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在1200℃時,天然氣脫硫工藝中會發生下列反應
①H2S(g)+3/2O2(g)=SO2(g)+H2O(g)△H1
②2H2S(g)+SO2(g)=3/2S2(g)+2H2O(g)△H2
③H2S(g)+1/2O2(g)=S(g)+H2O(g)△H3
④2S(g)=S2(g)△H4
則△H4的正確表達式為( )
A. △H4=![]() (△H1+△H2-3△H3)B. △H4=
(△H1+△H2-3△H3)B. △H4=![]() (3△H3-△H1-△H2)
(3△H3-△H1-△H2)
C. △H4=![]() (△H1+△H2-3△H3)D. △H4=
(△H1+△H2-3△H3)D. △H4=![]() (△H1-△H2-3△H3)
(△H1-△H2-3△H3)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】[化學——選修3:物質結構與性質]硼及其化合物用途非常廣泛,回答下列問題。
(1)下列B原子電子排布圖表示的狀態中,能量最低和最高的分別為________、________(填標號)
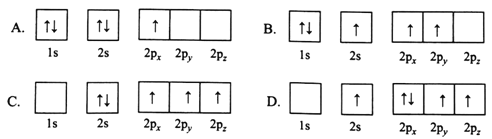
(2)H3BO3是一元弱酸,可用作醫用消毒劑其水溶液呈酸性的原理為:
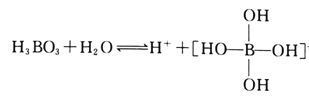
則1mol硼酸分子中含有的共用電子對數為________個。
(3)BF3可用于制造火箭的高能燃料,其分子的空間構型是________________,硼原子雜化方式是________________;BF3能與乙醚發生反應:(C2H5)2O+BF3→BF3·O(C2H5)2,該反應能發生,其原因是________________________________。
(4)硼的一種化合物結構簡式為O=B—CH=C=CH2,該分子中含________個σ鍵。
(5)下圖中圖(a)為類似石墨的六方BN,圖(b)為立方BN。
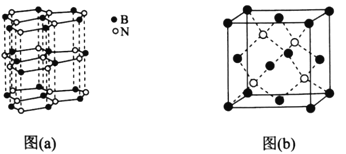
①六方BN具有良好的潤滑性,是因為________________________;六方BN不能像石墨一樣具有導電性,其原因是________________________。
②已知立方BN的晶胞參數為0.3615nm,阿伏加德羅常數的值為NA,則立方BN的密度為________________g·cm-3(列出計算式)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NA表示阿伏加德羅常數的數值,下列說法正確的是
A. 在標準狀況下.11.2L丙烷含有的極性鍵數目為5NA
B. 7g鋰在空氣中完全燃燒時轉移的電子數為NA
C. 1mol葡萄糖(C6H12O6)分子含有的羥基數目為6NA
D. 常溫下,0.2L0.5mol/LNH4NO3溶液中含有的氮原子數小于0.2NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是( )
A.CaO與水反應過程中,有共價鍵的斷裂和形成
B.H2O的熱穩定性比H2S強,是由于H2O的分子間作用力較大
C.KCl、HCl、KOH的水溶液都能導電,所以它們都屬于離子化合物
D.葡萄糖(C6H12O6)、二氧化碳和足球烯(C60)都是共價化合物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】可逆反應 2NO2(g)![]() N2O4 (g)在體積不變的密閉容器中反應,達到平衡狀態的標志是
N2O4 (g)在體積不變的密閉容器中反應,達到平衡狀態的標志是
①單位時間內生成 n mol N2O4 的同時生成 2n mol NO2
②單位時間內消耗 n mol N2O4的同時生成 2n mol NO2
③用NO2、N2O4的物質的量濃度變化表示的反應速率的比為2:1 的狀態
④混合氣體的顏色不再改變的狀態
⑤混合氣體的平均相對分子質量不再改變的狀態
A. ①④⑤B. ②⑤C. ①③④D. ①②③④⑤
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】碳及其化合物在生產、生活中有廣泛的應用,按要求回答問題:
(1)CO2可通過反應CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)轉化成有機物實現碳循環。一定條件下,在體積為1 L的密閉容器中,充入 1 mol CO2和3 mol H2,測得CO2和CH3OH(g)的濃度隨時間變化如圖所示。
CH3OH(g)+H2O(g)轉化成有機物實現碳循環。一定條件下,在體積為1 L的密閉容器中,充入 1 mol CO2和3 mol H2,測得CO2和CH3OH(g)的濃度隨時間變化如圖所示。

從3 min到9 min內,v(H2)=_____mol·L1·min1。平衡時H2的轉化率為________。平衡時混合氣體中CO2(g)的體積分數是________。一定溫度下,第9分鐘時v逆(CH3OH) _______第3分鐘時v正(CH3OH)(填“大于”、“小于”或“等于”)。
(2)如圖,將鋅片、C棒通過導線相連,置于稀硫酸中。

該裝置工作時,溶液中的SO42-向____極(填“C”或“Zn”)移動;電子沿導線流入_______極(填“C”或“Zn”)。寫出正極的電極反應式____。若正極產生11.2L氣體(標況下),則電路中應該有___mol電子發生了轉移。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com