
設NA為阿伏加德羅常數(shù)的值,下列敘述不正確的
| A.5g質量分數(shù)為46%的乙醇溶液中,氫原子的總數(shù)為0.6NA |
| B.5.6 g鐵與0.1 mol氯氣充分反應轉移電子數(shù)為 0.2NA |
| C.50 mL 12 mol?L-1濃鹽酸與足量二氧化錳加熱反應,轉移電子數(shù)為0.3 NA |
| D.常溫常壓下,46g NO2 與N2O4的混合氣體中含有的原子總數(shù)為3NA |
C
解析試題分析:A、5g質量分數(shù)為46%的乙醇溶液中,乙醇的質量=5g×46%=2.3g,物質的量=2.3g÷46g/mol=0.05mol,氫原子的物質的量=0.05mol×6=0.3mol。水的質量=5g-2.3g=2.7g,水的物質的量=2.7g÷18g/mol=0.15mol,氫原子的物質的量=0.15mol×2=0.3mol,所以氫原子總的物質的量是0.6mol,則氫原子的總數(shù)為0.6NA,A正確;B、5.6g鐵的物質的量是0.1mol,與0.1mol氯氣反應時鐵過量,氯氣完全反應,所以反應中轉移電子數(shù)為0.2NA,C不正確;D、NO2與N2O4的最簡式相同,均是NO2,所以46g NO2 與N2O4的混合氣體中含有的原子的物質的量=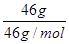 ×3=3mol,其原子總數(shù)為3NA,D正確,答案選C。
×3=3mol,其原子總數(shù)為3NA,D正確,答案選C。
考點:考查阿伏加德羅常數(shù)的有關計算


科目:高中化學 來源: 題型:單選題
某結晶水合物的化學式為R·nH2O,其相對分子質量為M。25 ℃時,a g該晶體能夠溶于b g水中形成V mL溶液。下列關系中不正確的是
A.該溶液中溶質的質量分數(shù)為 |
B.該溶液的物質的量濃度為 |
C.該溶液中溶質與溶劑的質量比為 |
D.該溶液的密度為 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
同溫同壓下,等質量的SO2氣體和SO3氣體相比較,下列敘述中正確的是( )
| A.密度比為4:5 | B.物質的量之比為4:5 |
| C.體積比為1:1 | D.原子數(shù)之比為3:4 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
鎂和鋁分別與等濃度、等體積的過量稀硫酸反應,產生氣體的體積(V)與時間(t)關系如圖。反應中鎂和鋁的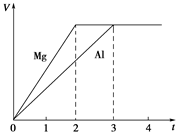
| A.物質的量之比為3∶2 |
| B.質量之比為3∶2 |
| C.摩爾質量之比為2∶3 |
| D.反應速率之比為2∶3 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
用NA表示阿伏加德羅常數(shù),下列敘述中正確的是( )
| A.標準狀況下,22.4L乙醇完全燃燒后生成CO2的分子數(shù)為2NA |
| B.56g的鐵發(fā)生氧化還原反應,一定失去3NA個電子 |
| C.標準狀況下,22.4L氟氣中所含氟原子數(shù)為2NA |
D.0.1mol·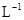 稀硫酸中含有 稀硫酸中含有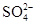 離子數(shù)為0.1NA 離子數(shù)為0.1NA |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
過氧化鈣(CaO2)是一種安全無毒物質,帶有數(shù)量不等的結晶水,通常還含部分CaO。已知:2CaO2·nH2O 2CaO+O2↑+2nH2O,2CaO2+4HCl=2CaCl2+2H2O+O2↑。現(xiàn)稱取2.168 g過氧化鈣樣品分成兩等份進行下列實驗:
2CaO+O2↑+2nH2O,2CaO2+4HCl=2CaCl2+2H2O+O2↑。現(xiàn)稱取2.168 g過氧化鈣樣品分成兩等份進行下列實驗:
實驗一:將一份過氧化鈣樣品充分灼熱,結果得到的O2在標準狀況下體積為134.4 mL。
實驗二:將另一份樣品溶于適量的稀鹽酸中,充分反應后,加入足量的Na2CO3溶液,結果得到1.40 g沉淀。
(1)試計算2.168 g樣品中CaO的質量.
(2)試計算樣品中CaO2·nH2O的n值。
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
往含I-和Cl-的稀溶液中滴入AgNO3溶液,沉淀的質量與加入AgNO3溶液體積的關系如圖所示。則原溶液中c(I-)/c(Cl-)的比值為( ) 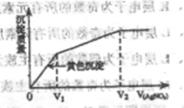
| A.(V2-V1)V1 | B.V1/V2 |
| C.V1/(V2-V1) | D.V2/V1 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
用NA表示阿伏加德羅常數(shù)的值。下列敘述中不正確的是
| A.16. 9 g過氯化鋇(BaO2)固體中陰、陽離子總數(shù)約為0. 2NA |
| B.常溫常壓下,28 g乙烯和環(huán)丁烷(C4H8)的混合氣體中含有的碳原子數(shù)為2 NA |
| C.a g某氣體含分子數(shù)為b,c g該氣體在標況下的體積為22. 4bc/ aNAL |
| D.某密閉容器盛有0. l molN2和0. 3 mol H2,在一定條件下充分反應,轉移電子的數(shù)目為0. 6NA |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列說法正確的是:
①Cl-的結構示意圖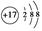 ;
;
②羥基的電子式: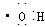 ;
;
③HClO的結構式:H—Cl—O;
④NaHCO3在水中的電離方程式:NaHCO3=Na++H++CO32-;
⑤Na2O的水溶液能導電,這不能說明Na2O是電解質;
⑥SiO2既能與氫氟酸反應又能與NaOH溶液反應,故SiO2是兩性氧化物;
⑦分餾、干餾、裂化都是化學變化( )
| A.①②⑤ | B.①④⑥⑦ | C.②③④⑥ | D.②③⑤⑥⑦ |
查看答案和解析>>
國際學校優(yōu)選 - 練習冊列表 - 試題列表
湖北省互聯(lián)網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com